
- •Конспект лекцій з дисципліни «Біохімічні основи мікробного синтезу» для студентів напряму 6.051401 «Біотехнологія»
- •Тема 1. Транспорт компонентів середовища в клітині мікроорганізмів
- •Тема 2. Компоненти середовища, які містять азот та їх асиміляція мікроорганізмами.
- •Тема 6. Асиміляція вуглеводів мікроорганізмами
- •Тема 10. Основні принципи регуляції обміну речовин у мікроорганізмів
- •Тема 14. Метаболічний фонд мікроорганізмів
- •Тема 15. Мікробіологічний синтез органічних кислот
- •Тема 9. Біосинтези через ацил-КоА
- •Тема 10. Біосинтез циклічних структур через гексозомонофосфатний шлях обміну вуглеводів
- •Тема 12. Біосинтез амінокислот
- •Тема 14. Мікробіологічний синтез пептидів
- •Тема 15. Синтез нуклеотидів, їх похідних та флавінів
- •Глава 16 біосинтез стрептоміцину
- •2. Біосинтез n-метилглюкозаміну та стрептози
- •Глава 23. Коферменти та їх функції
- •Оксиредуктази
- •Трансферази
- •Гідролази
- •Лігази (синтетази)
- •Тема т26. Типи бродіння
- •26.1 Спиртове бродіння
- •26.2 Молочнокисле бродіння
- •26.2.1 Гомоферментативне молочнокисле бродіння
- •26.2.2 Гетероферментативне молочнокисле бродіння
- •26.3 Пропіоновокисле бродіння
- •26.4 Мурашинокисле бродіння
- •26.5. Маслянокисле та ацетоно-бутилове бродіння.
- •19. Перенесення електронів в анаеробних умовах (анаеробне дихання)
- •27.1Денітрифікауія та відновлення нітрату
- •27.2. Утворення сірководню у процесі відновлення сульфату
- •27.3 Утворення метану у процесі відновлення карбонату
- •27.4. Утворення ацетату у процесі відновлення карбонату
- •27.5. Утворення сукцинату у процесі відновлення фумарату
- •27.6 Відновлення іонів Fe (III) до Fe (II)
- •51918, М. Дніпродзержинськ, вул. Дніпробудівська,2
Гідролази
![]()
На відміну від усіх інших класів ферментів гідролази не потребують в коензимах.
Ліази
Ліази-ферменти, які розривають С-С, С-О, С-N та інші зв’язки в реакціях, які не являються гідролітичними або окислювальними. Ці ферменти відрізняються від інших тим, що в каталізуючих ними реакціях в одному напрямлені приймають участь два субстрати, а в зворотньому- тільки один. При дії на один субстрат від нього відщеплюється молекула з утворенням ненасиченого залишку. До числа ферментів, що відносяться до ліаз, приналежать декарбоксилази, дезамінази, альдолази та кетолази.
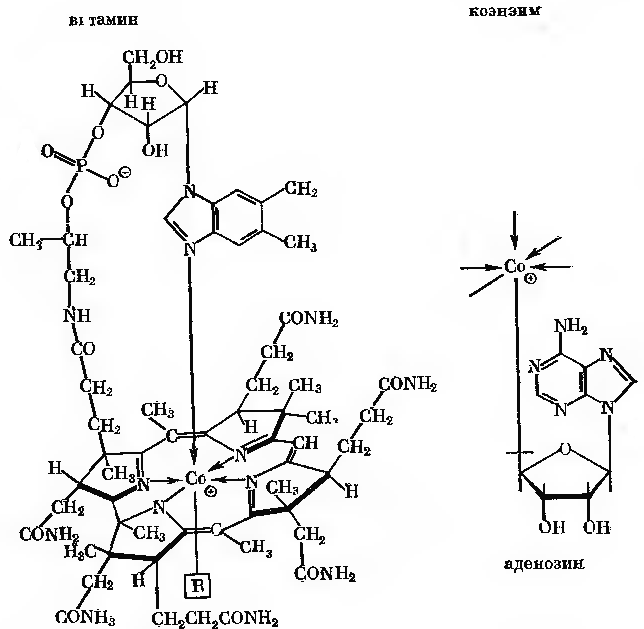
Реакція
![]()
Деякі декарбоксилази та транскетолази використовують тіамінпірофосфат в якості коензиму.
Приклад дії карбоксилази:
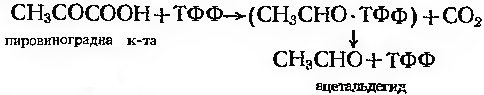
Транскетолаза:
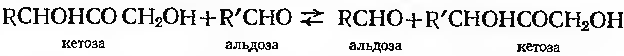
Деякі дезамінази використовують в якості коензиму піридоксальфосфат.
Приклади дії сериндегідратази:
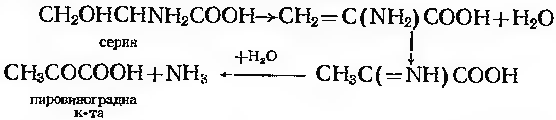
Цистеїндесульфураза:
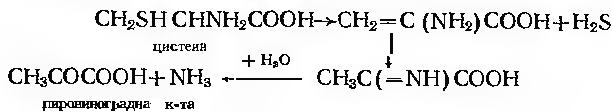
Ізомерази
Ізомерази каналізують перетворення, які відбуваються в межі однієї молекули:
![]()
До їх числа відносяться рацемази та епімерази, наприклад аланінрацемаза:
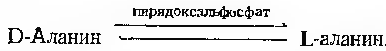
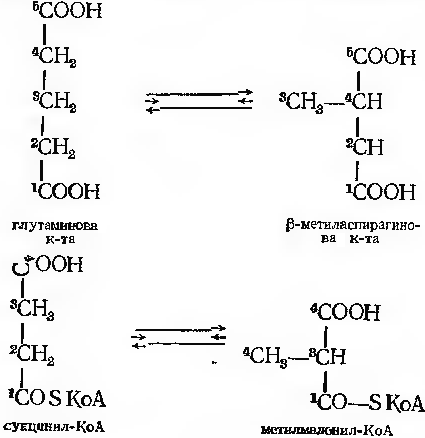
Присутність кобамідного коферменту потребує деякі мутази, наприклад метиласпартатмутаза або метитмалоніл-КоА мутаза:
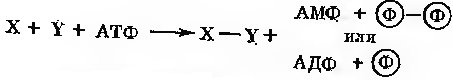
Можливий механізм
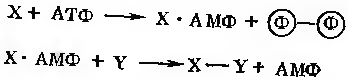
Пиклади дії ізомераз, в яких приймає участь коензим В12:
Лігази (синтетази)
Лігази представляють собою ферменти, які каналізують сполуки двох молекул, сполучене з гідролізом пірофосфатного зв’язку в молекулі АТФ або аналогічного три фосфату. Утворені при цьому зв’язки часто є високоенергетичними:

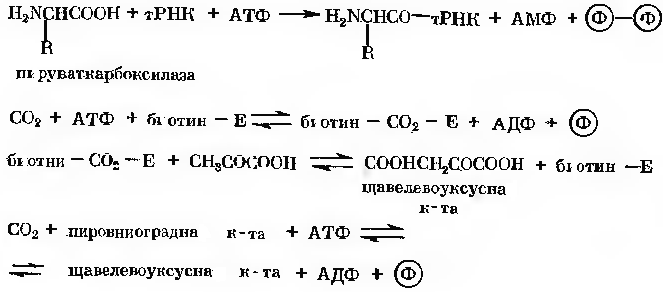
Приклад дії ферментів, активуючих амінокислоти:
![]()
У
даному випадку фермент має біотин в
якості простатичної групи. Карбоксильна
група біотину має зв’язок з
![]() групою
залишку лізину в молекулі ферменту.
групою
залишку лізину в молекулі ферменту.
Тема т26. Типи бродіння
Із трьох принципово можливих способів регенерації АТФ (дихання, бродіння та фотосинтез) бродіння найпростіший.
Бродіння — це такий метаболічний процес, у якому регенерується АТФ, а продукти розщеплення органічного субстрату можуть служити одночасно і донорами, і акцепторами водню. Загальна схема бродіння показана на рис. 26.1. Органічний субстрат є джерелом енергії та вуглецю. Реакції синтезу АТФ є реакціями окиснення. Від окисненого вуглецю клітина позбавляється, виділяючи С02. Окремі етапи окиснення являють собою дегідрування, за якого водень переноситься на НАД. Акцепторами водню, який міститься у вигляді НАДН, є проміжні продукти розщеплення субстрату. За рахунок НАДН ці проміжні продукти відновлюються, а продукти відновлення виводяться з клітини.
У процесі зброджування вуглеводів та інших субстратів утворюються (окремо чи в суміші) такі продукти, як етанол, лактат (молочна кислота), пропіонат, форміат, бутират, сукцинат, ацетат, н-бутанол, 2,3-бутандіол, ацетон, 2-пропанол, С02 та Н2. Залежно від того, які продукти переважно утворюються, розрізняють спиртове, молочнокисле, маслянокисле, пропіоновокисле, мурашинокисле та оцтовокисле бродіння. Молекулярний кисень у процесах бродіння участі не бере. Більшість мікроорганізмів, які здійснюють бродіння, є облігатними анеробами або факультативними аеробами, здатними рости як у присутності кисню, так і без нього. При цьому кисень пригнічує бродіння, і воно змінюється диханням.
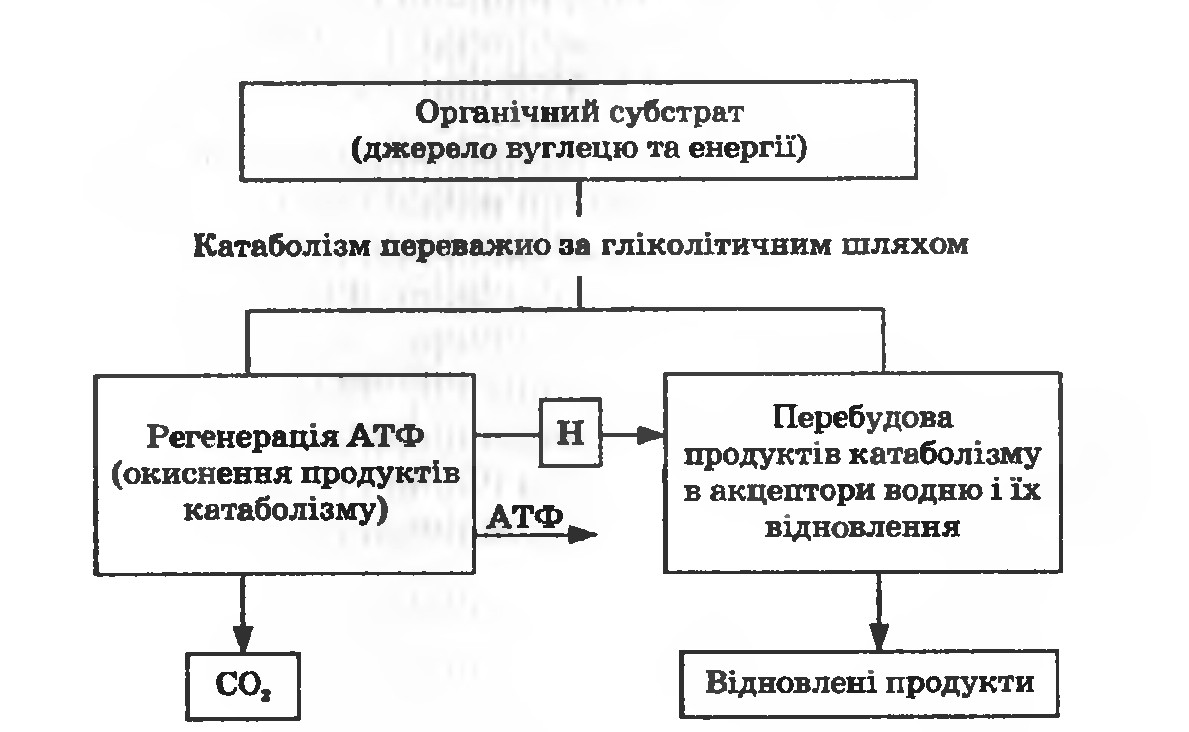
Рисунок 26.1 – Загальна схема бродіння
У процесі зброджування глюкози утворюється від одного до чотирьох молей АТФ. У фосфорилюванні на рівні субстрату беруть участь такі три найважливіші реакції:
1,3-Дифосфогліцерат + АДФ → 3-Фосфогліцерат + АТФ
(фосфогліцераткіназа);
Фосфоенолпіруват + АДФ → Піруват + АТФ (піруваткіназа);
Ацетилфосфат (бутирилфосфат) + АДФ →
→Ацетат (бутират) + АТФ (ацетаткіназа).
У більшості мікроорганізмів використовуються перші дві реакції. При цьому необхідні акцептори водню утворюються з пірувату або ацетил-КоА. У процесі зброджування одного моля глюкози утворюється лише два або три моля АТФ, а продуктами бродіння є лактат, етанол, ацетон, бутират, н-бутанол, 2-пропанол, 2,3-бутандіол, капронат, ацетат, С02 та Н2.
При використанні третьої реакції, яка каталізується ацетат-кіназою, утворюється додатковий АТФ. Ацетилфосфат утворюється з ацетил-КоА за допомогою фосфотрансацетилази:
Ацетил-КоА + Фн → Ацетилфосфат + КоА.
Крім того, можливе утворення ацетилфосфату з фосфорильованих сахаридів (ксилулозо-5-фосфату, фруктозо-6-фосфату) за участю фосфокетолази.
