
- •Факторы риска или потенциальные причины ошибок по gmp:
- •Асептическое производство
- •Обеспечение чистоты воздуха
- •Рациональное зонирование помещений (по функциям);
- •Приточная система на базе центрального кондиционера, обеспечивающая:
- •Подготовка воздуха
- •1.Метод мембранной фильтрации
- •2.Метод прямого посева
ИСТОРИЯ ИНЪЕКЦИОННЫХ ЛЕКАРСТВ
1851г. - подкожные впрыскивания (барометрические трубки с поршнем и серебряным наконечником), доктор А.П. Лазарев (Владикавказский военный госпиталь).
1852 г. – чешский ученый К. Правац сконтструировал шприц с иглой (Шарль-Габриель, француз)
1855 г. – A.Wood, injectiones subcutane (экстракты, настойки, растворы)
1885 г. – ампулы в качестве сосудов для стерильных растворов предложил петербургский фармацевт проф. А.П.Пель (Фридлендер, Марпманн, Лютце, Бернатуик, Лимузин) А.Пель - внедрение асептики («сулемовая комната»)
Характеристика
Преимущества
Быстрота действия
Высокая биологическая доступность
Точность и удобство дозирования
Введение больным в любом состоянии
Отсутствие влияния ЖКТ
Крупносерийное производство
Недостатки
вероятность постинъекционных осложнений (сепсис, эмболии и др.)
болезненность введения
сложность введения (умения и наличие приспособлений)
высокие требования к производству
высокая стоимость единицы продукции
Общие требования к лекарственным средствам для парентарального применения
Стерильность
Отсутствие механических включений
Апирогенность
Нетоксичность
Стабильность
Объем
Содержание лекарственного вещества
Изотоничность
рН (изогидричность)
Изоионичность
---
ЛЕКАРСТВЕННЫЕ ФОРМЫ ДЛЯ ИНЪЕКЦИИ - стерильные лекарственные формы для парентерального применения в виде растворов, суспензий, эмульсий, а также твердых лекарственных веществ (порошки, таблетки, пористые массы), которые растворяют в стерильном растворителе непосредственно перед введением. Различают инъекции малого объема до 100 мл, и большого объема 100 мл и более (инфузии).
ПОРОШКИ ДЛЯ ИНЪЕКЦИЙ - стерильные твердые лекарственные средства, применяемые для приготовления растворов или суспензий для инъекций.
РАСТВОРЫ ДЛЯ ИНЪЕКЦИЙ - стерильные водные или неводные растворы лекарственных веществ в соответствующем растворителе.
СУСПЕНЗИИ ДЛЯ ИНЪЕКЦИЙ - стерильные высокодисперсные суспензии.
ЭМУЛЬСИИ ДЛЯ ИНЪЕКЦИЙ - стерильные высокодисперсные эмульсии.
(ОСТ 91500.05.001-00 ОТРАСЛЕВОЙ СТАНДАРТ
СТАНДАРТЫ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ.
ОСНОВНЫЕ ПОЛОЖЕНИЯ)
Факторы риска или потенциальные причины ошибок по gmp:
Материалы – это сырьё (активное и неактивное), тара и упаковка, этикетки и маркировка, сопутствующие материалы, конечные партии продуктов, вспомогательные материалы и др.
Механические средства – это здания, оборудование, станки, аппаратура.
Методы и процедуры – это технологии, общие и рабочие формулы, инструкции и др.
Персонал – группа людей, имеющая специальное образование и способная выполнять операции, связанные с производством ЛС, упаковкой, контролем качества, складированием, реализацией, обслуживанием, ремонтом и др.
ТРЕБОВАНИЯ К УПАКОВКЕ должна быть:
герметичной и защищать от воздействия внешней среды в процессе транспортировки и хранения (непроницаема для паров воды, газов);
химически индифферентной, не взаимодействовать с содержимым упаковки, не должна поглощать или выделять каких-либо соединений, подвергаться микробной контаминации;
прочной, небьющейся, выдерживать напряжения и удары;
сохранять стабильность и фармакотерапевтические свойства ЛС при хранении не менее трёх лет.
простой в обращении;
носителем информации (нормативной, рекламной и эстетической);
технологичной, вписываться в технологический процесс, интенсифицируя производительность труда;
экономически целесообразной
Стекло медицинское
ТРЕБОВАНИЯ
прозрачность
бесцветность
легкоплавкость
химическая устойчивость
(водостойкость, щелочестойкость)
механическая прочность
Ампулы требования
химическая устойчивость(рН)
термическая устойчивость
остаточное напряжение
светозащитные свойства
Сила излома (с кольцом)
Радиальное биение стебля
Кварцевый песок (SiO2)
Нефелин (KNa3[AlSiO4]4)
Доломит (CaCO3, MgCO3)
Бура (Na2B4O7)
Известняк (CaCO3
Поташ (K2CO3)
Кислота борная (HBO3)
Сода кальцинированная (Na2CO3)
Марки и состав ампульного стекла (ГОСТ 19808-86)
Марки стекла |
Состав стекла, % от массы |
||||||||
SiO2 |
Al2O3 |
B2O3 |
CaO± MgO |
Na2O |
K2O |
Fe2O3 |
MnO |
BaO |
|
НС-3 |
72,8 |
4,5 |
6,0 |
6,9 |
8,1 |
1,7 |
- |
- |
- |
НС-1 |
73,0 |
4,5 |
4,0 |
8,0 |
8,5 |
2,0 |
- |
- |
- |
СНС-1 |
67,0 |
4,1 |
5,2 |
6,3 |
7,5 |
2,0 |
2,9 |
5,0 |
- |
АБ-1 |
73,0 |
3,0 |
- |
9,5 |
13,5 |
1,0 |
- |
- |
- |
МТО |
73,0 |
1,5 |
- |
10,0 |
15,5 |
- |
- |
- |
- |
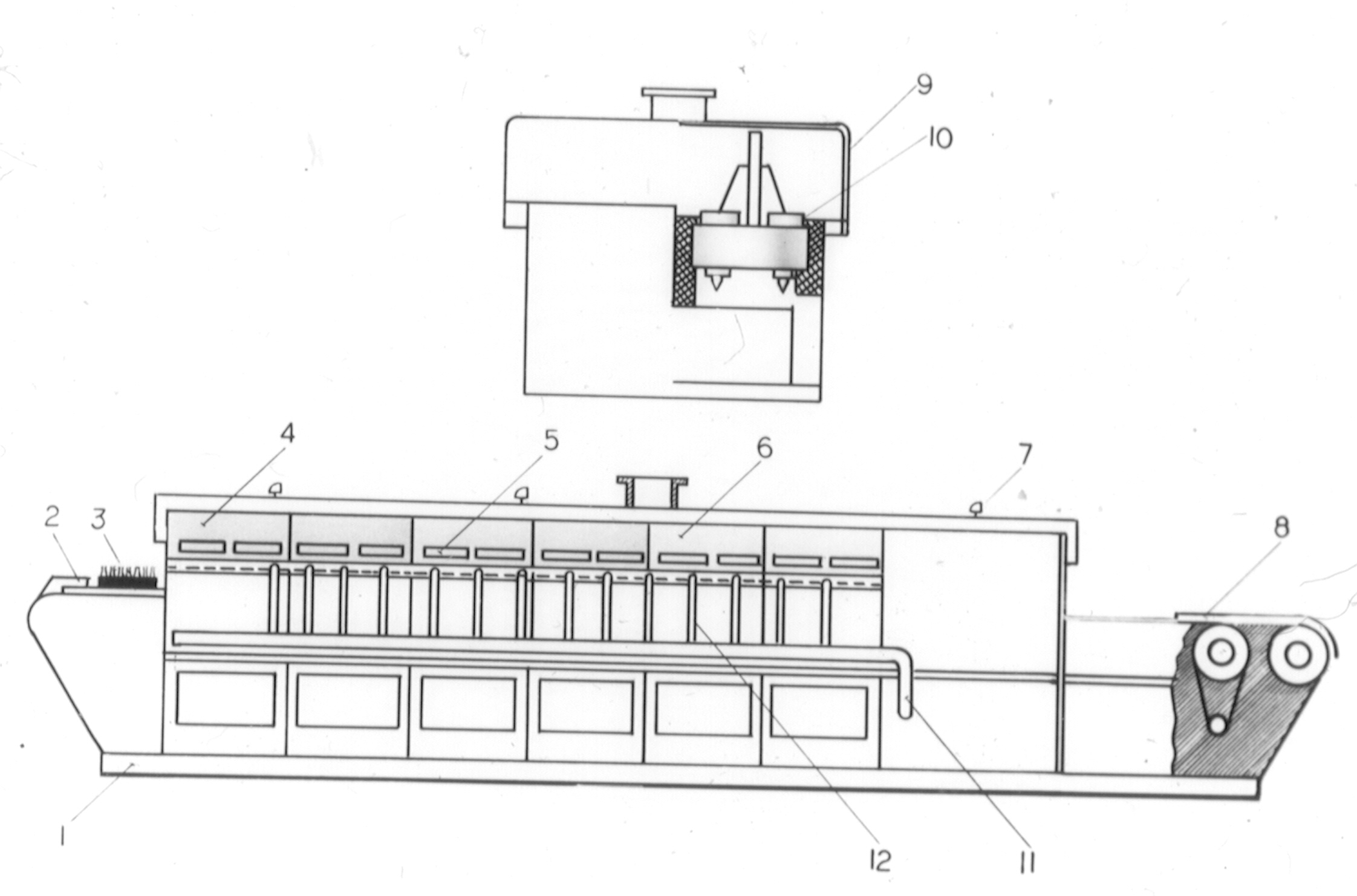
Изготовление стеклодрота
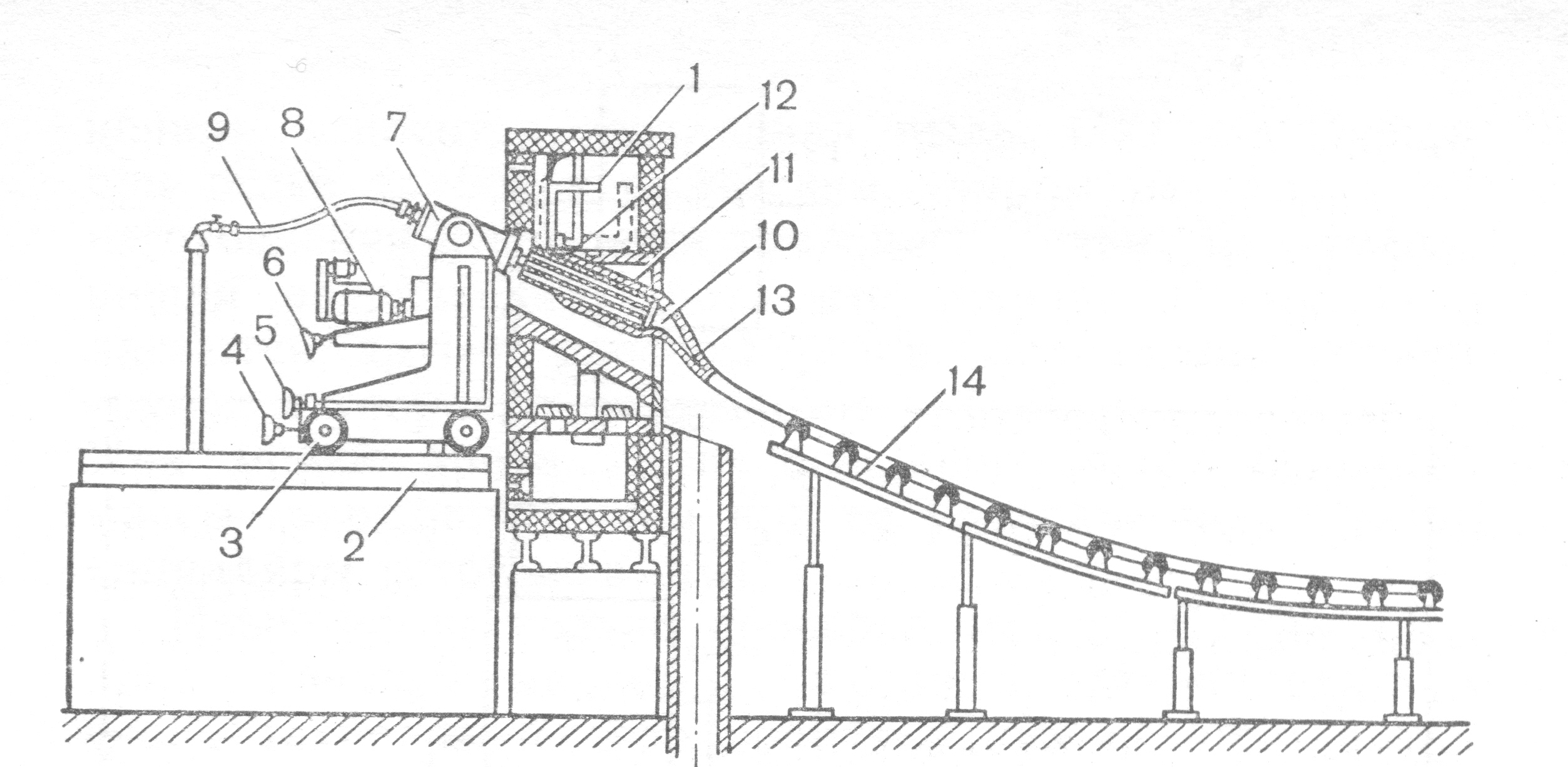
1- питатель стекломассы,7- шпиндель, 8 – шланг подачи воздуха
10 – труба из жаропрочной стали, 11 – вращающийся керамический мундштук
Калибровка дрота
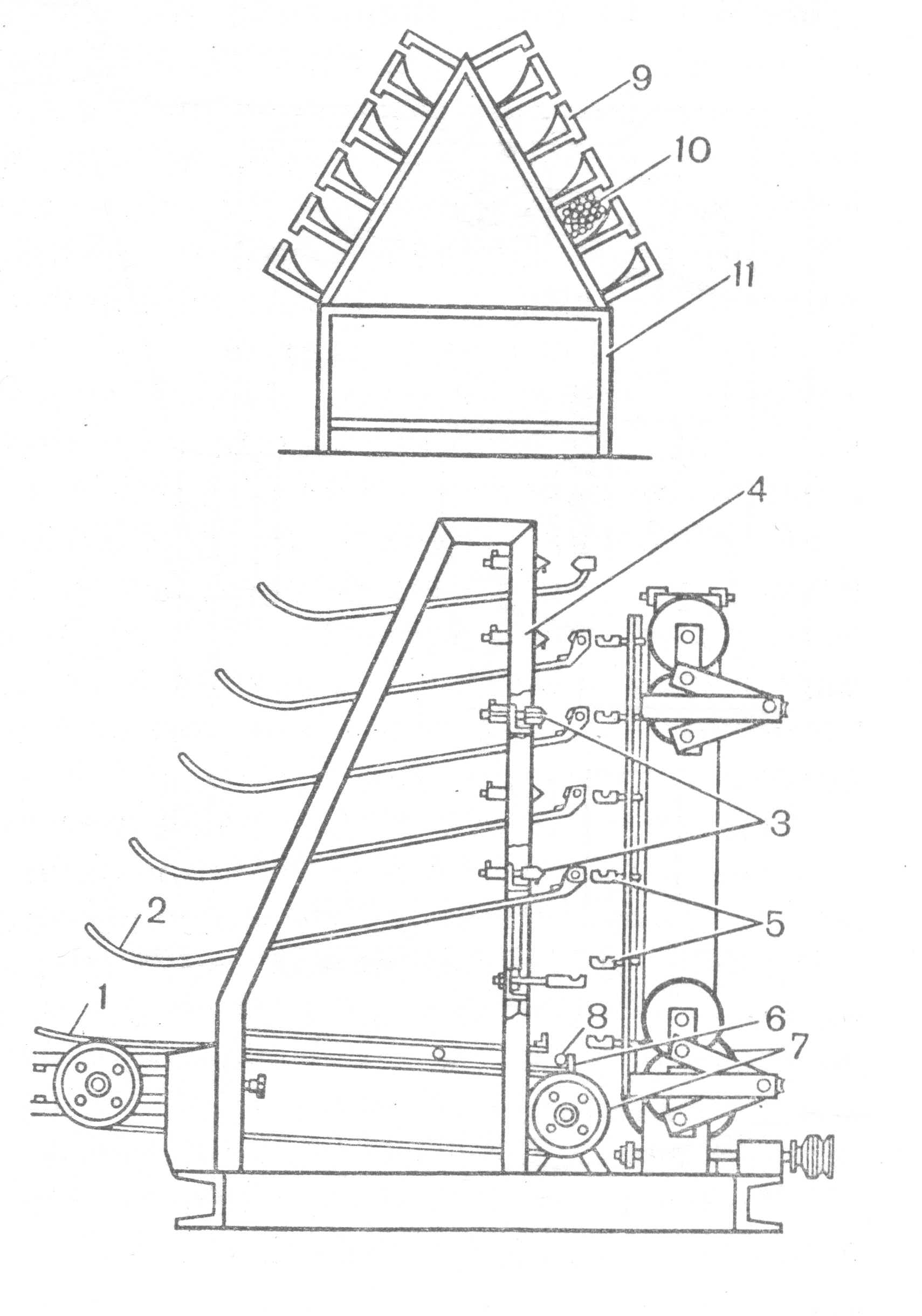 (оценка
качества)
(оценка
качества)
чистота поверхности
длина
кривизна
конусность
отсутствие включений
толщина стенок (по массе)
наружный диаметр
Мойка дрота
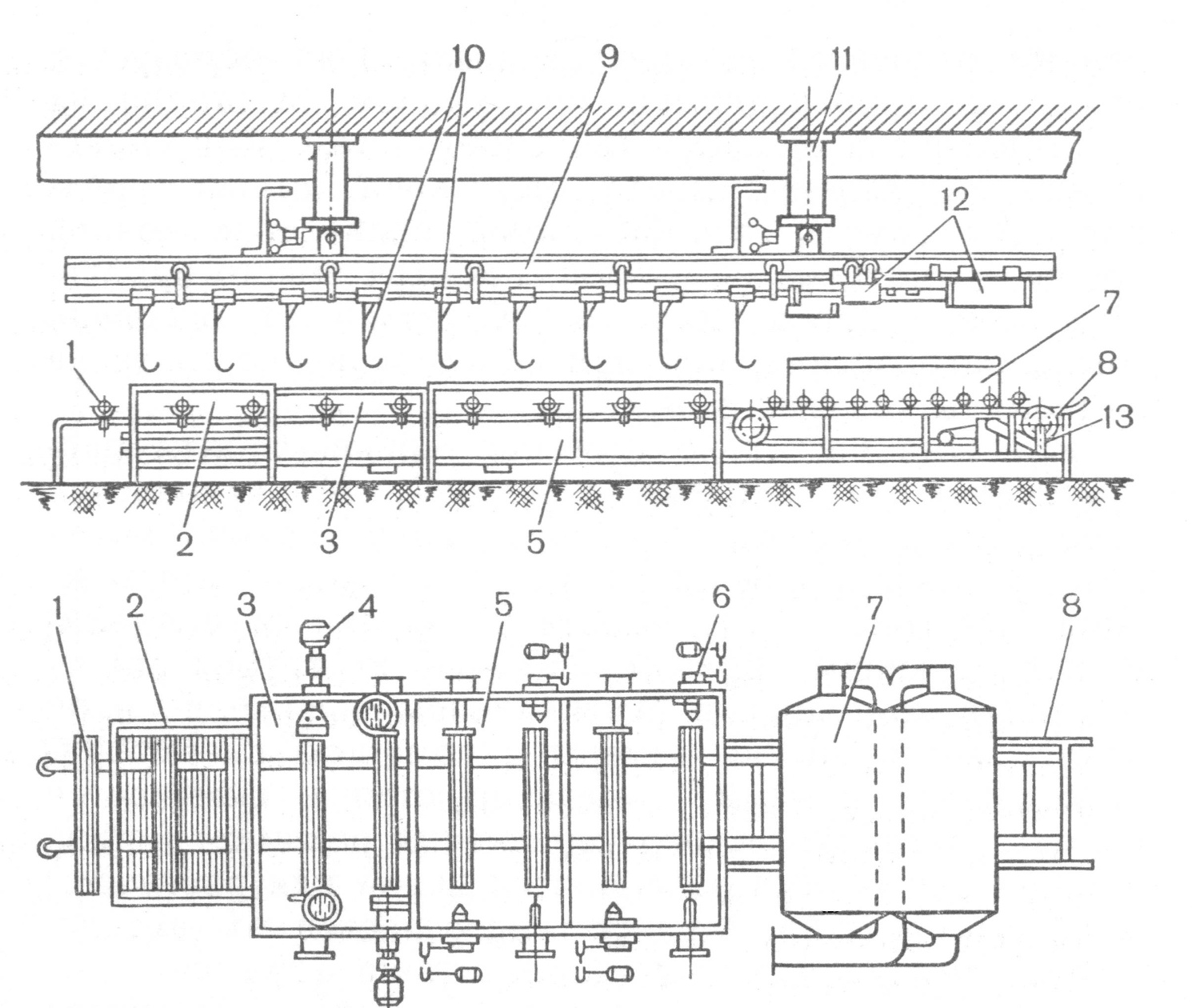
Поточная линия камерной горизонтальной мойки
----
Выделка ампул
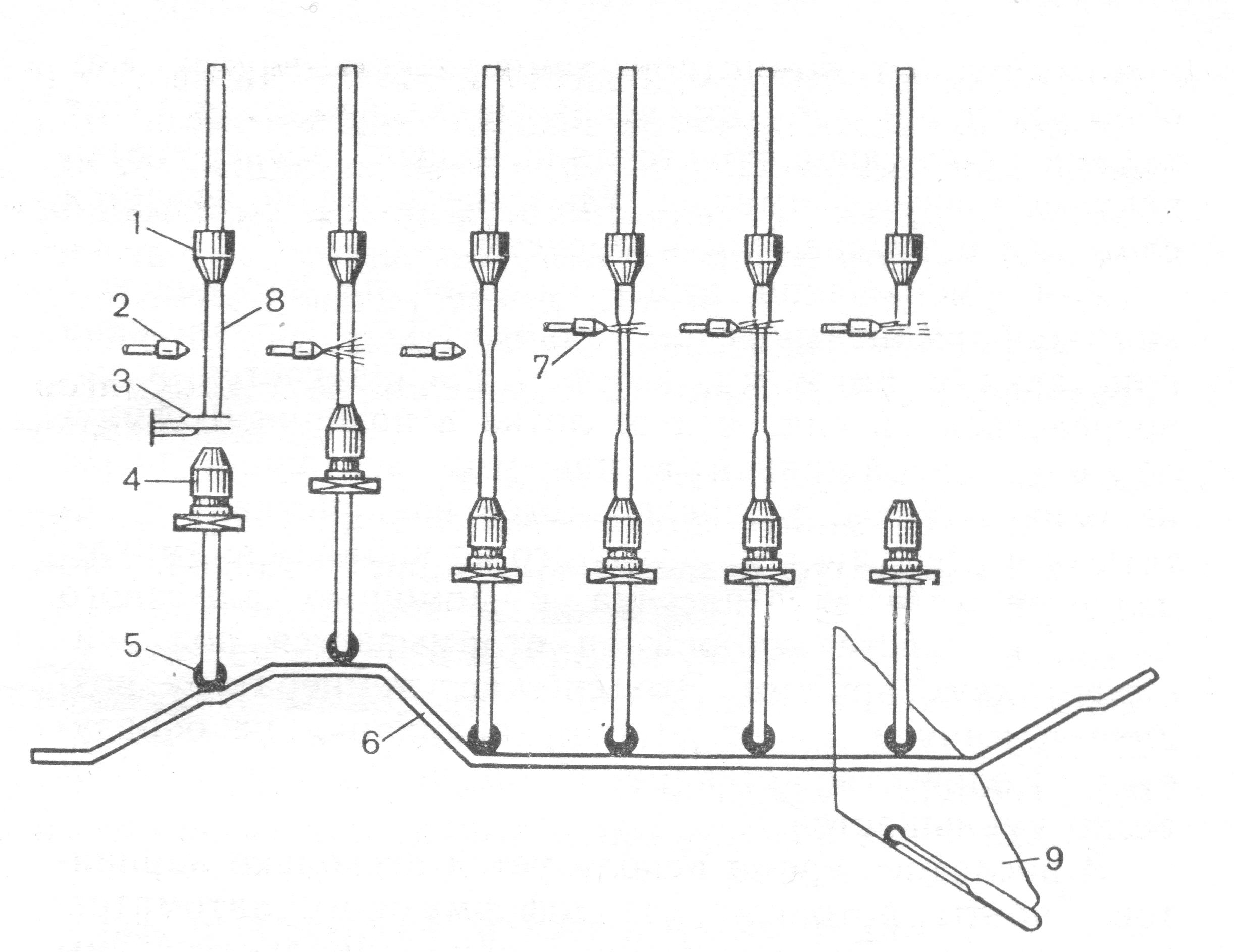

Отжиг ампул
Контроль – полярископ-поляриметр (ПКС-125, ПКС-250),
удельная разность хода лучей не более 8 млн-1
Свечение: красно-фиолетовое – хорошо
красно-оранжевое – удовлетворительно
желтое, зеленое, голубое - неудовлетворительно
Мойка ампул (наружняя, внутр.) смотреть методичку
-----
Полимерные упаковки
"выдувание - наполнение - герметизация"
меньшая масса
меньшая хрупкость
технологичность
низкая стоимость
паро-, влагопроницаемость
стабильность
прозрачность
санитарно-химические характеристики
диффузия ЛВ внутрь упаковки
Факторы риска или потенциальные причины ошибок по GMP:
Материалы – это сырьё (активное и неактивное), тара и упаковка, этикетки и маркировка, сопутствующие материалы, конечные партии продуктов, вспомогательные материалы и др.
Механические средства – это здания, оборудование, станки, аппаратура.
Методы и процедуры – это технологии, общие и рабочие формулы, инструкции и др.
Персонал – группа людей, имеющая специальное образование и способная выполнять операции, связанные с производством ЛС, упаковкой, контролем качества, складированием, реализацией, обслуживанием, ремонтом и др.
--
НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ П Р А В И Л А производства и контроля качества лекарственных средств Good Manufacturing Practice For Medicinal Products (GMP) ГОСТ Р 52249-2009
Приложение 1
ПРОИЗВОДСТВО СТЕРИЛЬНЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ
Принципы
Общие положения
Классификация чистых помещений и чистых зон
Текущий контроль чистых помещений и чистых зон
Изолирующая технология
Технология "выдувание - наполнение - герметизация"
Продукты, подлежащие финишной стерилизации
Персонал
Помещения
Оборудование
Очистка и дезинфекция
Технологический процесс
Стерилизация
Термическая стерилизация
Влажное тепло (пар)
Радиационная стерилизация
Завершающие операции по приготовлению стерильной продукции
Контроль качества
Процессы производства стерильных ЛС
предусматривающие финишную стерилизацию (т.е. стерилизацию в герметичной первичной упаковке);
проводимые в асептических условиях на одном или всех этапах производства.
Оснащенное состояние - состояние, в котором чистое помещение построено и функционирует, технологическое оборудование полностью укомплектовано, но персонал отсутствует.
Эксплуатируемое состояние - состояние чистого помещения, в котором технологическое оборудование функционирует в требуемом режиме с заданным числом работающего персонала.
Соответствие концентрации частиц в оснащенном состоянии заданным требованиям должно достигаться после короткого времени восстановления 15 - 20 мин (рекомендуемое значение) при отсутствии персонала после завершения работы.
Квалификация помещений
А - локальная зона для проведения операций, представляющих высокий риск для качества продукции (зоны вскрытия ампул и флаконов, наполнения, укупорки, соединения частей оборудования в асептических условиях)
обеспечивается однонаправленным (ламинарным) поток воздуха, обеспечивающий в незамкнутой чистой зоне однородную скорость 0,36- 0,54 м/с, фильтр НЕРА(High-efficiency Particle Air − высокоэффективной очистки воздуха) с эффективностью 99,97 %
В - зона, непосредственно окружает зону А и предназначена для асептического приготовления и наполнения; мойки и стерилизации вспомогательных материалов
С и D - чистые зоны для выполнения менее ответственных стадий производства стерильной продукции (мойка дрота, выделка ампул и др.)
Непрерывный контроль концентрации частиц в зонах А и В
эффективность фильтров не менее 99,95%,
скорость воздуха в помещении 0,1-0,2 м/с,
перепад давления воздуха в помещениях 10-15 (50) Па,
кратность воздухообмена не менее 10 час-1
(В зонах B, C и D кратность воздухообмена должна определяться с учетом размеров помещения, находящегося в нем оборудования и персонала.
