
- •Учебно-методическое пособие к практическому занятию по теме: «Культивирование клеток и моделирование повреждения клеточной мембраны»
- •Культивирование клеток
- •Преимущества культуры клеток тканей
- •Ограничения культуры клеток
- •Типы культур клеток тканей
- •Повреждающее действие пероксида водорода на клетку (перитонеальный макрофаг)
- •Материалы
- •Процедура
- •Методические указания к практическому занятию по теме: «Культивирование клеток и моделирование повреждения клеточной мембраны»
- •Блок - информации
- •Виды повреждающих факторов:
- •Проявления повреждения клетки:
- •Отличительные особенности свободных радикалов
- •Наиболее распространенные в организме формы свободных радикалов
- •Образование активных форм кислорода и перекисное окисление липидов
Типы культур клеток тканей
Существует два основных типа культуры клеток тканей: органная культура и культура клеток.
(1) Органная культура сохраняет, по крайней мере, частично характерные особенности архитектуры ткани in vivo. Ткань органа культивируется на поверхности раздела жидкость - газ (на плоту, решетке или геле), что благоприятствует сохранению сферической или трехмерной формы. Вследствие сохранения клеточных взаимодействий, встречающихся в ткани, из которой была получена культура, органные культуры сохраняют отличительные черты этой ткани. Эта культура не может размножаться. В отличие от культуры клеток, каждый эксперимент с органной культурой требует нового культивирования. Поэтому количественный анализ является более сложным. Тем не менее, органные культуры сохраняют гистологические взаимодействия, без которых сложно воспроизводить характерные особенности ткани.
(2) Культура клеток подразумевает культивирование изолированных клеток на твердой подложке в состоянии монослоя или как суспензия в среде культивирования. Культуры клеток могут быть получены из ткани или дисперсионных суспензий клеток. Деление клеток в условиях культуры клеток происходит значительно быстрее, чем в органной культуре. Благодаря этому возможно быстрое воспроизведение линий клеток. Клеток монослоя или суспензии могут быть перенесена, или другими словами субкультивированна, в новую посуду. Это процесс называется термином «пассаж». Дочерняя культура, полученная таким образом, дает начало линии клеток.
Повреждающее действие пероксида водорода на клетку (перитонеальный макрофаг)
(Практическая часть занятия)
Цель опыта: приобрести навыки выделения и работы с первичной культурой клеток. Изучить влияние повреждающего действия активных форм кислорода на мембранные структуры клетки.
Приборы и материалы: 1 мышь весом 15-20 гр., лоток, бикс, препаровальный столик, булавки, ножницы глазные, пинцет анатомический, шприц инсулиновый, шприц 5 мл, камера Горяева, микроскоп, пипетки лабораторные, штативы пробирочные и для эппендорфов, эппендорфы, маркер.
Реактивы: физиологический раствор, хлоралгидрат из расчета 35 мг/100 г веса, синь трепановая, пероксид водорода 3%, бензоат натрия.
Ход работы:
1. Наркотизируем мышь.
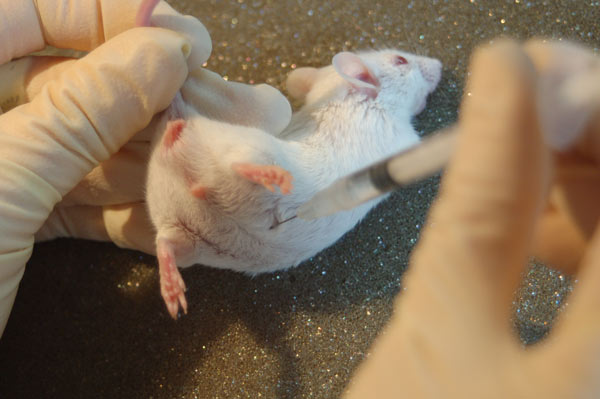
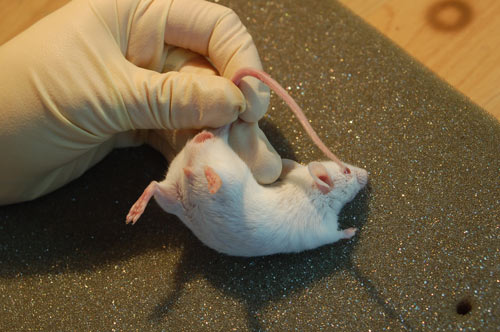
Для этого берем мышь большим и указательным пальцами за хвост, ближе к основанию и сажаем ее на клетку или ровную поверхность. Прижимаем мышь безымянным пальцем, приподнимаем хвост и делаем укол инсулиновым шприцом (0,1 мл р-ра хлоралгидрата) в нижнюю часть живота, стараясь не проникать иглой глубоко.
2. Закрепляем мышь на препаровальном столе булавками. Пинцетом аккуратно подхватываем и приподнимаем шкурку немного ниже грудины.
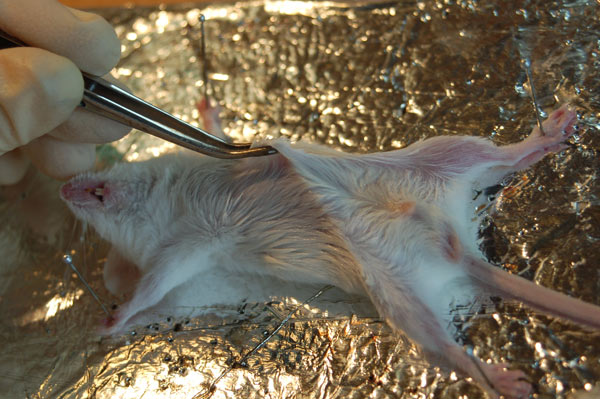
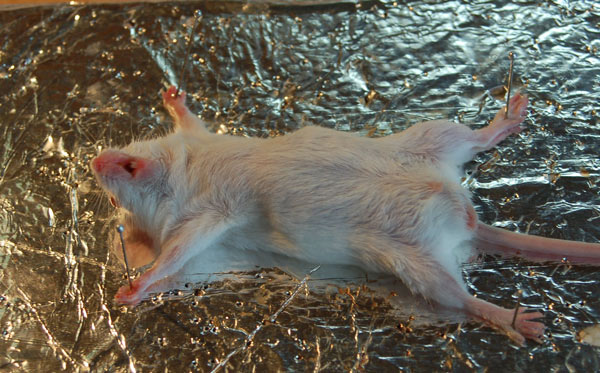
-
3. Ножницами делаем надрез и аккуратно удаляем волосистый покров с брюшка.
4. Прокалываем иглой (5 мл шприца) брюшину и вводим 5 мл физ. раствора, не вынимая иглу.

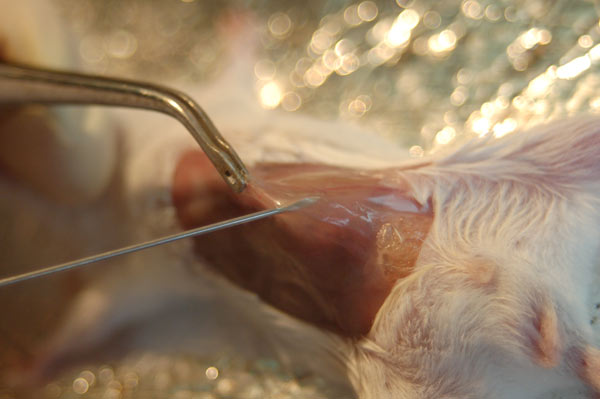
-
5. Массируем пальцами брюшную полость в течение 1,5-2 минут.
6. Откачиваем шприцом жидкость.
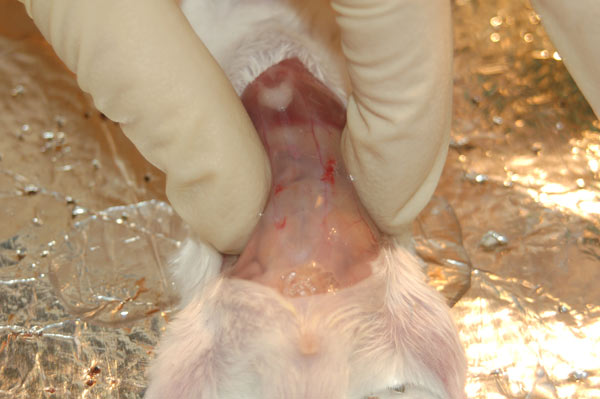
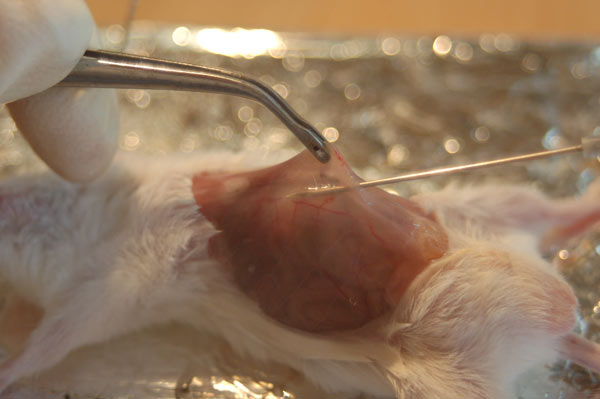
Собранную взвесь клеток центрифугируем 4 мин при 1000 оборотов/мин
Удаляем надосадочную жидкость пипеткой, доводим объем до 1 мл физ раствором, затем пипетируем (взбалтываем пипеткой) взвесь клеток. Эта взвесь клеток представляет собой ПЕРВИЧНУЮ КУЛЬТУРУ КЛЕТОК.
Помечаем эппендорфы: контроль 1/1 как «К1/1», контроль 2/1 как «К2/1», пероксид водорода 1/1 как «ПВ1/1» и пероксид водорода 2/1 как «ПВ2/1». Собираем камеру Горяева.
Отливаем пипеткой 100 мкл взвеси клеток в эппендорф с пометкой контроль 1/1, добавляем 100 мкл раствора бензоата натрия и ждем 2 минуты. После этого добавляем 200 мкл р-ра трепановой сини и пипетируем. Затем сразу помещаем каплю суспензии клеток в один из карманов камеры Горяева (См. ПРОТОКОЛ ниже). Наблюдаем при малом увеличении (объектив х10, окуляр х10 или х15) микроскопа количество окрасившихся клеток. Результаты записываем в тетрадь.
Отливаем пипеткой 67 мкл взвеси клеток в эппендорф с пометкой контроль 2/1, добавляем 134 мкл раствора бензоата натрия и ждем 2 минуты. После этого добавляем 200 мкл р-ра трепановой сини и пипетируем. Затем сразу помещаем каплю суспензии клеток в один из карманов камеры Горяева. Наблюдаем при малом увеличении (объектив х10, окуляр х10 или х15) микроскопа количество окрасившихся клеток. Результаты записываем в тетради.
В третий эппендорф с пометкой пероксид водорода 1/1 наливаем 100 мкл взвеси клеток+ 100мкл р-ра пероксида водорода, ждем 2 минуты. Таким образом, на клетки действует 1.5% пероксида водорода. После этого добавляем 200 мкл р-ра трепановой сини и пипетируем. Затем сразу помещаем каплю суспензии клеток в один из карманов камеры Горяева. Наблюдаем при малом увеличении (объектив х10, окуляр х10 или х15) микроскопа количество окрасившихся клеток и отмечает соотношение прокрашенных и непрокрашенных клеток. Результаты записываем в тетрадь.
В четвертый эппендорф с пометкой пероксид водорода 2/1наливаем 67 мкл взвеси клеток+ 134 мкл р-ра перекиси водорода, ждем 2 минуты. Таким образом, на клетки действует 2% пероксида водорода. После этого добавляем 200 мкл р-ра трепановой сини и пипетируем. Затем сразу помещаем каплю суспензии клеток в один из карманов камеры Горяева. Наблюдаем при малом увеличении (объектив х10, окуляр х10 или х15) микроскопа количество окрасившихся клеток и отмечает соотношение прокрашенных и непрокрашенных клеток. Результаты записываем в тетрадь.
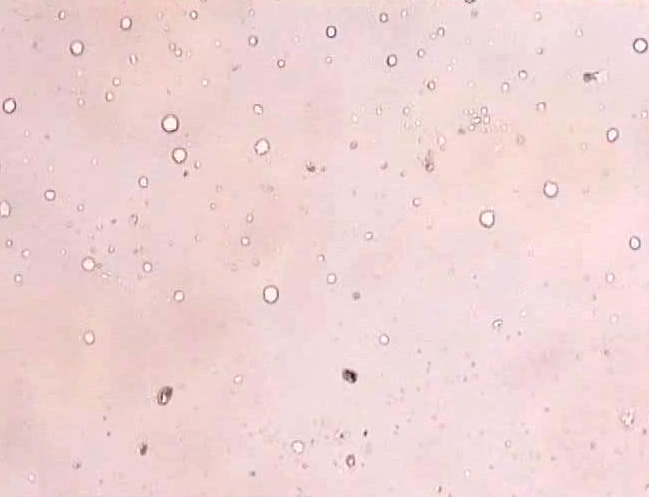
Нормальные макрофаги (указано стрелкой) Поврежденные макрофаги (указано стрелкой)
ПРОТОКОЛ «Микроскопический подсчет живых клеток»
В образец клеток добавляется трипановый синий, краситель, который не проникает в живые клетки, но окрашивает мертвые клетки в темно-синий цвет. Затем клетки помещаются на специальное стекло с нанесенной решеткой, которое называется гемоцитометр (или камера Горяева), и количество клеток подсчитывается вручную под микроскопом.
