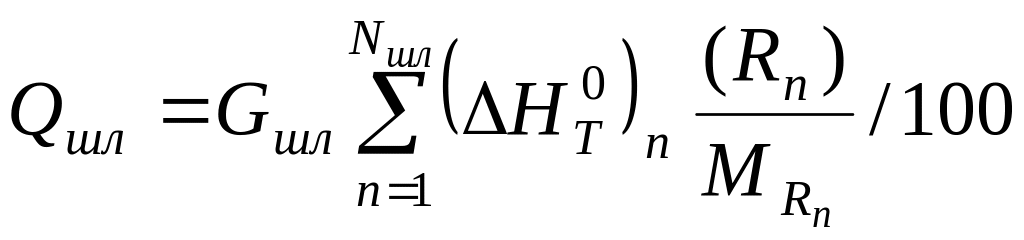- •Расчет теплового баланса металлургического процесса
- •Расчет теплового баланса металлургического процесса
- •1. Общие принципы расчета теплового баланса металлургического процесса
- •2. Пример расчета теплового баланса
- •3. Этапы выполнения лабораторной работы
- •Расчет Теплового баланса металлургического процесса
- •654007, Г. Новокузнецк, ул. Крова, 42.
Факультет информационных
технологий
Кафедра информационных
технологий в металлургии
Расчет теплового баланса металлургического процесса
Новокузнецк
2009
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
«Сибирский государственный индустриальный университет»
Кафедра информационных технологий в металлургии
Расчет теплового баланса металлургического процесса
Методические указания к выполнению лабораторных работ
по дисциплинам «Математические модели и автоматизированные технологии», «Физико-химические модели в металлургии». Специальность: 230201 - Информационные системы и технологии
Новокузнецк
2009
УДК 669.162.275.012.34(07)
Р 248
Рецензент:
Доктор технических наук, профессор СибГИУ
К.М. Шакиров
М 341 Расчет теплового баланса металлургического процесса: Метод. указ./ Сост.: И.А. Рыбенко, С.П. Мочалов: СибГИУ.- Новокузнецк, 2009.- 28с.
Изложены принципы расчета теплового баланса металлургического процесса. Рассмотрен пример расчета, приведены варианты заданий.
Предназначено для студентов специальности: 230201 – Информационные системы и технологии.
1. Общие принципы расчета теплового баланса металлургического процесса
При выводе уравнений теплового баланса принято, что основными определяющими процессами для теплового состояния системы являются: физическое тепло входных и выходных потоков, химические реакции с соответствующими тепловыми эффектами и теплообмен с окружающей средой. Уравнения теплового баланса базируются на законе сохранения энергии Qприх=Qрасх.
С учетом теплосодержания входных - выходных потоков, общего тепла химических реакций, протекающих в системе, тепла от внешних источников, а также потерь в окружающую среду уравнение теплового баланса имеет вид:
![]() (1)
(1)
где
![]()
![]() -энтальпия
единицы массы k-го
входного и l-го
выходного потоков относительно
температуры 298К,
кДж/кг;
К, L
- общее количество входных и выходных
потоков; Gk,
Gl
– массы
входных и выходных потоков соответственно,
кг; Qист,
- приход
тепла в систему от внешних источников,
кДж; Qпот
- тепловые
потери в окружающую среду, кДж;
-энтальпия
единицы массы k-го
входного и l-го
выходного потоков относительно
температуры 298К,
кДж/кг;
К, L
- общее количество входных и выходных
потоков; Gk,
Gl
– массы
входных и выходных потоков соответственно,
кг; Qист,
- приход
тепла в систему от внешних источников,
кДж; Qпот
- тепловые
потери в окружающую среду, кДж;
![]() ,
,
![]() -
тепловой эффект экзотермических и
эндотермических химических реакций,
кДж.
-
тепловой эффект экзотермических и
эндотермических химических реакций,
кДж.
Основными статьями приходной части теплового баланса являются тепло жидкого чугуна, тепло экзотермических реакций окисления компонентов шихты газообразным кислородом, тепло реакций шлакообразования и тепло внешних источников тепла.
К расходной части теплового баланса относятся затраты тепла на нагрев металла, шлака, газа, на разложение карбонатов, оксидов железа, испарение влаги и тепловые потери в окружающую среду.
Энтальпия единицы массы жидкого чугуна относительно T= 298 K определяется следующим образом:
 , (2)
, (2)
где
![]() - изменение энтальпии 1 моля m-го
вещества жидкого чугуна при нагреве от
298 К до
Tk,
кДж/моль; Rmчуг-
концентрация вещества Rm
в чугуне,
%; MRm
- молярная масса вещества Rm,
кг/моль; Nчуг
– количество
веществ в чугуне.
- изменение энтальпии 1 моля m-го
вещества жидкого чугуна при нагреве от
298 К до
Tk,
кДж/моль; Rmчуг-
концентрация вещества Rm
в чугуне,
%; MRm
- молярная масса вещества Rm,
кг/моль; Nчуг
– количество
веществ в чугуне.
Тепловой эффект экзотермических реакций определяется суммой тепловых эффектов реакций окисления железа, углерода, примесей и горения метана.
![]() , (3)
, (3)
где Wэкз – число экзотермических реакций; Hw - тепловой эффект w-ой химической реакции, кДж.
Тепловой эффект w-ой химической реакции рассчитываем по формуле:
![]() , (4)
, (4)
где
![]() - стандартный тепловой эффект w-ой
химической реакции;
- стандартный тепловой эффект w-ой
химической реакции;
![]() -
количество молей вещества R,
прореагировавшего в w-ой
реакции.
-
количество молей вещества R,
прореагировавшего в w-ой
реакции.
Число молей участвовавшего в реакции вещества Rw определяется разностью его содержания во входных - выходных потоках:
![]() . (5)
. (5)
Таким образом, тепловой эффект экзотермических реакций равен:
![]() (6)
(6)
К экзотермическим реакциям относятся также реакции шлакообразования, тепловой эффект реакций шлакообразования рассчитывается по формуле:
![]() , (7)
, (7)
где
![]() - количество соответствующих оксидов
в шлаке, кг.
- количество соответствующих оксидов
в шлаке, кг.
Энтальпию единицы массы металла, шлака и газа рассчитываем аналогично энтальпии единицы массы чугуна:

 (8)
(8)
 ,
,
где ![]() - изменение энтальпии 1 моля n-го
вещества при нагреве от 298
К до Tk,
кДж/моль; [Rn],
(Rn),
{Rn},
- концентрация вещества Rn
в металле,
шлаке и газе соответственно, %; MRn
- молярная масса вещества Rn,
кг/моль; Nм,
Nшл,
Nг
– количество веществ в металле, шлаке
и газе.
- изменение энтальпии 1 моля n-го
вещества при нагреве от 298
К до Tk,
кДж/моль; [Rn],
(Rn),
{Rn},
- концентрация вещества Rn
в металле,
шлаке и газе соответственно, %; MRn
- молярная масса вещества Rn,
кг/моль; Nм,
Nшл,
Nг
– количество веществ в металле, шлаке
и газе.
К эндотермическим реакциям относятся реакции разложения оксидов железа, разложения карбонатов и испарения влаги, суммарный тепловой эффект эндотермических реакций рассчитаем по формуле:
![]() (9)
(9)
С учетом вышеизложенного уравнение теплового баланса имеет вид:
 (10)
(10)
В таблице 1 представлен расчет теплового баланса по статьям.
Таблица 1 – Расчет теплового баланса по статьям
Статья |
Тепловой эффект |
Приходная часть |
|
Физическое тепло чугуна |
|
Тепло экзотермических реакций |
|
Тепло шлакообразования |
|
Тепло внешних ист-ков |
|
Расходная часть |
|
Тепло металла |
|
Тепло шлака |
|
Тепло газа |
|
Тепло эндотермических реакций |
|
Тепловые потери |
Qпот |