- •1 Термодинамический расчет
- •1.1 Расчет тепловых эффектов химических реакций
- •1.1.1 Расчет тепловых эффектов при стандартных условиях
- •1.1.2 Зависимость теплового эффекта химической реакции от температуры. Уравнение Кирхгофа
- •1.2 Расчет изменения изобарно-изотермического потенциала
- •1.3 Расчет константы равновесия
- •1.3.1 Расчет константы равновесия для идеальных газов
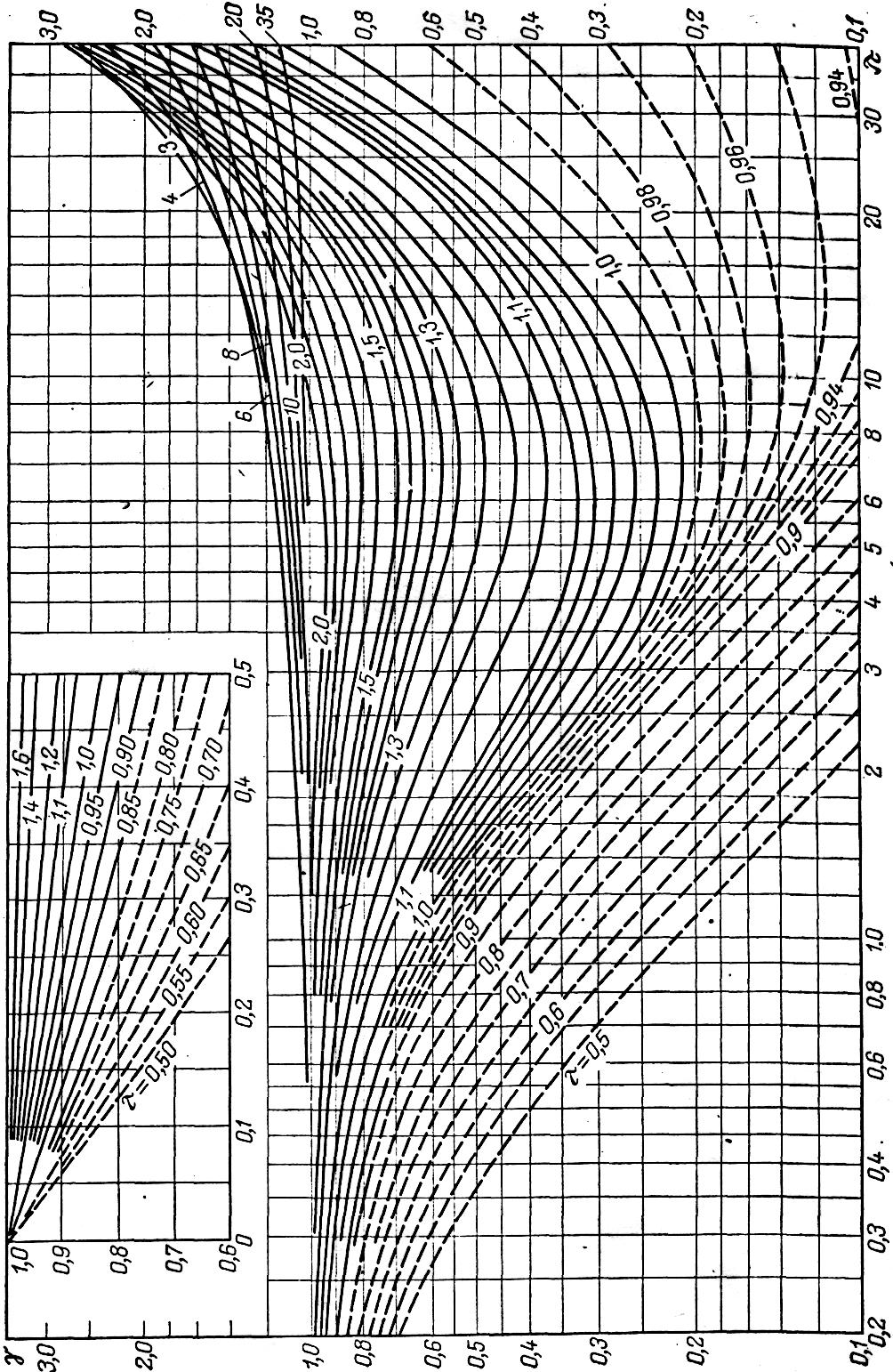
- •1.3.2 Расчет константы равновесия для реальных газов
- •1.4 Расчет равновесного выхода
- •1.5 Последовательность проведения термодинамического расчета химических реакций
- •2 Расчетные методы определения термодинамических свойств
- •3 Пример расчета термодинамических свойств
- •Рекомендации к ведению реакции
- •4 Задания для термодинамического расчета
- •Список литературы
- •Содержание
Список литературы
1. Краткий справочник физико – химических величин / Под ред. А.А.. Равделя и др. – Л.: Химия, 1983. – 232 с.
2. Карапетьянц М.Х. Химическая термодинамика. - М.:Химия, 1975, - 584 с.
3. Физическая химия: В 2-х т. / Под ред. К.С. Краснова. – М.: Высшая школа, 2001.
4. Курс физической химии: В 2-х т. / Под ред. Я. И. Герасимова. – М.: ГХИ, 1963.
5. Киреев В.А. Курс физической химии. - М.: Химия, 1975, - 576с.
6. Белоклокова Т.М., Евдокимова Н.Г., Рахимов М.Н. Расчет критических свойств чистых компонентов. Методические указания к инженерным расчетам физико-химических свойств для специальности 25.04. – Уфа, УНИ. 1995, - 16с.
7. Столяров Е.А., Орлова Н.Г. Расчет физико-химических свойств жидкостей. Справочник . - Л.: Химия, 1976, - 112с.
8. Рид Р., Праусниц Дж., Шервуд Т. Свойства газов и жидкостей. Справочное пособие / Пер. с англ., под ред. Б.И. Соколова – 3-е изд., перераб. и доп. - Л.: Химия, 1982, - 592 с.
Приложение А
Таблица А 1 – Термодинамические величины
Вещество |
∆Нообр, кДж/моль
|
Sо298, Дж/(моль∙К) |
Ср, Дж/(моль∙К) |
Коэффициенты уравнения СР=f(Т) |
Ткр, К |
Ркр, МПа |
||||
а |
b,10 -3 |
с,10- 6 |
с',10 5 |
|||||||
Н2(г) |
0,00 |
130,52 |
28,83 |
27,28 |
3,26 |
- |
0,50 |
33,2 |
1,32 |
|
О2(г) |
0,00 |
205,04 |
29,37 |
31,46 |
3,39 |
- |
-3,77 |
154,6 |
5,04 |
|
N2(г) |
0,00 |
191,50 |
29,12 |
27,88 |
4,27 |
- |
- |
126,2 |
3,39 |
|
Cl2(г) |
0,00 |
222,98 |
33,93 |
37,03 |
0,67 |
- |
-2,85 |
417,2 |
7,71 |
|
Н2О(г) |
-241,81 |
188,72 |
33,61 |
30,00 |
10,71 |
- |
0,33 |
647,1 |
22,06 |
|
СО(г) |
-110,53 |
197,55 |
29,14 |
28,41 |
4,10 |
- |
-0,46 |
132,9 |
3,50 |
|
СО2(г) |
-393,51 |
213,66 |
37,11 |
44,14 |
9,04 |
- |
-8,54 |
304,2 |
7,38 |
|
NO(г) |
91,26 |
210,64 |
29,86 |
29,58 |
3,85 |
- |
-0,59 |
180,2 |
6,48 |
|
NO2(г) |
34,19 |
240,06 |
36,66 |
41,16 |
11,33 |
- |
-7,02 |
431,4 |
10,13 |
|
N2O4(г) |
11,11 |
304,35 |
79,16 |
83,89 |
39,75 |
- |
-14,90 |
431,4 |
10,13 |
|
NH3(г) |
-45,94 |
192,66 |
35,16 |
29,80 |
25,48 |
- |
-1,67 |
405,4 |
11,33 |
|
HCl(г) |
-92,31 |
186,79 |
29,14 |
26,53 |
4,60 |
- |
1,09 |
324,7 |
8,26 |
|
СН4(г) |
-74,85 |
186,27 |
35,71 |
14,32 |
74,66 |
-17,43 |
- |
191,6 |
4,66 |
|
С2Н2(г) |
226,75 |
200,82 |
43,93 |
26,44 |
66,65 |
-26,48 |
- |
308,3 |
6,14 |
|
С2Н4(г) |
52,30 |
219,45 |
43,56 |
11,32 |
122,01 |
-37,90 |
- |
282,4 |
5,04 |
|
С2Н6(г) |
-84,67 |
229,49 |
52,64 |
5,75 |
175,11 |
-57,85 |
- |
305,3 |
4,87 |
|
С3Н6(г) |
20,41 |
266,94 |
63,89 |
12,44 |
188,38 |
-47,60 |
- |
365,0 |
4,62 |
|
С3Н8(г) |
-103,85 |
269,91 |
73,51 |
1,72 |
270,75 |
-94,48 |
- |
370,0 |
4,26 |
|
С4Н6(г) 1,3-бутадиен |
110,16 |
278,74 |
79,54 |
8,08 |
273,22 |
-111,75 |
- |
425,2 |
4,33 |
|
С4Н8(г) 1-бутен |
-0,13 |
305,60 |
85,65 |
21,47 |
258,40 |
-80,84 |
- |
419,6 |
4,02 |
|
С4Н10(г) бутан |
-126,15 |
310,12 |
97,45 |
18,23 |
303,56 |
-92,65 |
- |
425,2 |
3,80 |
|
С4Н10(г) изобутан |
-134,52 |
294,64 |
96,82 |
9,61 |
344,79 |
-128,83 |
- |
408,1 |
3,65 |
|
С5Н12(г) пентан |
-146,44 |
348,95 |
120,21 |
6,90 |
425,93 |
-154,39 |
- |
469,8 |
3,37 |
|
С5Н12(г) изопентан |
-154,47 |
343,59 |
118,78 |
2,05 |
439,32 |
-160,54 |
- |
461,0 |
3,42 |
|
С6Н6(г) |
82,93 |
269,20 |
81,67 |
-21,09 |
400,12 |
-169,87 |
|
562,7 |
4,92 |
|
С6Н12(г) |
-123,14 |
298,24 |
106,27 |
-51,70 |
598,77 |
-230,00 |
|
554,2 |
4,11 |
|
Продолжение таблицы А 1 |
||||||||||
Вещество |
∆Нообр, кДж/моль
|
Sо298, Дж/(моль∙К) |
СР, Дж/(моль∙К) |
Коэффициенты уравнения СР=f(Т)
|
Ткр, К |
Ркр, МПа |
||||
а |
b, 10 -3 |
с, 10- 6 |
с', 10 5 |
|||||||
С6Н14(г) гексан |
-167,19 |
388,40 |
143,09 |
8,66 |
505,85 |
-184,43 |
- |
507,9 |
3,03 |
|
С7Н16(г) гептан |
-187,78 |
427,90 |
165,98 |
10,00 |
587,14 |
-215,56 |
- |
540,2 |
2,74 |
|
С8Н10(г) о-ксилол |
19,00 |
352,75 |
133,26 |
0,04 |
504,59 |
-193,55 |
- |
632,2 |
3,65 |
|
С8Н10(г) м-ксилол |
17,24 |
357,69 |
127,57 |
-11,30 |
526,64 |
-204,76 |
- |
619,2 |
3,55 |
|
С8Н10(г) п-ксилол |
17,95 |
352,42 |
126,86 |
-10,67 |
521,03 |
-200,66 |
- |
618,2 |
3,44 |
|
С8Н18(г) октан |
-208,45 |
466,73 |
188,87 |
11,84 |
666,51 |
-244,93 |
- |
569,9 |
2,49 |
|
СН3ОН(г) |
-201,00 |
239,76 |
44,13 |
15,28 |
105,20 |
-31,04 |
- |
512,6 |
8,10 |
|
СН3СОН(г) |
-166,00 |
264,20 |
54,64 |
13,00 |
153,50 |
-53,70 |
- |
461,2 |
6,28 |
|
С2Н4О(г) окись этилена |
-52,63 |
242,42 |
48,50 |
-2,02 |
190,60 |
-73,60 |
- |
468,2 |
7,19 |
|
СН3СООН(г) |
-437,84 |
282,50 |
66,50 |
14,82 |
196,70 |
-77,70 |
- |
594,8 |
5,79 |
|
С2Н5ОН(г) |
-234,80 |
281,38 |
65,75 |
10,99 |
204,70 |
-74,20 |
- |
516,3 |
6,38 |
|
СН3СОСН3(г) |
-217,57 |
294,93 |
74,90 |
22,47 |
201,80 |
-63,50 |
- |
508,7 |
4,72 |
|
CCl4(г) |
-100,42 |
310,12 |
83,76 |
59,36 |
97,00 |
-49,57 |
- |
556,6 |
4,62 |
|
СН3Сl(г) |
-86,31 |
234,47 |
40,75 |
15,57 |
92,74 |
-28,31 |
- |
416,3 |
6,68 |
|
С2Н5Сl(г) |
-111,72 |
275,85 |
62,72 |
11,63 |
193,00 |
-72,92 |
- |
460,4 |
5,27 |
|
С6Н5Сl(г) |
51,84 |
313,46 |
98,03 |
-3,09 |
388,92 |
-166,25 |
- |
632,4 |
4,52 |
|
СН5N(г) метиламин |
-23,01 |
242,59 |
50,08 |
14,70 |
132,60 |
-41,08 |
- |
430,1 |
7,46 |
|
С2Н7N(г) диметиламин |
-18,83 |
272,96 |
69,04 |
4,54 |
242,10 |
-86,84 |
- |
437,7 |
5,31 |
|
С3Н9N(г) триметиламин |
-23,85 |
288,78 |
91,76 |
1,60 |
341,00 |
-129,30 |
- |
433,3 |
4,07 |
|
Таблица А 2 - Величина Mn для вычисления ∆G
Т, К |
М0 |
М1 , 103 |
М2 , 106 |
М-2 ,10-5 |
300 |
0,0000 |
0,0000 |
0,0000 |
0,0000 |
400 |
0,0392 |
0,0130 |
0,0043 |
0,0364 |
500 |
0,1133 |
0,0407 |
0,0140 |
0,0916 |
600 |
0,1962 |
0,0759 |
0,0303 |
0,1423 |
700 |
0,2794 |
0,1153 |
0,0498 |
0,1853 |
800 |
0,3597 |
0,1574 |
0,0733 |
0,2213 |
900 |
0,4361 |
0,2012 |
0,1004 |
0,2521 |
1000 |
0,5088 |
0,2463 |
0,1310 |
0,2783 |
1100 |
0,5765 |
0,2922 |
0,1652 |
0,2988 |
1200 |
0,6410 |
0,3389 |
0,2029 |
0,3176 |
Таблица А 3 -
Составляющие связей для расчета
![]() и
и
![]()
СВЯЗЬ |
, Дж/(моль К)
|
кДж/моль |
СВЯЗЬ |
, Дж/(моль К)
|
кДж/моль |
|
54,051 |
-16,048 |
|
100,560 |
-113,130 |
|
-68,716 |
11,439 |
|
136,175 |
38,129 |
|
57,822 |
13,408 |
|
38,129 |
90,085 |
|
-59,917 |
28,073 |
|
112,292 |
-58,241 |
Ø
|
49,023 |
13,618 |
|
-2,514 |
-60,336 |
Ø
|
-72,906 |
30,378 |
|
41,062 |
-211,595 |
|
70,811 |
- |
|
132,404 |
- |
|
77,934 |
- |
|
147,488 |
-113,130 |
|
82,543 |
-31,006 |
|
-53,632 |
38,967 |
|
88,828 |
-2,933 |
|
74,163 |
-10,894 |
|
94,904 |
9,218 |
|
-6,285 |
28,073 |
|
100,979 |
40,643 |
|
113,130 |
3,352 |
|
103,284 |
59,079 |
|
48,604 |
- |
|
109,359 |
90,923 |
|
180,589 |
-12,570 |
|
-16,79 |
-50,28 |
|
148,745 |
37,710 |

1
 )
)
![]() четырехвалентная группа С=С
.
четырехвалентная группа С=С
.
2) Ø- шестивалентная ароматическое ядро.
3) Н-СО- связь между водородом и углеродом карбонильной группы.
Таблица А 4 - Групповые составляющие для расчета теплоемкости по методу Джонсона - Хуанга.
Группа |
а |
в, 10-2 |
с, 10-4 |
d,10-6 |
-СН3 |
1,789 |
9,147 |
-0,3616 |
0,00465 |
-СН2- |
-0,779 |
9,398 |
-0,5291 |
0,01148 |
=СН2 |
2,774 |
7,416 |
-0,3662 |
0,00670 |
=СН- |
-1,001 |
6,968 |
-0,4425 |
0,01089 |
-С6Н5 |
-31,743 |
46,119 |
-3,0545 |
0,07546 |
|
8,673 |
5,866 |
-0,4848 |
0,01475 |
-С |
-22,006 |
16,287 |
-1,8436 |
0,06373 |
- СН
|
-8,137 |
11,866 |
-0,9557 |
0,02770 |
-СН2- (пятичленное кольцо) |
-8,954 |
10,362 |
-0,5007 |
0,00830 |
-СН2- (шестичленное кольцо) |
-9,712 |
10,353 |
-0,5422 |
0,01077 |
- С-
|
-19,504 |
15,428 |
-1,4879 |
0,04115 |
-С=
|
-0,224 |
5,623 |
-0,4270 |
0,01144 |
Приложение Б