
- •Методы восстановления в химической технологии бав
- •Химические методы восстановления
- •1. Восстановление натрием
- •1.3. Амальгама натрия
- •2. Восстановление оловом и хлоридом олова (II)
- •3. Восстановление цинком
- •3.2.Цинк в щелочной среде восстанавливает:
- •4. Восстановление железом
- •5. Восстановление гидридами металлов
- •2. Восстановление сульфидами щелочных металлов
- •Каталитическое восстановление водородом
- •Электролитическое восстановление
Методы восстановления в химической технологии бав
Восстановление и окисление являются неразрывно связанными процессами. Если одно из участвующих в реакции веществ восстанавливается, то другое окисляется. Поэтому отнесение одних реакций к окислению, а других – к восстановлению связано с тем, какое вещество является в данном случае целевым продуктом.
Восстановлением называют процесс, в результате которого атом или группа атомов приобретают электроны (их электронная плотность увеличивается). При этом изменяется и состав молекулы:

Для определения величины электронного облака у атома или группы атомов пользуются понятием «степень окисления».
Методы восстановления и окисления можно разделить на четыре группы: химические, каталитические, электролитические и биохимические (микробиологические). Многие из них применяются в фармацевтической промышленности
Химические методы восстановления
- делят на группы по типу восстановителя.
1. Восстановление натрием
1.1. Натрий в спирте (Буво - Блан) используется для восстановления сложных эфиров карбоновых кислот до соответствующих спиртов (но не карбоксильных групп !).
Уравнение реакции:
![]()
Механизм восстановления:

![]()
Выход целевых продуктов, как правило, не превышает 80%. Потери обусловлены реакцией между натрием и спиртом.

Выделяющийся водород неактивен, а образующиеся алкоголяты вызывают конденсацию и переэтерификацию и образование высококипящих побочных продуктов.
Методика восстановления простая, но опасная.
К кипящей смеси сложного эфира и пятикратного количества абсолютного спирта порциями добавляют кусочки металлического натрия, взятого в небольшом избытке. После загрузки всего натрия и необходимой выдержки, реакционную массу выливают в воду для разложения образовавшихся алкоголятов. Спирт отгоняют, а продукты реакции извлекают экстракцией.
Отвод тепла осуществляют с помощью эффективного обратного холодильника. Это сложная техническая проблема, т.к. тепловой эффект реакции очень высок (520 кДж/моль).
Для снижения опасности процесса, повышают температуру реакции, используя высококипящие спирты, либо изменяют порядок загрузки реагентов: спиртовой раствор эфира прибавляют к натрию. Так, восстановление диэтилового эфира себациновой кислоты проводят в 1-бутаноле.
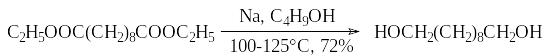
1.2. Натрий в жидком аммиаке - применяется для восстановления:
а) сложных эфиров до спиртов (лучше, чем по методу Буво-Блана)
![]()
б) алкинов до олефинов (при этом тройная связь на конце цепи не восстанавливается)
![]()
![]()
в) органических галогенидов, которое идет в двух направлениях:
![]()
Механизм аналогичен механизму восстановления по Буво-Блану
Для ведения процесса необходима специальная аппаратура, т.к. температура кипения аммиака очень низка (-33,5°С). При более высокой температуре реакцию проводят в автоклаве.
1.3. Амальгама натрия
- раствор натрия в ртути, при этом образуются меркуриды NaHgx. В зависимости от концентрации натрия (ж.<1,25%>тв.) амальгама при комнатной температуре жидкая или твердая.
Процесс растворения натрия в ртути ведут под слоем толуола и в атмосфере азота, чтобы предохранить теплую амальгаму от воздействия кислорода воздуха при 40-50°С, получая таким образом 2-3%-ую амальгаму.
Амальгамой натрия восстанавливают:
а) сопряженные двойные связи (но не изолированные)
![]()
б) отдельные представители аренов, например, фталевые кислоты, ароматические полициклические углеводороды (до ди- или тетрагидропроизводных).

в) карбонильную группу в альдегидах и кетонах до соответствующих спиртов (очень легко!).
![]()
г) Нитро- и другие азотсодержащие группы (очень легко), но практического значения этот метод не получил вследствие наличия более доступных восстановителей.
Механизм восстановления амальгамой натрия такой же, как и в реакции Буво-Блана.
Методика восстановления: субстрат растворяют, эмульгируют или суспендируют в спирте или воде и постепенно добавляют избыток амальгамы (с водой она реагирует медленно). После полного разложения амальгамы, выделившую ртуть отделяют декантацией и промывают водой или спиртом.
Величины рН по ходу реакции повышается и замедляет реакцию. Чтобы избежать этого, необходимо непрерывно контролировать и регулировать пропусканием СО2 значения рН.
