
Порушення білкового обміну
Білкам належить найважливіша роль у життєдіяльності організму. Вони становлять основу структурних елементів клітини, виконують функції ферментів і гормонів, транспортують біологічно активні речовини, створюють осмотичний тиск плазми та інших рідин, є потенційним енергетичним резервом. Значних запасів білків в організмі немає, тому вони повинні постійно синтезуватися з амінокислот, що надходять з їжею. Добова потреба в білках — близько 120 г.
У патологічних умовах білковий обмін може порушуватися на всіх етапах — від процесів травлення до виведення азотистих шлаків. Якщо шлунковий сік містить невелику кількість соляної кислоти чи ферменту пепсину, білки не розпадаються на поліпептиди. У дванадцятипалій кишці цей негідролізований білок не піддається подальшому розщепленню трипсином і пептидазами підшлункової залози. Вільних амінокислот, спроможних всмоктатися у кров, утворюється мало. Те ж саме стається, якщо сік підшлункової залози взагалі не надходить у кишечник (перетискування чи закриття вивідної протоки) або при ентеритах, коли залози кишечника не виділяють достатню кількість ентерокінази — активатора трипсиногену. Травленню і всмоктуванню білків перешкоджає посилена перистальтика кишечника. У результаті цих порушень виникає аліментарна білкова недостатність.
Білки, які не гідролізувалися і не всмокталися в тонкій кишці, переходять у товсту, де піддаються гниттю і бактеріальному розщепленню. Це супроводжується утворенням великої кількості амінів (гістаміну, тираміну, кадаверину, путресцину) і ароматичних сполук (фенолу, індолу, скатолу, крезолу), здатних викликати кишкову аутоінтоксикацію.
При багатьох патологічних станах змінюється вміст білків у крові (норма — 60-80 г/л). Збільшення їх кількості (гіперпротеіїнемія) виникає, як правило, внаслідок посиленого синтезу ¥глобулінів (антитіл) при запаленнях, інфекційних хворобах. Відносне збільшення вмісту всіх білкових фракцій (альбумінів, глобулінів, фібриногену) може зумовлюватись зневодненням організму і згущенням крові (діарея в дітей, блювота, обширні опіки). Зменшення кількості білків у крові називають гіпопротеїнемією. Вона спостерігається у випадках недостатнього синтезу білків (голодування, ентерит, цироз печінки), виходу їх за межі судинного русла (крововтрата, ексудація) або виділення із сечею . внаслідок збільшення фільтрації чи зменшення реабсорбції в нирках (протеїнурія). Гіпопротеїнемія зумовлена, головним чином, і зменшенням альбумінової фракції. Порушення співвідношення між і білковими фракціями крові називають диспротеїнемією.
Іноді синтезуються білки, взагалі не властиві здоровому організмові, вони відомі під назвою парапротеїнів. До них належать макроглобуліни з молекулярною масою 1000-1600 кД, які з'являються у хворих з мієломною хворобою, а також кріоглобуліни, що випадають в осад, коли знижується температура навколишнього середовища.
Загальне уявлення про білковий обмін можна скласти на основі дослідження азотистого балансу. Порівнюють кількість азоту, що надійшов в організм, з кількістю азоту, виведеного з організму. В нормі ці дві величини рівні. За добу здорова людина споживає і виводить 12-14 г азоту. Позитивний азотистий баланс зустрічається в дітей у процесі росту, при вагітності, відгодовуванні, лікуванні чоловічими статевими гормонами. Негативний азотистий баланс виникає під час голодування, проносу, при масивних опіках, розпаді пухлин, нирковій недостатності, тиреотоксикозі, отруєннях фосфором, миш'яком, сулемою. Інфекційна гарячка супроводжується так званим токсигенним розпадом білка, який відбувається під впливом продуктів життєдіяльності мікроорганізмів.
Кінцевий етап обміну білків завершується утворенням аміаку і сечовини. Спочатку білкові молекули розпадаються до амінокислот. Останні дезамінуються, і аміак іде у мітохондорії гепатоцитів на синтез сечовини, яка від нього у 18 разів менш токсична і виводиться нирками. Тому нагромадження аміаку в нормі не буває. Отже, сечовиноутворення — важливий фізіологічний механізм захисту клітин від токсичного впливу високих концентрацій аміаку.
В умовах патології в крові може скупчуватися багато азотовмісних продуктів метаболізму, і загальна концентрація азоту буде зростати. Це явище називають гіперазотемією. Ступінь гіперазотемії залежить від рівня залишкового азоту крові, який визначається після осадження білків. Він складається з азоту, що входить до складу сечовини (50 %), амінокислот (25 %), креатину (5 %), креатиніну (2,5 %), сечової кислоти (4 %) та інших сполук. У здорових людей небілковий азот становить 15-25 ммоль/л і мало залежить від кількості спожитих білків. У хворих він може зростати в 5-Ю разів.
Гіперазотемія за походженням буває двох видів: продукційна і ретенційна. Продукційною гіперазотемією супроводжується інтенсивний розпад білкових молекул. Якщо це поєднується з порушенням функцій печінки (гепатит, цироз), то концентрація амінокислот і аміаку в крові зростає на фоні низького вмісту сечовини. Ретенційна гіперазотемія виникає в разі затримки кінцевих продуктів білкового обміну в крові. Виведення їх з організму утруднюється при гломерулонефриті у зв'язку з ослабленням екскреторної функції нирок. Різке зростання залишкового азоту при цій патології відбувається, переважно, за рахунок сечовини. Ще більше затримується азот у термінальній стадії ниркової недостатності (уремії).
З усіх речовин, що затримуються в крові при гіперазотемії, найбільший токсичний вплив чинить аміак. Дуже чутливий до нього головний мозок. Механізм токсичної дії аміаку уявляють так. У мозку аміак зв'язується з глютаміновою кислотою, яка перетворюється на глютамін. Кількість глютамінової кислоти зменшується, а заодно зменшується і кількість ос-кетоглютаро-вої кислоти, яка є її джерелом. Внаслідок цього сповільнюється цикл Кребса і зменшується утворення енергії в нейронах.
Морфологічним проявом порушення обміну білка в клітині є паренхіматозні білкові дистрофії (диспротеїнози). Суть їх полягає в зміні фізико-хімічних і морфологічних властивостей внутрішньоклітинних білків. Вони піддаються або денатурації і коагуляції, тобто ущільненню, або, навпаки, розрідженню, гідратації і коліквації. Зв'язок білків із ліпідами порушується, настає деструкція мембран. Завершуються такі зміни коагуляційним (сухим) або коліквативним (вологим) некрозом. До паренхіматозних білкових дистрофій належать зерниста, гіаліново-крапельна, водянкова та рогова дистрофії.
Зерниста дистрофія не є власне проявом альтерації, вона свідчить про функціональне перенапруження клітин при інтоксикаціях, інфекційних хворобах, гіпоксії. Електронномікроскопічними і гістоферментохімічними дослідженнями доведено, що в основі зернистої дистрофії лежить не накопичення білків у цитоплазмі, а гіперплазія, тобто збільшення числа ультраструктур паренхіматозних органів. їх розміри збільшуються, стають в'ялими і тьмяними на розрізі (тьмяне набубнявіння).
У випадку гіаліново-крапельної дистрофії дрібненькі зерна білка зливаються у великі білкові краплі, які, збільшуючись, заповнюють усе тіло клітини. Субклітинні структури при цьому руйнуються. Завершується гіаліново-крапельна дистрофія коагуляційним некрозом клітини. Зустрічається найчастіше в нирках і печінці. Функція органів при цьому знижується. Зміни незворотні.
Гідропічна, або водянкова, дистрофія характеризується появою в клітині вакуолей, наповнених цитоплазматичною рідиною, тобто в клітині з'являється надлишок води. Зумовлена водянкова дистрофія затримкою рідини в тканинах (серцеві або ниркові набряки, запалення, травми). Вона буває загальною і місцевою. Зустрічається в шкірі, скелетних м'язах, головному мозку, нирках, печінці, надниркових залозах. Органи і тканини збільшуються, набрякають. Вакуолі внутрішньоклітинної рідини відтискують ядро на периферію, останнє зморщується, ультраструктури руйнуються. На завершення водянкової дистрофії настає коліквативний (вологий) некроз клітини.
Для рогової дистрофії, або патологічного зроговіння, характерне надмірне утворення рогової речовини в епітелії шкіри (гіперкератоз, іхтіоз) або утворення рогової речовини там, де в нормі її не буває (патологічне зроговіння слизових оболонок — лейкоплакія).
Стромально-судинні білкові дистрофії виявляють у стромі органів і в стінках судин. До них належать мукоїдний набряк, фібриноїдний набряк, гіаліноз і амілоїдоз. Як правило, мукоїдний набряк, фібриноїдний набряк і гіаліноз є послідовними стадіями дезорганізації сполучної тканини. ^ основі ньото процесу лежить накопичення продуктів плазми крові в основній речовині внаслідок підвищеної судинно-тканинної проникності (плазморагія), а також деструкція основної речовини і волокнистих структур з утворенням білково-вуглеводних компонентів, які не зустрічаються в нормі.
Мукоїдне набухання — це зворотні зміни сполучної тканини. За рахунок збільшення активності стрептокінази і гіалуронідази настає деполімеризація основної речовини. Внаслідок цього звільнюються глікозаміноглікани, які мають гідрофільні властивості. До них додаються білки плазми крові, переважно глобуліни. Розвиваються гідратація і набряк основної речовини. Набрякають також колагенові волокна. Серед причин мукоїдного набухання найбільше значення мають гіпоксія, інфекційні та алергічні захворювання, ревматоїдні хвороби, атеросклероз, ендокринопатії. Патоморфологічні зміни локалізуються в стінках артерій, клапанах серця, ендо- і перикарді, стромі органів. Якщо усунути причину, то структура сполучної тканини відновлюється. Якщо ж причина продовжує діяти, то мукоїдний набряк переходить у фібриноїдний.
Фібриноїдним набряком позначають глибоку незворотну дезорганізацію сполучної тканини, в основі якої лежить деструкція основної речовини і колагенових волокон з утворенням фібриноїду. Фібриноїд - складна речовина, до складу якої входять продукти розпаду колагенових волокон, основної речовини і білки плазми крові. Обов'язковим компонентом фібриноїду є фібрин, звідси й назва "фібриноїдний набряк"; "фібриноїд". Як наслідок фібриноїдного набряку розвивається фібриноїдний некроз, тобто повна дезорганізація сполучної тканини. Зовнішній вигляд тканин при мукоїдному і фібриноїдному набряках мало змінений. Причини фібриноїдного набряку ті ж самі, що й мукоїд-ного. Він зустрічається, крім того, в артеріолах при гіпертонічній хворобі й у капілярах ниркових клубочків при гломерулонефриті. У цих випадках фібриноїдний набряк має системний характер, але може бути й місцевим (у дні хронічної виразки шлунка, у трофічних виразках). Фібриноїдний набряк закінчується склерозом (утворенням рубця) і гіалінозом.
Паліноз, або гіалінова дистрофія, характеризується утворенням однорідної щільної напівпрозорої маси, подібної до гіалінового хряща. Гіалін — це фібрилярний білок, в утворенні якого беруть участь білки плазми крові, зокрема фібрин, а також продукти тканинного розпаду.
Розрізняють гіаліноз судин і гіаліноз власне сполучної тканини. Гіаліноз судин розвивається, переважно, в артеріолах при гіпертонічній хворобі. Внаслідок підвищеної проникності артеріол стінки їх просочуються білками плазми крові, які разом із продуктами розпаду стінок артеріол ущільнюються, утворюючи гіалін. Такі ж зміни виникають у стінках артерій при цукровому діабеті (діабетична ангіопатія). Гіаліноз власне сполучної тканини розвивається як нас-: лідок фібриноїдного набряку в рубцях, фіброзних злуках, у дні хронічної виразки шлунка. До гіалінозу клапанів серця призводить ревматичне ураження їх (рис. 6). Грубі спотворюючі рубці з гіалінозом, які часто виникають після опіків, особливо напалмових, називають келоїдами. Гіаліноз — незворотний процес, хоча протягом тривалого часу рубці можуть розсмоктуватися.
Амілоїдоз характеризується появою аномального білка, якого в нормі немає. Цей складний фібрилярний білок фарбується, подібно до крохмалю, йодом у синій колір, звідси й назва "амілоїд" - подібний до крохмалю. Механізм утворення амілоїду складний і проходить чотири послідовні стадії: 1) передамілоїдна стадія, суть якої полягає в трансформації мезенхімальних клітин, що синтезують білки, в амілоїдобласти; 2) синтез амілоїдобластами основного компонента амілоїду — фібрилярного білка (фібрил); 3) агрегація фібрил у каркас амілоїду (сітку); 4) з'єднання каркаса з глікопротеїдами плазми і глікозаміногліканами тканини, в результаті чого утворюється складний глікопротеїд — амілоїд. Він локалізується, переважно, в стінках дрібних судин. Частіше уражаються капіляри ниркових клубочків (рис. 7), селезінки, рідше — міокарда, печінки, надниркових залоз, кишечника. Розрізняють такі види амілоїдозу: первинний (ідіопатичний), причина якого невідома; спадковий (сімейний); набутий (вторинний), який виникає при масивному розпаді тканин в організмі; старечий; локальний пухлиноподібний.
Найбільше практичне значення має набутий (вторинний) амілоїдоз, який розвивається як ускладнення захворювань, що супроводжуються розпадом тканини (кавернозний туберкульоз, абсцеси легень, бронхоектатична хвороба, масивні опіки, остеомієліт) з утворенням амілоїдних речовин. Вони виводяться нирками, засмічують стінки капілярів клубочків і накопичуються в нирці. Орган ущільнюється, збільшується, набуває білого кольору, а на розрізі — сального вигляду ("велика сальна нирка"). Такі зміни зумовлюють хронічну ниркову недостатність (уремію). Відкладається амілоїд і в органах по ходу колагенових волокон і в ретикулярній стромі. У селезінці він нагромаджується спочатку навколо артерій у вигляді напівпрозорої маси, подібної до зерен саго ("сагова селезінка"), а потім розповсюджується на всю пульпу органа ("сальна селезінка").
Змішані білкові дистрофії пов'язані з порушенням метаболізму як у паренхімі, так і в стромі органів і тканин. Вони виникають при розладах обміну складних білків — хромопротеїдів, нуклеопротеїдів й ліпопротеїдів.
Хромопротеїдами називають кольорові речовини, які надають тканині певного забарвлення. Вони поділяються на три групи: гемоглобіногенні, альбуміногенні й ліпогенні. До першої групи належать похідні гемоглобіну, міоглобіну, цитохромів і каталази (гемосидерин, гематоїдин, білівердин, білірубін), до другої — меланін (похідне амінокислоти тирозину), до третьої — жиророзчинні пігменти (ліпофусцин, каротин).
Гемоглобіногенні пігменти. Гемоглобін складається з двох частин: білкової (глобін) і простетичної (гем, у структурі якого є чотири пірольних кільця і залізо). Гемоглобін знаходиться в еритроцитах і виконує функцію переносника кисню від легень до тканин. Коли старі еритроцити руйнуються в макрофагах системи мононуклеарних фагоцитів (печінка, селезінка, кістковий мозок, легені), частина вільного гемоглобіну виходить у кров і забарвлює плазму в червоний колір. У випадках масивного розпаду (гемолізу) еритроцитів він виводиться із сечею (гемоглобінурія). При цьому пошкоджуються артеріоли ниркових клубочків і утворюються гемоглобінові циліндри, які закривають просвіт ниркових канальців, перешкоджаючи відтоку сечі. Нирка збільшується, подразнюються навколониркові нервові сплетення, з'являється біль у попереку.
У тканинних макрофагах гемоглобін, який вивільнився внаслідок руйнування еритроцитів, піддається деградації. Від нього відщеплюється глобін, а гем втрачає циклічну структуру і залізо. При фізіологічному розпаді еритроцитів з гему послідовно утворюються гемосидерин, білівердин і білірубін. За патологічних умов, коли посилюється внутрішньосудинний гемоліз еритроцитів (масивні опіки, травми, інтоксикації, гемолітичні анемії, переливання несумісної крові), названих вище пігментів утворюється більше і, крім того, з'являються нові — гематоїдин, гематини і порфирини.
Гемосидерин — залізовмісний пігмент, який при надмірному утворенні відкладається в тканинах. Розрізняють загальний і місцевий гемосидероз. Загальний гемосидероз виникає при посиленому внутрішньосудинному гемолізі еритроцитів. Гемоглобін поза еритроцитами поглинається макрофагами, які містяться в селезінці, лімфатичних вузлах, кістковому мозку, загрудинній залозі (тимусі), печінці. Внутрішньоклітинно гемоглобін перетворюється в гемосидерин і скупчується в цитоплазмі. Такі макрофаги називають сидерофагами. Гемосидерин має коричнево-буре забарвлення, такого ж кольору набувають селезінка, печінка, лімфатичні вузли, кістковий мозок, загрудинна залоза.
Місцевий гемосидероз виникає в місцях крововиливів. Поза судинами еритроцити швидко фагоцитуються макрофагами, де гемоглобін перетворюється в гемосидерин. Якщо сидерофаги руйнуються, пігмент вільно відкладається у тканинах і зберігається дуже довго. Це використовується в судовій медицині для агностики колишньої травми. Гемосидероз легень належить до місцевого, він розвивається при венозному повнокрів'ї. Переповнені венозною кров'ю судини розширюються, а проникність їх збільшується настільки, що еритроцити виходять у позасудинний простір (діапедез). В альвеолярних і стромальних макрофагах гемоглобін перетворюється в гемосидерин . Легені збувають коричневого забарвлення. Сидерофаги в харкотинні ззивають "клітинами серцевих вад".
Білівердин — продукт більш глибокої деградації гему в макрофагах: із нього видаляється залізо, а пірольне кільце розривається ферментом гемоксигеназою.
Білірубін утворюється з білівердину. Він надходить у кров і :ає початок усім іншим жовчним пігментам. Спочатку утвоворюється так званий некон'югований (незв'язаний) білірубін. Він надходить у печінку, проникає в гепатоцити і зв'язується там із глюкуроновою кислотою.
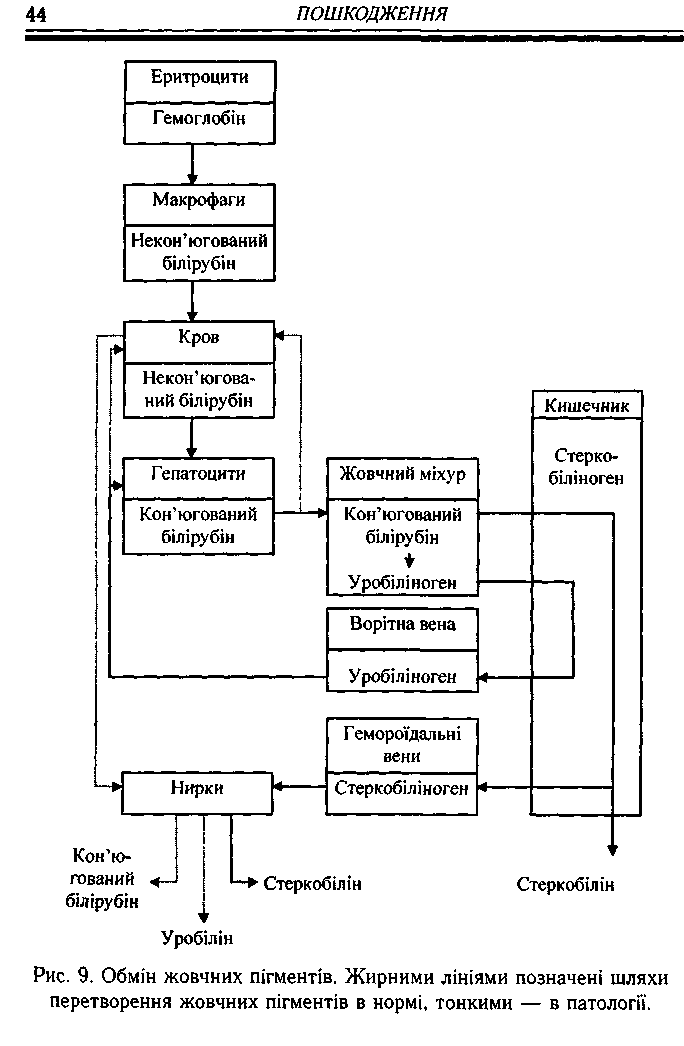
Якщо жовчні пігменти нагромаджуються в організмі, вони забарвлюють шкіру, слизові, склери, серозні оболонки і внутрішні органи в жовтий колір. Цей синдром називають жовтяницею.
Описані нижче гемоглобіногенні пігменти не належать до жовчних.
Гематоїдин — беззалізистий кристалічний пігмент яскраво-рожевого кольору, утворюється в центрі гематоми.
Гематини бувають трьох видів: малярійний пігмент, солянокислий гематин і формаліновий пігмент. Малярійний пігмент утворюється під впливом плазмодіїв малярії, які паразитують в еритроцитах. Він забарвлює печінку, селезінку, лімфатичні вузли, головний мозок у чорно-бурий колір. Солянокислий гематин утворюється І при дії на гемоглобін соляної кислоти. Він з'являється в шлунку під час кровотечі, тому краї ерозії і виразки шлунка темно-коричневого кольору, а блювотні маси мають колір кави. Формаліновий пігмент : утворюється при фіксації тканин у формаліні.
Порфирини не відіграють помітної ролі в життєдіяльності організму. Невелика кількість їх виявляється в крові, тканинах і сечі здорових людей. Вони мають властивість підвищувати чутливість шкіри до світла і в цьому відношенні є антагоністами меланіну. Порушення обміну порфиринів називають порфиріями. Усі вони спадкового походження. При цьому підвищується рівень пігментів у крові (порфиринемія) і сечі (порфиринурія), виникають світлобоязнь, еритема, дерматит.
Із гемоглобіногенними пігментами пов'язане цвітіння синців:
синій колір зумовлений відновленим гемоглобіном, перехід до жовто-червоного — білірубіном, далі до яскраво-рожевого — ге-
матоїдином. Коричнева облямівка синця — гемосидерином.
