
- •1. Гемостаз, общая характеристика. Механизмы гемостаза. Факторы системы гемостаза. Физиологическое значение системы гемостаза.
- •2. По характеру расстройств:
- •Типы кровоточивости
- •2. Механизм коагуляционного гемостаза. Факторы свертывания крови.
- •3. Первичные и вторичные физиологические антикоагулянты.
- •Фибринолиз
- •I фаза. Превращение плазминогена (профибринолизина) в плазмин (фибринолизин).
- •II фаза.
- •Естественные антикоагулянты
- •Скорость свертывания крови замедляется при:
- •4. Патология сосудисто-тромбоцитарного гемостаза при тромбоцитопениях, тромбоцитопатиях, тромбоцитозах: виды, причины, механизмы развития, проявления.
- •1. Рефлекторный спазм поврежденных сосудов.
- •2. Адгезия (приклеивание, прилипание) тромбоцитов к раневой поверхности.
- •3. Накопление и агрегация (скучивание, образование конгломерата) тромбоцитов у места повреждения.
- •1. Тромбоцитопении вследствие патологии тромбоцитопоэза.
- •2. Тромбоцитопении вследствие повышения разрушения тромбоцитов.
- •3. Тромбоцитопении вследствие повышения потребления тромбоцитов.
- •4. Перераспределительные тромбоцитопении.
- •1. Повреждение эндотелия и первичный спазм сосудов.
- •2. Адгезия тромбоцитов к участку деэндотелизации.
- •3.Активация тромбоцитов и вторичный спазм сосудов.
- •4. Агрегация тромбоцитов.
- •5. Образование гемостатической пробки.
- •5. Наследственные и приобретенные формы нарушения коагуляционного гемостаза. Этиология, патогенез, проявления.
- •6. Синдром диссеминированного внутрисосудистого свертывания крови (двс-синдром): этиология, патогенез, принципы классификации, основные клинические проявления, принципы диагностики и терапии.
- •I. По течению:
- •II. По локализации процесса:
- •III. По тяжести процесса:
- •7. Принципы коррекции нарушений гемостаза.
2. Механизм коагуляционного гемостаза. Факторы свертывания крови.
Механизмы коагуляционного гемостаза
Различают три этапа процесса свертывания крови. Первый этап завершается образованием активного протромбиназного комплекса на ФЛМ (фосфо-липидах мембран), в состав которого входят факторы X, V и Са2+. Второй этап характеризуется образованием тромбина — активной формы фактора II. На третьем этапе (конечная фаза свертывания) происходят формирование и стабилизация сгустка фибрина.
Первый этап каскадно-комплексной схемы свертывания крови включает активацию коагуляционного гемостаза по внутреннему и внешнему механизмам.
Внутренний (контактный) механизм характеризуется последовательной активацией факторов XII, XI, IX, VIII, X. В результате повреждения сосудистой стенки на поверхности тромбоцитарного агрегата образуется комплекс из трех белков — фактора XII (фактор Хагемана), плазменного прекалликреина (ППК) и высокомолекулярного кининогена (ВМК). После связывания с ВМК и калликреином (образуется из ППК под влиянием ВМК) фактор XII превращается в активную протеазу — ХIIа, которая взаимодействует с неактивным фактором XI на ФЛМ и активирует его — образуется фактор ХIа. Далее фактор ХIа комплексируется с неактивным фактором IX и Са2+ на ФЛМ, что в условиях вспомогательной активации фактором VIIa сопровождается формированием IХа, последующее взаимодействие которого с активной формой фактора VIII — VIIIa (ее образование происходит под действием тромбина - IIа) и Са2+ на ФЛМ приводит к активации фактора X.
Внутренний механизм первого этапа свертывания протекает намного медленнее, чем внешний. Он определяется:
временем свертывания крови (5–11 мин в норме);
каолиновым временем - временем свертывания рекальцифицированной цитратной плазмы в условиях контактной (каолин) активации факторов XII и XI (77–116 с при использовании нефракционированного каолина и 60-98 с при применении легкой фракции каолина);
активированным парциальным тромбопластиновым временем (АПТВ) временем свертывания рекальцифицированной цитратной плазмы в условиях контактной (каолин) и фосфолипидной (кефалин) активации факторов XII, XI, IX, VIII (в норме соответствует 30–42 с).
Внешний механизм активации гемостаза предполагает наличие в крови внешнего (в обычных условиях не присутствующего в крови) фактора III (тканевого фактора — ТФ, или тканевого тромбопластина), высвобождающегося из эндотелиоцитов и гладкомышечных клеток поврежденных сосудов. Под его влиянием происходит активация фактора VII с образованием VIIa. Реакция стимулируется следовыми количествами плазменных протеиназ — IIа, VIIa, IXa, Xa, циркулирующих в крови. Взаимодействие факторов III и VIIa на ФЛМ в присутствии ионов Са2+ сопровождается активацией фактора X с образованием Ха.
Свертывание крови по внешнему пути, который в пробирке имитируется добавлением к рекальцифицированной плазме тканевого тромбопластина, обозначается как протромбиновый (тромбопластиновый) тест. Нормальное время свертывания плазмы в присутствии тканевого тромбопластина (протромбиновое время - ПВ) колеблется в пределах 12-15 с. На основе ПВ рассчитываются протромбиновое отношение - ПО (отношение ПВ исследуемой плазмы к ПВ нормальной плазмы; в норме 0,7–1,1) и международное нормализованное отношение — MHO (ПОМИЧ, где МИЧ -международный индекс чувствительности тромбопластина; в норме от 1,0 до 1,4).
Таблица 1. Плазменные факторы свертывания крови
Номер, наименование и природа фактора |
Место образования. Содержание в плазме |
Факторы активации и механизм действия |
I Фибриноген (структурный белок) |
Гепатоциты 1,8–4,0 г/л (80–120% активности) |
Под действием тромбина превращается в фибрин (Iа – основное вещество тромба) Участвует в агрегации тромбоцитов Способствует репарации тканей |
II Протромбин (профермент сериновой протеазы тромбина) |
Гепатоциты (в присутствии витамина К) Около 0,1 г/л |
Под действием активной протромбиназы превращается в тромбин (IIа) Активирует фибриноген с образованием фибрина |
III Тканевой тромбопластин или апопротеини III (трансмембранный белок) |
Эндотелиоциты, макрофаги Не содержится (высвобождается при повреждении стенки сосуда, тканей) |
Кофактор фактора VII, запускает внешний путь свёртывания крови |
IV Ионы кальция – Са2+ |
Гранулы тромбоцитов (плотные тельца), всасывается из кишечника 1,1-1,4 ммоль/л |
Участвует в образовании комплексов плазменных факторов и липидов Входит в состав активной протромбиназы Способствует агрегации тромбоцитов Связывает гепарин Принимаетучастие в образовании первичной гемостатической пробки и ретракции тромба Тормозит фибринолиз |
V Проакцелерин или лабильный фактор (церулоплазминоподобный связывающий белок) |
Гепатоциты, мегакариоциты, тромбоциты Около 0,01 г/л (70-150% активности) |
Активируется фактором IIа Входит в состав активной протромбиназы Создаёт оптимальные условия для взаимодействия фактора Ха и II |
VII Проконвертин или стабильный фактор (профермент сериновой протеазы) |
Гепатоциты (в присутствии витамина К) Около 0,005 г/л (80-120% активн6ости) |
Активируется фактором III Активирует факторы IX, X (участвует в образовании протромбиназы по внешнему пути) |
VIII:С Антигемофильный глобулин (церулоплазминоподобний связывающий белок) |
Гепатоциты 0,01-0,02 г/л (60-250% активности) |
Активируется тромбином Создаёт оптимальные условия для взаимодействия факторов IXа и X |
VIII: ВФ Фактор Виллебранда (структурный белок) |
Эндодотелиоциты, мегакариоциты 80-120% активности |
Стабилизирует фактор VIII Способствует адгезии тромбоцитов |
IX Фактор Кристмаса или компонент плазменного тромбопластина, РТС-фактор (профермент сериновой протеазы) |
Гепатоциты (в присутствии витамина К) Около 0,003 г/л (70-130% активности) |
Активируется факторами IXа, VIIа Активирует фактор Х |
X Фактор Стюарта-Прауэра (профермент сериновой протеазы) |
Гепатоциты (в присутствии витамина К) Около 0,01 г/л 80-120% активности |
Активируется факторами VIIIа и VIIа Входит в состав активной протромбиназы Переходит протромбин в тромбин (IIа) |
XI Плазменный предшественник тромбопластина или РТА- фактор, фактор Розенталя (профермент сериновой протеазы) |
Гепатоциты Около 0,005 г/л (70-130% активности) |
Активируется фактором XIIa Активирует фактор IX |
XII Фактор Хагемана Или контактный фактор (профермент сериновой протеазы) |
Гепатоциты Около 0,03 г/л (70-150% активности) |
Активируется калликреином и ВМК Запускает внутренний путь свертывания крови Активирует ППК, систему фибринолиза |
XIII Фибринстабилизирующий фактор (профермент трансглутаминазы) |
Гепатоциты, мегакариоциты 0,01-0,02 г/л (70-130% активности) |
Активируется тромбином и Са2+ Стабилизирует фибрин Способствует репарации тканей |
Плазменный прекалликреин (ППК) или фактор Флетчера (профермент плазменного калликреина) |
Гепатоциты Около 0,05 г/л (60-150% активности) |
Активируется ВМК, фактором XIIa Активирует факторы VII,XII, ВМК, плазминоген |
Высокомолекулярный кининоген (ВМК) или фактор Фитцджеральда (гликопротеин) |
Гепатоциты Около 0,06 г/л (80-130% активности) |
Активирует факторы XI, XII плазминоген, ППК |
Внутренний и внешний механизмы гемостаза тесно взаимосвязаны, их разделение является в некоторой степени условным. Так, фактор VIIa активирует факторы свертывания XII и (в присутствии тканевого тромбопластина и ионов кальция) IX (рис. 14–18). В свою очередь, фактор VII может быть активирован факторами ХIIа и ХIа. Предполагается, что внешний механизм обеспечивает фоновое свертывание крови. Инициация внешнего пути гемостаза протекает быстрее (12–15 с), чем внутреннего механизма (30–42 с). Это приводит к формированию базового количества тромбина, достаточного для последующей активации факторов внутреннего каскада гемокоагуляции.
После активации фактора X внутренний и внешний пути имеют одинаковое (общее) развитие, и поэтому дальнейшие превращения факторов свертывания крови обозначают как общий путь свертывания крови.
Второй этап характеризуется активацией фактора V и образованием активного протромбиназного комплекса (активной протромбиназы) на ФЛМ из факторов Va, Xa и Са2+, способствующего превращению протромбина (фактор II) в тромбин (фактор IIа).
Третий этап — конечная фаза свертывания крови, характеризующаяся трансформацией растворенного в плазме фибриногена в фибрин, образующий каркас сгустка крови. На этом этапе происходит отщепление тромбином от молекулы фибриногена двух фибринопептидов А и двух фибринопептидов В с образованием фибрин-мономеров, полимеризующихся в димеры и далее — в тетрамеры и более крупные олигомеры, трансформирующиеся в волокна фибрина, образующие сгусток. Стабилизация сгустка фибрина осуществляется фактором XIII, активирующимся под действием тромбина (IIа) в присутствии ионов кальция, в результате чего водородные связи между мономерами фибрина трансформируются в ковалентные связи, и образующиеся сгустки фибрина становятся более прочными и устойчивыми к различным растворителям (мочевине, монохлоруксусной кислоте и др.).
Повышенное содержание в плазме крови промежуточных продуктов превращения фибриногена в фибрин служит показателем активации системы свертывания крови и наличия тромбинемии.
КОАГУЛЯЦИОННЫЙ (ВТОРИЧНЫЙ) ГЕМОСТАЗ
Основоположником современной теории свертывания крови является профессор Дерптского (Юрьевского, ныне Тартуского, университета) А. А. Шмидт. Затем его теорию уточнил П. Моравиц (1905).
В ходе вторичного гемостаза процессы коагуляции фибрина обеспечивают плотную закупорку поврежденных сосудов тромбом — красным кровяным сгустком, который содержит не только тромбоциты, но и другие клетки и белки плазмы крови. Коагуляционный гемостаз обеспечивает остановку кровотечения благодаря образованию фибриновых тромбов.Факторы свертывания крови
В свертывании крови принимают участие следующие группы факторов:
Плазменные факторы свертывания крови.
Факторы свертывания крови форменных элементов крови.
Тканевые факторы свертывания крови.
Они получили название «факторы свертывания крови» и содержатся в плазме крови, форменных элементах (эритроцитах, лейкоцитах, тромбоцитах) и в тканях. Наибольшее значение имеют плазменные факторы. Они обозначаются римскими цифрами. В физиологических условиях большинство факторов свертывания крови содержится в ней в неактивном состоянии в виде неактивных форм ферментов (за исключением IV фактора — ионов кальция).
Плазменные факторы свертывания крови:
Фибриноген — глобулярный белок, синтезируется в печени. Под влиянием тромбина превращается в фибрин. Образует фибриллярную сеть кровяного сгустка. Стимулирует регенерацию тканей.
Протромбин — гликопротеид. Под влиянием протромбиназы превращается в тромбин, обладающий протеолитической активностью по отношению к фибриногену.
Тромбопластин состоит из белка апопротеина III и фосфолипидов. Входит в состав мембран клеток крови и тканей. Является матрицей, на которой протекают реакции образования протромбиназы.
Ионы Са2+ участвуют в образовании комплексов, которые входят в состав протромбиназы. Стимулируют ретракцию сгустка, агрегацию тромбоцитов, связывают гепарин, ингибируют фибринолиз.
Проакцелерин — белок, необходим для образования тромбина. Связывает Ха-фактор с тромбином.
Исключен из классификации.
Проконвертин — гликопротеид. Необходим для образования протромбиназы.
Антигемофильный глобулин А образует комплексную молекулу с фактором Виллебранта. Необходим для взаимодействия IХа с X. При его отсутствии развивается гемофилия А.
Фактор Виллебранта (FW) образуется эндотелием сосудов, необходим для адгезии тромбоцитов и стабилизации VIII фактора.
Кристмас-фактор — антигемофильный глобулин В. Гликопротеид. Активирует Х фактор. При его отсутствии развивается гемофилия В.
Х. Фактор Стюарта-Прауэра — гликопротеид. Ха входит в состав протромбиназы. Активируется факторами VIIа и IХа. Переводит протромбин в тромбин.
Плазменный предшественник тромбопластина — гликопротеид. Активируется фактором XIIа, калликреином, высокомолекулярным кининогеном (ВМК).
Фактор Хагемана — белок. Образуется эндотелием, лейкоцитами, макрофагами. Активируется при контакте с чужеродной поверхностью, адреналином, калликреином. Запускает процесс образования протромбиназы, активирует фибринолиз, активирует XI фактор.
Фибринстабилизирующий фактор (ФСФ) — фибриназа. Синтезируется фибробластами, мегакариоцитами. Стабилизирует фибрин, активирует регенерацию.
Фактор Флетчера активирует XII фактор, плазминоген.
Фактор Фитцджеральда — высокомолекулярный кининоген. Образуется в тканях, активируется калликреином. Активирует факторы XII , XI, фибринолиз.
Тромбоцитарные факторы свертывания крови
F1 — тромбоцитарный акцелератор-глобулин;
F2 — акцелератор тромбина, фибринопластический фактор;
F3 — тромбоцитарный тромбопластин или тромбопластический фактор. Представляет собой фосфолипид мембран и гранул, высвобождается после разрушения тромбоцитов;
F4 — антигепариновый фактор. Связывает гепарин и тем самым ускоряет процесс свертывания крови;
F5 — свертывающий фактор, или фибриноген. Определяет адгезию (клейкость) и агрегацию (скучивание) тромбоцитов;
F6 — тромбостенин. Обеспечивает уплотнение и сокращение кровяного сгустка. Состоит из субъединиц А и М, подобных актину и миозину. Будучи АТФ-азой, тромбостенин сокращается за счёт энергии, освобождаемой при расщеплении АТФ;
F7 — тромбоцитарный котромбопластин;
F8 — антифибринолизин;
F9 — фибринстабилизирующий фактор;
F10 — серотонин. Вызывает сужение сосудов и уменьшение кровопотери;
F11 — фактор агрегации — АДФ, обеспечивающий скучивание (адгезию) тромбоцитов.
Эритроциты.
В эритроцитах содержатся факторы, аналогичные тромбоцитарным: тромбопластин, АДФ, фибриназа. Разрушение эритроцитов способствует образованию тромбоцитарной пробки и фибринового сгустка. Массовые разрушения эритроцитов (при переливании несовместимой по групповой принадлежности или Rh-фактору крови) представляет большую опасность в связи с возможностью внутрисосудистого свертывания крови.
Лейкоциты.
В лейкоцитах содержатся тромбопластический, антигепариновый, гепарин (базофилы), активаторы фибринолиза. Моноциты и макрофаги синтезируют II, VII, IX, X факторы системы свертывания и апопротеин III, который является компонентом тромбопластина. Поэтому при инфекционных и обширных воспалительных процессах возможен запуск внутрисосудистого свертывания крови (ДВС-синдром), который может привести к смерти больного.
Ткани (особенно стенки сосудов).
Простациклин (в эндотелии сосудов) является мощным ингибитором агрегации. От соотношения количества простациклина (ингибитора агрегации) и тромбоксана (мощного стимулятора агрегации тромбоцитов) зависит степень агрегации тромбоцитов.
Активный тромбопластин.
Антигепариновый.
Естественные антикоагулянты.
Активаторы и ингибиторы фибринолиза.
Среди тканевых факторов наиболее заметная роль принадлежит тканевому тромбопластину (фактор III). Им богаты ткани головного мозга, плацента, легкие, предстательная железа, эндотелий. Поэтому разрушение тканей также может приводить к развитию ДВС-синдрома.
Схема последовательной активации факторов свертывания крови
Процесс свертывания крови — ферментативный цепной (каскадный) процесс перехода растворимого белка фибриногена в нерастворимый фибрин. Каскадным он называется потому, что в процессе гемокоагуляции происходит последовательная цепная активация факторов свертывания крови. Свертывание крови является матричным процессом, так как активация факторов гемокоагуляции осуществляется на матрице. Матрицей могут быть фосфолипиды мембран разрушенных форменных элементов (главным образом II тромбоцитов) и обломки клеток тканей.
Процесс свертывания крови осуществляется в три фазы.
1-я фаза — образование протромбиназы.
В крови, в зоне поврежденного сосуда, образуется активная протромбиназа, превращающая неактивный протромбин в тромбин.
Процесс образования протромбиназы — самый длительный и лимитирует весь процесс свертывания крови. Различают два пути формирования протромбиназы:
1. внешний, активируемый при повреждении сосудистой стенки и окружающих тканей;
2. внутренний — при контакте крови с субэндотелием, компонентами соединительной ткани сосудистой стенки или при повреждении самих клеток крови.
Внешний механизм формирования протромбиназы осуществляется при поступлении тканевого тромбопластина (фосфолипидные осколки мембран поврежденных клеток) в кровоток из поврежденных тканей и сосудистой стенки, взаимодействии его с плазменным фактором VII и ионами кальция. Образующийся в результате комплекс превращает неактивный плазменный фактор X в его активную форму (Ха).
Внутренний механизм запускается при появлении разрушенных и поврежденных клеток крови или при контакте фактора XII с субэндотелием.
Первый этап активации внутренней системы состоит в том, что фактор XII вступает в контакт с «чужеродными» поверхностями. В активации и действии фактора XII участвуют также высокомолекулярный кининоген, тромбин или трипсин.
Далее следует активация факторов XI и IX. После образования фактора IХа формируется комплекс: «фактор IХа + фактор VIII (антигемофильный глобулин А) + тромбоцитарный фактор 3 + ионы кальция». Этот комплекс активирует фактор Х.
Фактор Ха образует с фактором V и тромбоцитарным фактором 3 новый комплекс, называемый протромбиназой, Активация протромбокиназы по внешнему пути занимает около 15 секунд, по внутреннему — 2–10 минут.
2-я фаза — образование тромбина.
Протромбиназа в присутствии ионов Са++ превращает неактивный фермент плазмы протромбин в его активную форму — тромбин.
3-я фаза — образование фибрина.
Превращение растворимого фибриногена в нерастворимую форму фибрин. Тромбин представляет собой пептидазу, вызывающую частичный протеолиз молекулы фибриногена, превращая его в фибрин.
Эта фаза протекает последовательно, в три этапа.
Первый этап — протеолитический.
Под действием тромбина происходит ферментативное расщепление димера фибриногена на две субъединицы. Тромбин отщепляет от молекулы фибриногена 4 пептида (два пептида А и два пептида В). В результате образуются фибрин-мономеры.
Второй этап — полимеризационный.
В результате полимеризации из молекул фибрин-мономеров образуется растворимый фибрин-полимер «S». Для полимеризации необходимо присутствие ионов кальция.
В основе этого неферментативного этапа лежит спонтанный самосборочный процесс, приводящий к агрегации фибрин-мономеров. Каждый из мономеров имеет 4 свободных центра связывания. Соединяясь ими друг с другом, мономеры в течение нескольких секунд формируют волокна фибрина. Процесс полимеризации происходит по принципу «бок в бок» или «конец в конец». Самосборка фибрина осуществляется путем формирования продольных и поперечных связей между фибрин-мономерами с образованием фибрин-полимера (фибрин S). Волокна фибрина S легко лизируются под влиянием не только плазмина, но и комплексных соединений, обладающих неферментативной фибринолитической активностью.
Третий этап — ферментативный.
Под влиянием фибринстабилизирующего фактора (FXIII) образуется нерастворимый фибрин («J»). Фибринстабилизирующий фактор активируется ионами Са++ и тромбином.
Под влиянием активного фибринстабилизирующего фактора (фактор XIII активируется тромбином в присутствии ионов кальция) в фибрине образуются дополнительные дисульфидные связи, и сеть фибрина становится нерастворимой (растворимый фибрин S переходит в нерастворимый фибрин I).
В фибриновую сеть вовлекаются форменные элементы крови, в результате чего формируется кровяной сгусток.
Тромб в дальнейшем подвергается двум процессам:
1) ретракции (сокращению). Первоначально сгусток еще относительно рыхлый и он подвергается ретракции, которая обеспечивается белком тромбостенином (F-6 тромбоцитов). Сгусток уплотняется, становится более компактным и стягивает края раны;
2) фибринолизу (растворению).
Время свертывания крови 5–7 мин (по Ли-Уайту). Ускорение процесса свертывания крови называется гиперкоагуляцией, замедление этого процесса — гипокоагуляцией.
Схема свертывания крови изображена на рисунке 1.
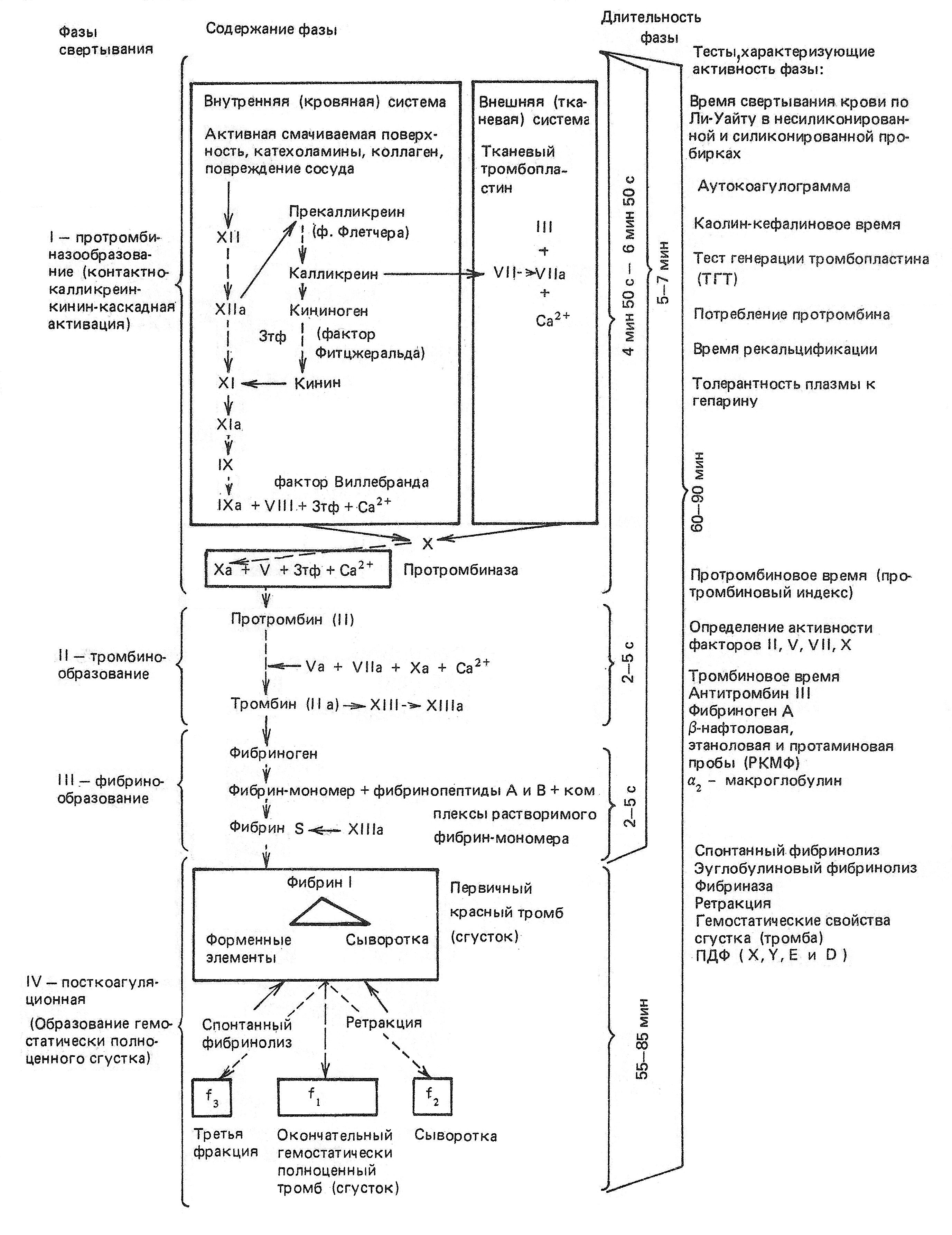
Рисунок 1 — Схема свертывания крови (по Е. П. Иванову, 1979, 1980).
Стрелки сплошные — активирующее действие, пунктирные — превращение
=================================
