
- •1 Классификация присадок к нефтепродуктам
- •Присадки можно классифицировать:
- •Рассмотрим следующий принцип классификации:
- •Присадки общего назначения для топлив и масел:
- •Различают 2 типа:
- •Присадки для дистиллятных нефтяных топлив.
- •3. Присадки для нефтяных масел.
- •2. Производство ароматических углеводородов
- •3. Методы извлечения ароматических соединений из риформата.
- •4. Промышленные методы производства жидких олефинов. Каталитическое дегидрирование парафиновых углеводородов. Методы выделения олефинов из пр. Реакции.
- •5. Олигомеризация газообразных олефинов (этилена, пропилена, изобутилена). Поточные схемы производства.
- •6. Производство изопропилбензола алкилированием бензола пропиленом. Катализаторы. Поточные схемы производства.
- •7. Совместное производство фенола и ацетона
- •2) Выделение технического гидропероксида изопропилбензола
- •8.Производство алкилбензолов алкилированием бензола жидкими олефинами
- •9. Сульфокатиониты как катализаторы процесса алкилирования фенола жидкими олефинами. Преимущества этих катализаторов.
- •10. Химия и технология производства алкилфенолов на сульфокатионитах
- •Химизм сульфидирования жидких олефинов элементной серой. Области применения продуктов сульфидирования олефинов
- •12. Методы получения синтетических жирных кислот из твердых парафинов
- •Обработка реакционной массы (оксидата):
- •13. Сущность метода Коха в процессе производства синтетических жирных кислот. Катализатор процесса.
- •14. Растительные и животные жиры как источник высших жирных кислот и спиртов
- •15. Химизмы производства акриловой кислоты. Области практического применения.
- •16. Ацетонциангидринный метод производства метакриловой кислоты и её метилового эфира. Вязкостно-депрессорные присадки к маслам типа полиметакрилатов. Поточная схема производства этих присадок.
- •16!!!! (Продолжение) Полиметакрилаты – присадки к маслам. Методы получения, функциональные свойства
- •17. Оксигенаты — компоненты углеводородных топлив. Мтбэ. Химия и технология производства. Экологические аспекты производства и применения
- •Химизм и оптимальные условия проведения процесса.
- •Экологические аспекты производства мтбэ
- •Поточная схема производства мтбэ. Типы реакционных устройств
- •18.Методы сульфирования алкилароматических соединений. Алкиларилсульфонаты – присадки к смазочным маслам. Методы получения
- •Н2sо4 или н2sо4∙ sо3 (олеум)
- •Комплексы sо3 :
- •Метод Гершеновича:
- •21. Алкенилсукцинимиды – присадки к смазочным маслам. Стадии производства, функциональные свойства
- •22. Химизм методов получения присадки к маслам и топливам «Ионол»
- •23. Пространственно затрудненные фенолы - антиокислительные присадки к углеводородным топливам и смазочным маслам. Типы присадок. Механизм ингибирования окисления углеводородов
- •24. Механизм ингибированного окисления ув. Роль пространственно затрудненных фенолов и разрушителей гидроперекиси.
7. Совместное производство фенола и ацетона
Процесс складывается из окисления изопропилбензола (ИПБ) в гидропероксид (ГП), концентрирования ГП, кислотного разложения ГП и ректификации продуктов разложения.
Окисление изопропилбензола проводится в жидкой фазе при t 110÷130°С в присутствии инициатора — самого гидропероксида ИПБ.
Окисление ИПБ протекает значительно легче, чем парафиновых углеводородов, что связано с более низкой энергией разрыва связи С—Н, находящейся в а-положении к ароматическому кольцу (309 против 380÷400 кДж/моль для парафина).
При температурах 70÷90°С ГП ИПБ вполне устойчива, а окисление ИПБ идет медленно, по закону неразветвленной цепной реакции. Выше 100°C ГП начинает распадаться на радикалы и реакция приобретает вырожденно-разветвленный хар-р.
Процесс идет по радикально-цепному механизму.
Большое влияние на обрыв цепи и, на скорость окисления могут оказывать ингибиторы (кислые продукты (НСООН), фенол, сернистые и ненасыщенные соединения.
Кислые продукты сами по себе не ингибируют процесс окисления, но в их присутствии ГП ИПБ разлагается на фенол и ацетон, а фенол является ингибитором ок-ния.
Продукты распада диметилфенилкарбинол (ДМФК) и ацетофенон (АФ) не тормозят процесс. Диметилфенилкарбинол и ацетофенон являются основными побочными продуктами, снижающими селективность процесса.
Большое значение при окислении изопропилбензола имеет чистота исходного углеводорода. ИПБ не должен содержать фенола, сернистых и ненасыщенных соединений, являющихся ингибиторами окисления. Для очень чистых образцов ИПБ скорость накопления гидропероксида достигает 10÷13%/ч. В пром.условиях скорость накопления колеблется в пределах 5÷7 %/ч, что объясняется ингибирующим влиянием примесей.
На процесс окисления изопропилбензола большое влияние оказывает рН среды. Скорость окисления в кислой среде (рН 6) значительно снижается, а в щелочной среде (рН 7,5) возрастает. Это связано с необходимостью нейтрализации кислых продуктов, содержащихся в сырье и образующихся в процессе распада гидропероксида. Кроме того, щелочь ускоряет инициирование цепей окисления.
2) Выделение технического гидропероксида изопропилбензола
Гидропероксид изопропилбензола начинает разлагаться с заметной скоростью при 145°С, причем разложение сопровождается саморазогреванием. Поэтому выделение гидропероксида из реакционной массы должно осуществляться в очень мягких условиях.
Гидропероксид ИПБ может быть извлечен из реакционной массы окисления химическим или физическим методами.
В химич.методе гидропероксид путем обработки р-ром едкого натра превращают в твердую натриевую соль, которую затем отфильтровывают. Для удаления увлеченного осадком маточного раствора соль промывают легким растворителем или растворяют в воде. Из водно-щелочного раствора гидропероксид выделяют в виде мутного маслянистого слоя путем пропускания через раствор диоксида углерода. Таким путем получается 97÷98%-ный технический гидропероксид.
Физический метод выделения сводится к концентрированию гидропероксида перегонкой. Реакционная масса после окисления подвергается двухступенчатой ректификации в вакууме для отгонки непрореагировавшего изопропилбензола и воды (концентрированный гидропероксид содержит 90÷93% основного вещества).
Технико-экономическое сравнение 2 методов выделения гидропероксида изопропилбензола показало, что физический метод обладает бесспорными преимуществами.
3)
Разложение гидропероксида изопропилбензола
по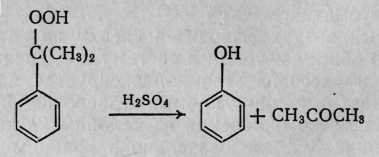 д
д-ем H2SO4
(фенол и
ацетон):
д
д-ем H2SO4
(фенол и
ацетон):
Технический ГПИПБ содержит также небольшие количества диметилфенил-карбинола и ацетофенона, образовавшихся в результате его термического распада. Из диметилфенилкарбинола далее могут образоваться сложный фенол (кумилфенол), а-метилстирол, димер а-метилстирола и смолистые вещества.
В промышленных условиях применяют 98%-ную серную кислоту в виде раствора в ацетоне. Максимальный выход целевых продуктов достигается при концентрации 0,07÷0,1 % H2SO4 от массы гидропероксида.
Процесс разложения гидропероксида зависит также от температуры. Оптимальная температура 50÷60˚С при времени контакта примерно 3,5 мин.
В процессе образуется около 7% побочных продуктов по отношению к продуктам основной реакции. Они получаются главным образом на стадии образования гидропероксида. Большое значение для экономики процесса производства фенола кумольным методом имеет использование побочных продуктов и их реконверсия в фенол. Особенно это относится к фенольной смоле.
Алкилфенолы исп-ся в основном для производства присадок и неионогенных ПАВ.
Сульфокатионит – сульфированный сополимер стирола с дивинилбензолом.
Алкилирование фенола:

 ОН R-CH=CH2__
R’-
__OH
ОН R-CH=CH2__
R’-
__OH
H+
(R’__ __OH)

R’
H2S04 использовали до начала 1960-х гг, позже перевели на сульфокатиониты (Исагулянц), процесс стал:
Непрерывным; Без стоков; Многотоннажным
Соотношение фенол:олефин = (2,0÷2,5):1,0
Алкилфенолы получались очень грязные в виде кубовых остатков, сверху отгоняли непрореагировавшие вещества. Кроме того, имела место реакция переалкилирования:
R(R)-С6Н3-ОН + С6Н5-ОН → 2 R-С6Н4-ОН
(1:5 моль)
