- •1 Классификация присадок к нефтепродуктам
- •Присадки можно классифицировать:
- •Рассмотрим следующий принцип классификации:
- •Присадки общего назначения для топлив и масел:
- •Различают 2 типа:
- •Присадки для дистиллятных нефтяных топлив.
- •3. Присадки для нефтяных масел.
- •2. Производство ароматических углеводородов
- •3. Методы извлечения ароматических соединений из риформата.
- •4. Промышленные методы производства жидких олефинов. Каталитическое дегидрирование парафиновых углеводородов. Методы выделения олефинов из пр. Реакции.
- •5. Олигомеризация газообразных олефинов (этилена, пропилена, изобутилена). Поточные схемы производства.
- •6. Производство изопропилбензола алкилированием бензола пропиленом. Катализаторы. Поточные схемы производства.
- •7. Совместное производство фенола и ацетона
- •2) Выделение технического гидропероксида изопропилбензола
- •8.Производство алкилбензолов алкилированием бензола жидкими олефинами
- •9. Сульфокатиониты как катализаторы процесса алкилирования фенола жидкими олефинами. Преимущества этих катализаторов.
- •10. Химия и технология производства алкилфенолов на сульфокатионитах
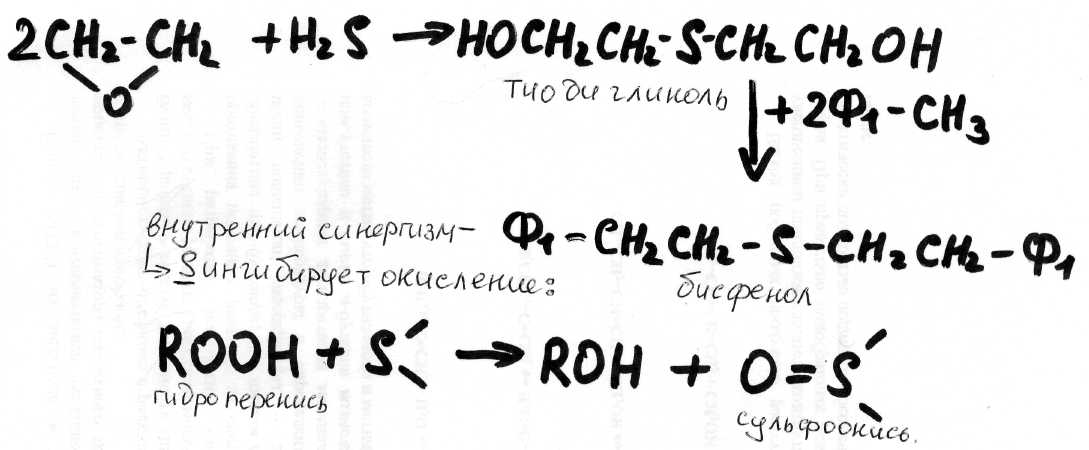
- •Химизм сульфидирования жидких олефинов элементной серой. Области применения продуктов сульфидирования олефинов
- •12. Методы получения синтетических жирных кислот из твердых парафинов
- •Обработка реакционной массы (оксидата):
- •13. Сущность метода Коха в процессе производства синтетических жирных кислот. Катализатор процесса.
- •14. Растительные и животные жиры как источник высших жирных кислот и спиртов
- •15. Химизмы производства акриловой кислоты. Области практического применения.
- •16. Ацетонциангидринный метод производства метакриловой кислоты и её метилового эфира. Вязкостно-депрессорные присадки к маслам типа полиметакрилатов. Поточная схема производства этих присадок.
- •16!!!! (Продолжение) Полиметакрилаты – присадки к маслам. Методы получения, функциональные свойства
- •17. Оксигенаты — компоненты углеводородных топлив. Мтбэ. Химия и технология производства. Экологические аспекты производства и применения
- •Химизм и оптимальные условия проведения процесса.
- •Экологические аспекты производства мтбэ
- •Поточная схема производства мтбэ. Типы реакционных устройств
- •18.Методы сульфирования алкилароматических соединений. Алкиларилсульфонаты – присадки к смазочным маслам. Методы получения
- •Н2sо4 или н2sо4∙ sо3 (олеум)
- •Комплексы sо3 :
- •Метод Гершеновича:
- •21. Алкенилсукцинимиды – присадки к смазочным маслам. Стадии производства, функциональные свойства
- •22. Химизм методов получения присадки к маслам и топливам «Ионол»
- •23. Пространственно затрудненные фенолы - антиокислительные присадки к углеводородным топливам и смазочным маслам. Типы присадок. Механизм ингибирования окисления углеводородов
- •24. Механизм ингибированного окисления ув. Роль пространственно затрудненных фенолов и разрушителей гидроперекиси.
21. Алкенилсукцинимиды – присадки к смазочным маслам. Стадии производства, функциональные свойства
Алкенилсукцинимиды относятся к моюще-диспергирующим беззольным присадкам.
В основе их получения лежит реакция Дильса-Альдера.
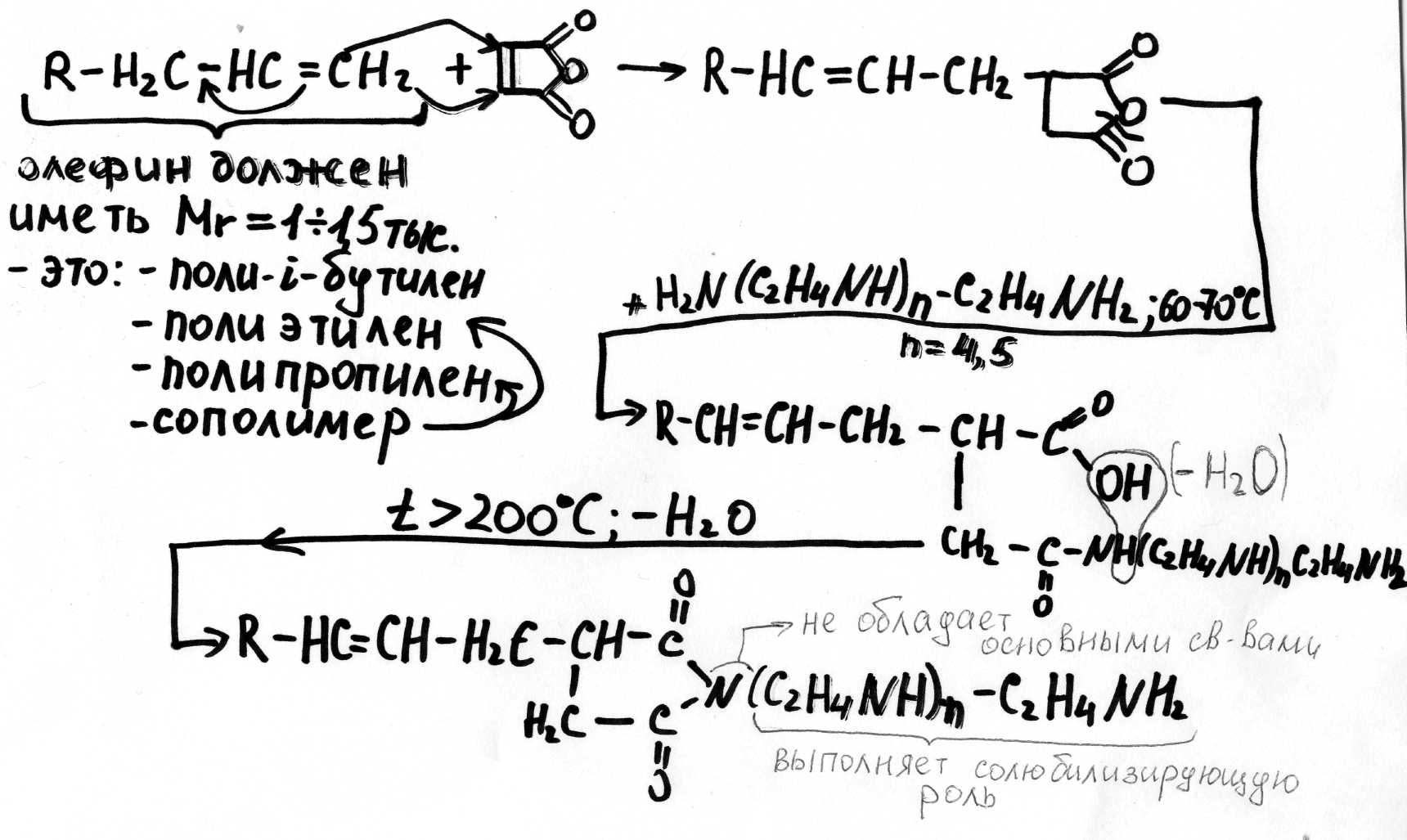
Алкилсукцинимиды должны использоваться вместе с зольными сульфонатными или алкилсульфонатными присадками
22. Химизм методов получения присадки к маслам и топливам «Ионол»
Широкое распространение из антиокислителей нашел ИОНОЛ – 2,6 –дитретбутил-4-метилфенол. Ионол производят в больших масштабах и добавляют к маслам (в концентрациях 0,2-0,3%), к гидрогенизационным РТ (до 0,003%), к авиационным бензинам (до 0,01%), к АБ (0,03-0,1% на нестабильный компонент).
Ионол получают двумя способами: на основе фенола и крезола.
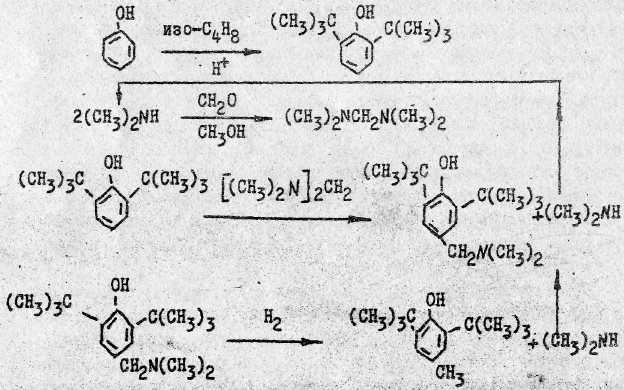
Получение ионола из фенола состоит из следующих стадий:
Алкилирование фенола изобутиленом в присутствии фенолята алюминия с получением 2,6-дитретбутилфенола.
Пол-е бисамина при вз-вии диметиламина с формальдегидом в р-ре метил. спирта
Аминометилирование 2,6-дитретбутилфенола бисамином
Гидрогенолиз основания Манниха до 2,6-дитретбутил-4-метил фенола и выделение ионола.
получение ионола алкилированием крезола изобутиленом проводят при 75-80°С в присутствии серной кислоты и при мольном отношении крезол:изобутилен = 1:3 с последующей нейтрализацией содосолевым раствором (соль добавляется для уменьшения растворимости п-крезола в промывных водах):
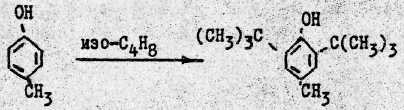
после дистилляции продуктов реакции целевой продукт – ионол – перекристаллизовывается из четыреххлористого углерода.
В качестве катализаторов предложены также катионнообменные смолы, алкилсульфокислоты, фторид бора и его молекулярные соединения и др.
23. Пространственно затрудненные фенолы - антиокислительные присадки к углеводородным топливам и смазочным маслам. Типы присадок. Механизм ингибирования окисления углеводородов
Механизм окисления УВ:
1. зарождение цепи:
RH + O2 → R∙ + HOO∙ ; 2RH + O2 → 2R∙ + H2O2
2. продолжение цепи:
R∙ +O2 → RO2∙ ; RO2∙ +RH → R∙ + ROOH
3. разветвление цепи (вырожденное):
ROOH → RO∙ + ∙OH ; 2ROOH → RO∙ +H2O + ROO∙
Рабинович обнаружил, что распад гидроперекиси происходит в т.н. «клетке Рабиновича», где образуется сразу 2 радикала, откуда они потом выходят в объем: [RO∙∙OH].
Пространственно затрудненные фенолы взаимодействуют с радикалами, радикалы гибнут и в объем не выходят – происходит обрыв цепи (особенно заметно при пониженных температурах, при повышенных – сглаживается):
InH + R∙ → RH + In∙
InH + RO∙ → ROH + In∙
Радикал ингибитора неактивен.
К присадкам такого типа относятся ионол, агидол, фенозан – бис-, трис- и тетрафенолы.
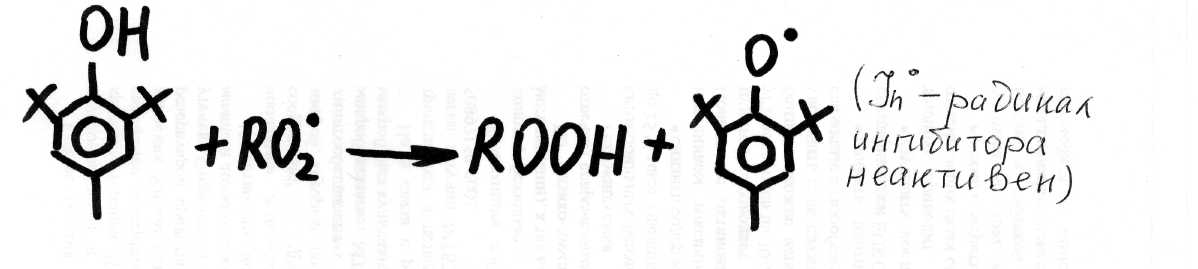


В Швейцарии получали трисфенол:

Московский НПЗ – производство фенозана-1.
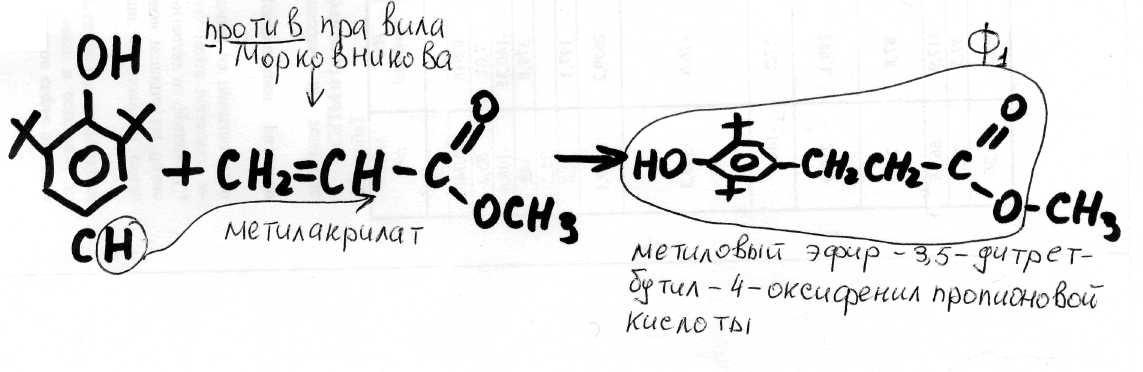
Далее – переэтерификация:
С этиленгликолем

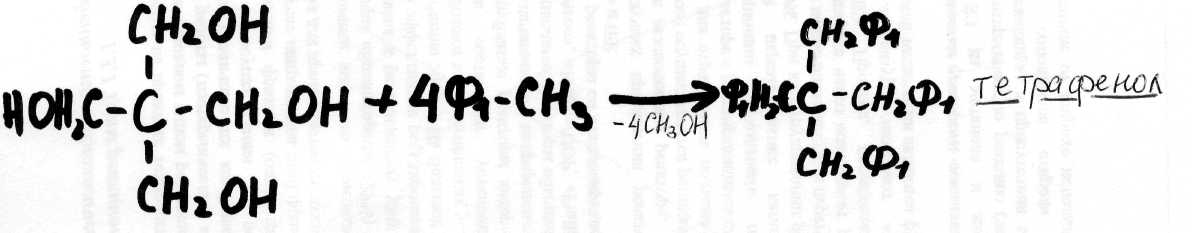
С пентаэритритом
С тиодигликолем