- •VI. Физико-химические процессы в биологических мембранах §6.1. Структура мембран
- •6.1.1. Жидкокристаллическая модель мембран
- •6.1.2. Динамические свойства мембран
- •§6.2. Основные функции мембран
- •6.2.1. Эндо- и экзоцитоз
- •6.2.2. Пассивный ионный и молекулярный транспорт через мембрану
- •Проницаемость мембран
- •Пассивный транспорт через мембранные каналы
- •Калиевый канал
- •Натриевый канал
- •6.2.3. Симпорт и антипорт
- •6.2.4. Активный ионный транспорт
- •Аденозинтрифосфатаза (атФаза)
- •Цикл Na/k-атФазы
- •§6.3. Потенциал покоя клеточных мембран
- •6.3.1. Механизм образования
- •6.3.2. Потенциал покоя
- •§6.4. О роли мембран
6.2.3. Симпорт и антипорт
Энергия, запасенная в мембранном градиенте Na+, часто используется для обеспечения транспорта других молекул через мембрану. Так одновременно с диффузией иона натрия через канал вместе с ним может пройти внутрь клетки молекула сахара, транспорт которой в таком случае называется симпортом (от греч. sýn – вместе), то есть движением частиц в одном и том же направлении (рис. 6–9). С одним ионом Na+ может симпортироваться одна молекула глюкозы.
Транспорт аминокислот в клетку подобен транспорту сахаров. Существует несколько различных систем симпорта, специализированных для отдельных групп родственных аминокислот.
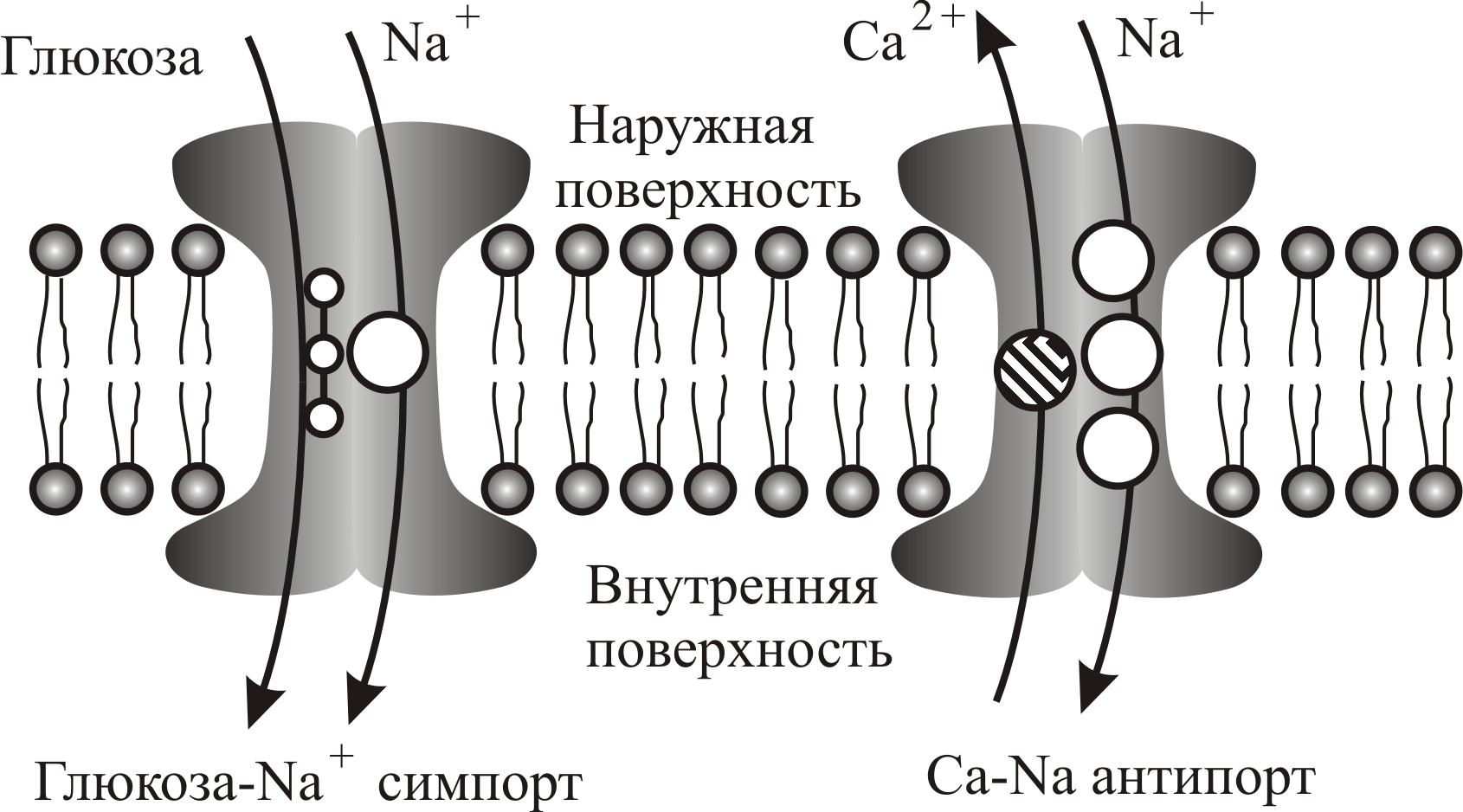
Рис. 6–9. Схемы пассивных симпорта глюкозы и антипорта кальция через белковые структуры клеточной мембраны совместно с диффузионным транспортом ионов натрия в клетку (против градиента концентрации натрия)
Поддержание высокого градиента кальция (см. табл.VI–1) обеспечивается кальций-натриевым антипортом (движением частиц в противоположных направлениях), при котором один ион кальция Са2+ проходит навстречу трем ионам натрия при диффузии Na+ (рис. 6–9).
В первом случае (рис. 6–9) ион Na+, связывается электростатическими силами с молекулой глюкозы и является ионом – переносчиком.
Во втором случае, три иона натрия, двигаясь внутрь клетки, блокируют положительно заряженные центры на поверхности канала так, что потенциал, меняющийся вдоль канала при движении ионов Na+, обеспечивает одностороннюю проницаемость канала для ионов Са2+ в направлении из клетки наружу.
Движущей силой для транспорта молекул в указанных выше случаях является значительный градиент концентрации ионов натрия.
6.2.4. Активный ионный транспорт
Активный транспорт — перенос частиц в направлении градиента электрохимического потенциала, то есть из областей с мéньшим значением электрохимического потенциала в области с бόльшим значением. Поэтому этот процесс не может идти самопроизвольно, а только в сопряжении с процессом гидролиза АТФ, то есть за счет энергии, запасенной в ковалентных связях.
Примером такого типа транспорта является процесс переноса ионов Na+ и K+ через мембрану, приводящий к асимметричному распределению ионов Na+ и K+ в цитоплазме клетки и окружающей среде.
Неравновесное распределение ионов Na+ и K+ является дополнительным депо энергии. За счет этой энергии работают белки – переносчики, переносящие питательные вещества (сахара и аминокислоты) через мембрану внутрь клетки.
Аденозинтрифосфатаза (атФаза)
Для активного транспорта ионов Na+ и К+ расходуется энергия гидролиза находящихся в клетках АТФ. Например, в нейронах мозга на этот транспорт затрачивается ~30% всего фонда энергии, запасенной в аденозинтрифосфате. Интересно, что мозг во время сна затрачивает на поддержание разницы концентраций ионов почти столько же энергии, как во время работы. Энергия идет главным образом на активацию специального фермента – сложного белка, который называется активируемой аденозинтрифосфатазой, или сокращенно – АТФазой.
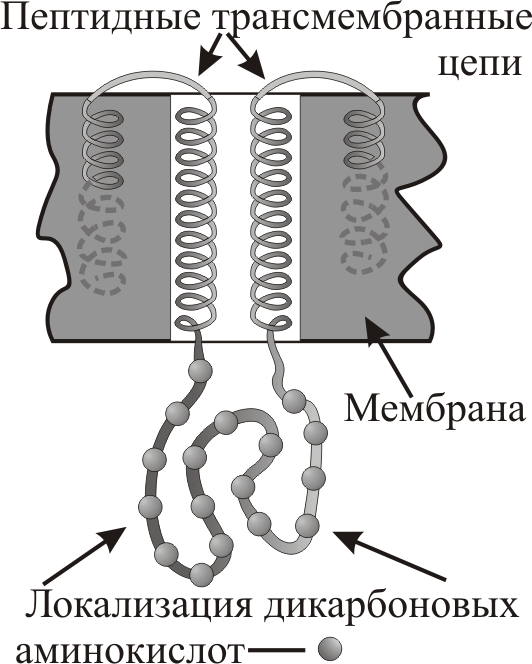
Этот фермент представляет собой сложный белок, состоящий из двух полипептидных цепей, встроенных в мембрану клетки. Полипептидная цепь АТФазы несколько раз пересекает мембранный матрикс. Пронизывающие мембрану α-спирали белка с внутренней стороны мембраны образуют ряд петель. В одной из петель локализованы активный центр, где осуществляется связывание и гидролиз АТФ, и участок фосфорилирования. В другой аналогичной петле (рис. 6–10) имеются центры связывания ионов Na+ и K+.
|
Рис. 6–10. Две полипептидные трансмембранные цепи фермента Na/K-АТФазы, образующие петлю. Серыми точками указана локализация дикарбоновых аминокислот (кислых), кислород которых формирует центры связывания ионов Na+и K+. При конформационном переходе фермента петля вдвигается между колоннами и оказывается по другую сторону мембраны. Таким образом, канал становится доступным для ионов, то с одной, то с другой стороны мембраны |
Взаимодействие ионов Na+ и K+ с центрами связывания осуществляется посредством координационных связей ионов с атомами кислорода, принадлежащими дикарбоновым аминокислотам белка – аспарагиновой и глутаминовой. Атомы кислорода этих кислот, располагаясь упорядоченно, формируют решетчатую структуру, обладающую сродством либо к ионам Na+ (конформация Е1, рис. 6–11а), либо к ионам K+ (конформация Е2, рис. 6–11б).
|
Рис. 6–11. Кристаллические структуры, образуемые атомами кислорода аминокислот фермента АТФазы в двух конформациях: Е1 – при связывании трех ионов натрия (а) и Е2 – при связывании двух ионов калия (б) |
Na/K–АТФаза поддерживает нужную асимметрию ионных концентраций, работая как молекулярная машина по перекачке ионов Na+ и K+ в направлении градиента их концентрации, используя для этого энергию гидролиза АТФ.