
- •V. Энергетический обмен клетки
- •§5.1. Метаболические реакции
- •Энергетически сопряженные реакции
- •§5.2. Модель молекулярного источника энергии
- •§5.3. Высокоэнергетические соединения – макроэрги. Атф
- •§5.4. Экзоэргические реакции. Гидролиз
- •§5.5. Окислительно-восстановительные реакции
- •5.5.1. Окислительные процессы в биологии
- •5.5.2. Ферментативное окисление
- •§5.6. Энергетическое сопряжение в реакциях фосфорилирования
- •§5.7. Законы биоэнергетики
- •§5.8. Клеточное дыхание
- •5.8.1. Общая схема
- •5.8.2. Две стадии клеточного дыхания
- •I. Первая стадия клеточного дыхания
- •II. Второй этап клеточного дыхания
- •§5.9. F1f0-атФсинтаза
- •5.9.1. Структура
- •5.9.2. Основные функции
- •5.9.3. Принцип действия
- •5.9.4. Синтез атф
- •5.9.5. Гидролиз атф
- •5.9.6. F1f0-atФсинтаза как биорегулятор клетки
- •§5.10. Межмолекулярный перенос энергии в биоструктурах
- •5.10.1. Химический и физический способы переноса энергии
- •5.10.2. Фотовозбуждение сложных молекул
- •5.10.3. Индуктивно-резонансный механизм миграции энергии
- •5.10.4. Модели индуктивно-резонансной миграции энергии
- •Механическая модель
- •Квантово-механическая модель
- •5.10.5. Обменно-резонансный механизм
- •5.10.6. Экситонный механизм
- •5.10.7. Некоторые замечания о механизмах переноса энергии фотовозбуждения
- •§5.11. Перенос электрона. Электронно-конформационное взаимодействие
- •5.11.1. Электронно-колебательное взаимодействие
- •5.11.2. Перенос электрона в окислительно-восстановительных реакциях
- •5.11.3. Проводимость белков
- •5.11.4. Полупроводниковая концепция транспорта
- •5.11.5. Химический механизм переноса заряда
- •5.11.6. Биологическое значение переноса заряда
- •§5.12. Фотосинтез
- •§5.13. Эволюция биоэнергетики
- •5.13.1. Ультрафиолетовый фотосинтез атф
- •5.13.2. О производстве энергии в экстремальных условиях
- •§5.14. Искусственные молекулярные устройства, моделирующие процессы переноса
II. Второй этап клеточного дыхания
В митохондриях происходит и второй этап клеточного дыхания. Митохондрии являются «энергетическими станциями» клеток, ибо в них происходит улавливание энергии поставляемой окислительными процессами. Энергетическое сопряжение окислительных процессов в митохондриях с генерацией АТФ (фосфорилированием) называется окислительным фосфорилированием. Окислительное фосфорилирование является столь важным жизненным процессом, что нарушение его нормального хода не совместимо с жизнью.
Признанной моделью энергетического сопряжения (в реакциях окислительного фосфорилирования в дыхательной цепи клеток) считается модель П. Митчелла, за развитие которой ему в 1979 г. присуждена Нобелевская премия (рис. 5–12). Хемиосмотическая теория Митчелла окислительного фосфорилирования связывает химические (хеми…) и транспортные (осмотические, от греч. osmosis – толчок, давление) процессы.
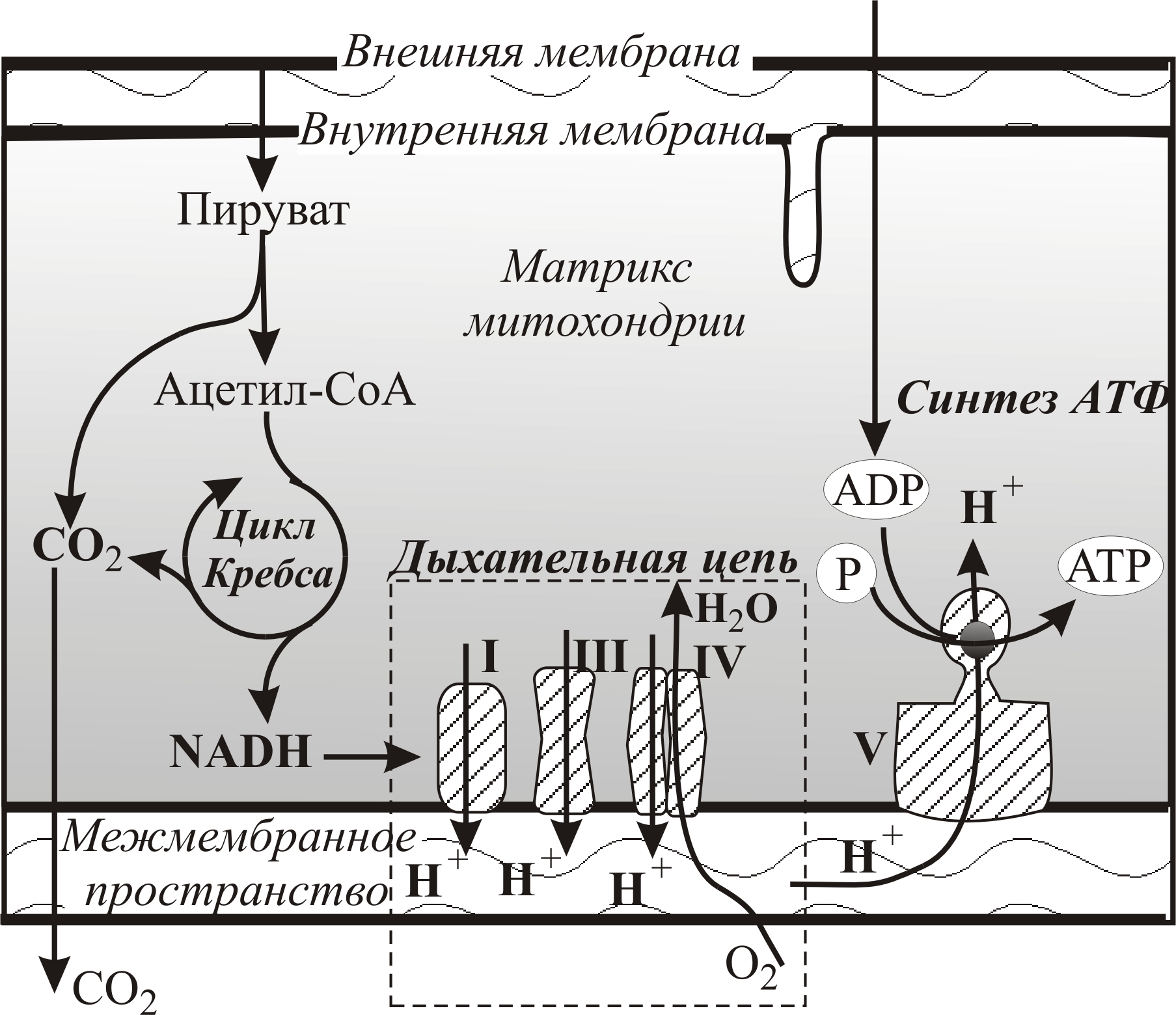
Рис. 5–12. Схема процессов окисления, происходящих в митохондрии. Дыхательная цепь обведена штриховой рамкой. Окислительный процесс в дыхательной цепи энергетически сопряжен с процессом фосфорилирования АДФ и синтеза АТФ в комплексе V. При окислении компонентов дыхательной цепи (в штриховой рамке) генерируются ионы водорода (протоны Н+), которые выходят из матрикса митохондрий на наружную сторону митохондриальной мембраны (черные стрелки) и создают необходимый для синтеза АТФ градиент концентраций ионов водорода
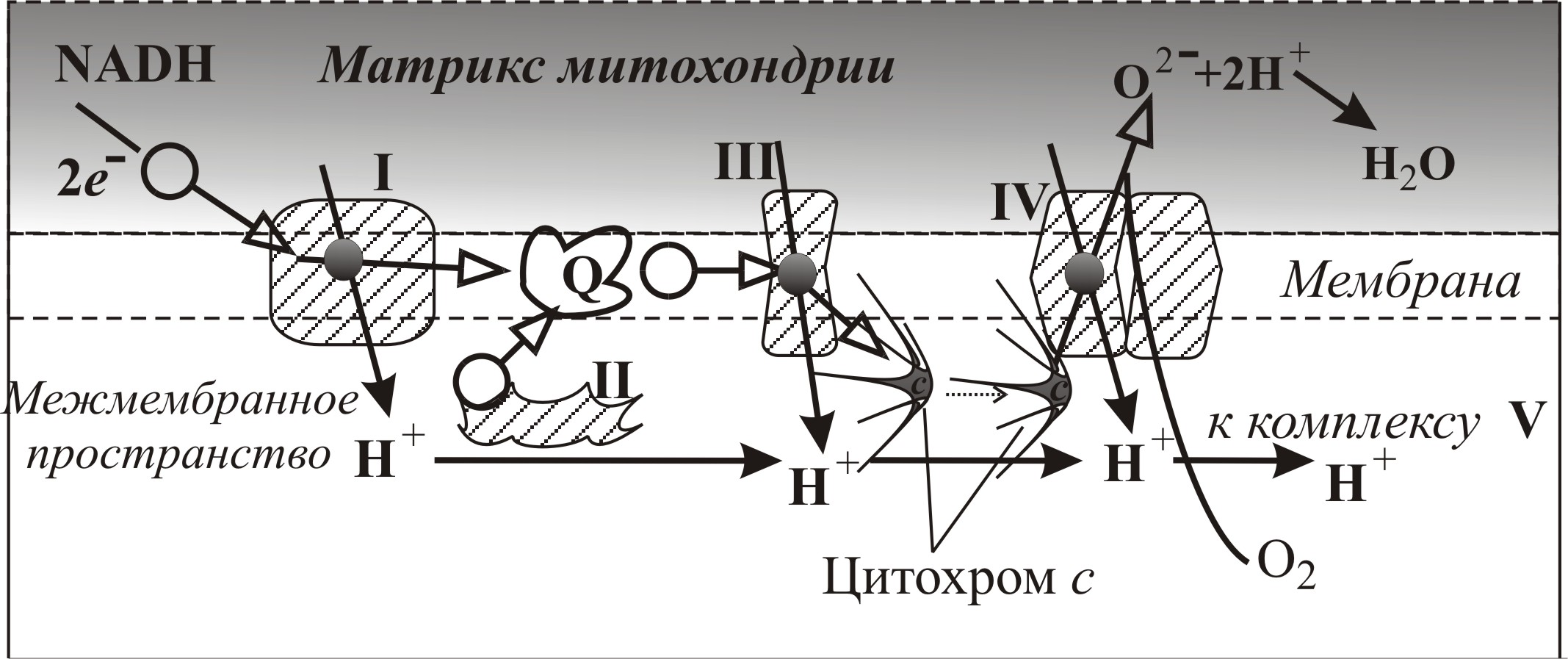
Рис. 5–13. Процессы переноса электронов (светлые стрелки) и протонов (черные стрелки) через мультиферментные комплексы I, II, III и IV дыхательной цепи
Согласно этой модели, на втором, кислородном этапе клеточного дыхания, электроны, образующиеся при дегидрировании (отщеплении водорода) NADH (акцептора водорода, АсН2), передаются в дыхательную цепь (рис. 5–12 и 5–13). В молекулах NADH (или других АсН2) электроны находятся в высокоэнергетическом состоянии, сохраняя энергию, приобретенную от «сжигания» углеводов, жиров и аминокислот.
Дыхательная цепь включает три белковых мультиферментных комплекса (комплексы I, III, IV), встроенных во внутреннюю митохондриальную мембрану, комплекс II, одновременно принадлежащий циклу Кребса, и две подвижные молекулы – переносчика: кофермент Q (убихинон) и цитохром с. Каждый комплекс состоит, как минимум, из пяти субъединиц и кофакторов, между которыми возможен перенос электронов. Комплекс V (АТФ-синтаза) не принимает участия в переносе электронов.
На рис. 5–13 показаны два пути переноса электронов на кофермент Q: через комплексы I и II. Восстановленный (присоединивший электроны) кофермент Q, двигаясь, как и последующие коферменты, через липидный слой мембраны, диффузно переносит электроны в комплекс III.
Комплекс III, в свою очередь, поставляет их на небольшой подвижный гемсодержащий белок цитохром с. Каждый цитохром, благодаря наличию простетической группы в виде железосодержащего гема (такой же гем содержится в гемоглобине (см. с. 282, 428)) способен передавать один электрон по схеме
Fe3+ + е– ↔ Fe2+.
Цитохром с переносит электроны к комплексу IV.
Комплекс IV содержит два медьсодержащих центра и гемы, через которые электроны поступают к кислороду. При восстановлении кислорода в комплексе IV образуется сильный основной анион О2–, который связывает два протона и переходит в воду:
![]() . (5.15)
. (5.15)
Перенос
электронов является высокоэргическим
процессом. Согласно теории Митчелла,
перенос
электронов по электрон-транспортной
цепи стимулирует перенос протонов Н+
через гидрофобный барьер мембраны и
тем самым способствует образованию
градиентов по обе стороны мембраны:
разности концентраций ионов
![]() ,
разности электрических потенциалов
,
разности электрических потенциалов
![]() и разности электрохимических потенциалов
Δμ. Транспорт ионов Н+
через мембрану осуществляется против
электрического поля и является
эндоэргическим процессом, на который
расходуется энергия, генерируемая в
электронной цепи.
и разности электрохимических потенциалов
Δμ. Транспорт ионов Н+
через мембрану осуществляется против
электрического поля и является
эндоэргическим процессом, на который
расходуется энергия, генерируемая в
электронной цепи.
Поэтому процесс электронного транспорта энергетически сопряжен с потоком протонов (черные стрелки), создаваемым комплексами I, III и IV, и направленным из матрикса в межмембранное пространство.
Напомним, что электрохимический потенциал моля заряженных ионов в растворе равен умноженной на число Авогадро NA работе внешних сил по переносу одного иона из бесконечности в данную точку пространства. Он может быть представлен в виде (с. 260 (5.50))
![]() ,
(5.16)
,
(5.16)
где первый член суммы μ0 –
химический потенциал в стандартном
состоянии (не зависит от φ и n),
то есть в отсутствие электрического
поля и при концентрациях всех компонентов
равных единице (см. с. 259-260). Второй
член равен работе против сил электрического
поля,
![]() – электрический потенциал, Z
– зарядовое число (для иона водорода
Z=1), F=еNA
– число Фарадея (заряд моля электронов),
e – заряд электрона,
n – концентрация ионов
(в молях на литр
– электрический потенциал, Z
– зарядовое число (для иона водорода
Z=1), F=еNA
– число Фарадея (заряд моля электронов),
e – заряд электрона,
n – концентрация ионов
(в молях на литр
![]() ).
Третий член суммы (5.11) выражает зависимость
химического потенциала (энергии Гиббса
G) от энтропии S
(с. 260 (5.50)). С учетом того, что
).
Третий член суммы (5.11) выражает зависимость
химического потенциала (энергии Гиббса
G) от энтропии S
(с. 260 (5.50)). С учетом того, что
![]() ,
где
,
где
![]() – водородный показатель (с.257, (5.22)),
получаем
– водородный показатель (с.257, (5.22)),
получаем
![]() .
.
Тогда
электрохимический потенциал
![]() ,
приходящийся на один ион водорода, можно
записать в размерности электрического
потенциала:
,
приходящийся на один ион водорода, можно
записать в размерности электрического
потенциала:
![]() .
(5.17)
.
(5.17)
Величина
μ1
на внешней стороне мембраны обычно
примерно на 0,25 В выше, чем на внутренней
стороне, причем основной вклад в разность
электрохимических потенциалов
![]() дает электрическая составляющая
дает электрическая составляющая
![]() (0,15 ÷ 0,20) В.
(0,15 ÷ 0,20) В.
Градиент
электрохимического потенциала
![]() создает силы, действующие на протоны в
направлении уменьшения электрохимического
потенциала, то есть в направлении
внутренней стороны мембраны. Под
действием этих сил протоны попадают в
комплекс V
(рис.5-12), где осуществляется синтез АТФ.
Структура и работа комплекса V
– F1F2-АТФсинтазы
рассмотрены ниже, §5.9. Следует иметь в
виду, что молекулярные механизмы,
обеспечивающие при переносе электронов
трансмембранный перенос протонов Н+,
а также механизмы химического синтеза
АТФ с помощью АТФ-синтазы остаются во
многом неясными.
создает силы, действующие на протоны в
направлении уменьшения электрохимического
потенциала, то есть в направлении
внутренней стороны мембраны. Под
действием этих сил протоны попадают в
комплекс V
(рис.5-12), где осуществляется синтез АТФ.
Структура и работа комплекса V
– F1F2-АТФсинтазы
рассмотрены ниже, §5.9. Следует иметь в
виду, что молекулярные механизмы,
обеспечивающие при переносе электронов
трансмембранный перенос протонов Н+,
а также механизмы химического синтеза
АТФ с помощью АТФ-синтазы остаются во
многом неясными.
В
теории Митчелла предполагается, что
энергия
![]() ,
выделяющаяся при движении протонов
внутрь митохондрий по направлению
электрического поля и градиента рН,
используется АТФ-синтетазой V
для синтеза АТФ из АДФ и Ф (рис.5-12). Таким
образом, концепция сопряжения П.Митчелла
может быть представлена в виде схемы
,
выделяющаяся при движении протонов
внутрь митохондрий по направлению
электрического поля и градиента рН,
используется АТФ-синтетазой V
для синтеза АТФ из АДФ и Ф (рис.5-12). Таким
образом, концепция сопряжения П.Митчелла
может быть представлена в виде схемы
Перенос электронов (дыхание) |
|
фосфорилирование АДФ в АТФ |
(5.18) |
Сопряжение переноса электронов и фосфорилирования возможно только в неповрежденной замкнутой мембранной структуре.
Суммарная реакция кислородного этапа дыхания имеет вид
12Н2 + 6О2 |
→ |
12Н2О + 34АТФ |
(5.19) |
|
Дыхательная цепь |
|
Таким образом, чистый выход на одну молекулу глюкозы при полном ее окислении до воды и СО2 составляет 38 молекул АТФ, синтезированных из АДФ и неорганического фосфата. Две молекулы АТФ дает гликолиз (5.8), две цикл Кребса (5.9) и 34 – кислородное дыхание (5.14).
Интересно, что клетки головного мозга могут использовать для дыхания только глюкозу (углеводы).
