
- •V. Энергетический обмен клетки
- •§5.1. Метаболические реакции
- •Энергетически сопряженные реакции
- •§5.2. Модель молекулярного источника энергии
- •§5.3. Высокоэнергетические соединения – макроэрги. Атф
- •§5.4. Экзоэргические реакции. Гидролиз
- •§5.5. Окислительно-восстановительные реакции
- •5.5.1. Окислительные процессы в биологии
- •5.5.2. Ферментативное окисление
- •§5.6. Энергетическое сопряжение в реакциях фосфорилирования
- •§5.7. Законы биоэнергетики
- •§5.8. Клеточное дыхание
- •5.8.1. Общая схема
- •5.8.2. Две стадии клеточного дыхания
- •I. Первая стадия клеточного дыхания
- •II. Второй этап клеточного дыхания
- •§5.9. F1f0-атФсинтаза
- •5.9.1. Структура
- •5.9.2. Основные функции
- •5.9.3. Принцип действия
- •5.9.4. Синтез атф
- •5.9.5. Гидролиз атф
- •5.9.6. F1f0-atФсинтаза как биорегулятор клетки
- •§5.10. Межмолекулярный перенос энергии в биоструктурах
- •5.10.1. Химический и физический способы переноса энергии
- •5.10.2. Фотовозбуждение сложных молекул
- •5.10.3. Индуктивно-резонансный механизм миграции энергии
- •5.10.4. Модели индуктивно-резонансной миграции энергии
- •Механическая модель
- •Квантово-механическая модель
- •5.10.5. Обменно-резонансный механизм
- •5.10.6. Экситонный механизм
- •5.10.7. Некоторые замечания о механизмах переноса энергии фотовозбуждения
- •§5.11. Перенос электрона. Электронно-конформационное взаимодействие
- •5.11.1. Электронно-колебательное взаимодействие
- •5.11.2. Перенос электрона в окислительно-восстановительных реакциях
- •5.11.3. Проводимость белков
- •5.11.4. Полупроводниковая концепция транспорта
- •5.11.5. Химический механизм переноса заряда
- •5.11.6. Биологическое значение переноса заряда
- •§5.12. Фотосинтез
- •§5.13. Эволюция биоэнергетики
- •5.13.1. Ультрафиолетовый фотосинтез атф
- •5.13.2. О производстве энергии в экстремальных условиях
- •§5.14. Искусственные молекулярные устройства, моделирующие процессы переноса
5.5.2. Ферментативное окисление
Рис. 5–7.
НАД – никотинамидадениндинуклеотид
(кофермент ниацин)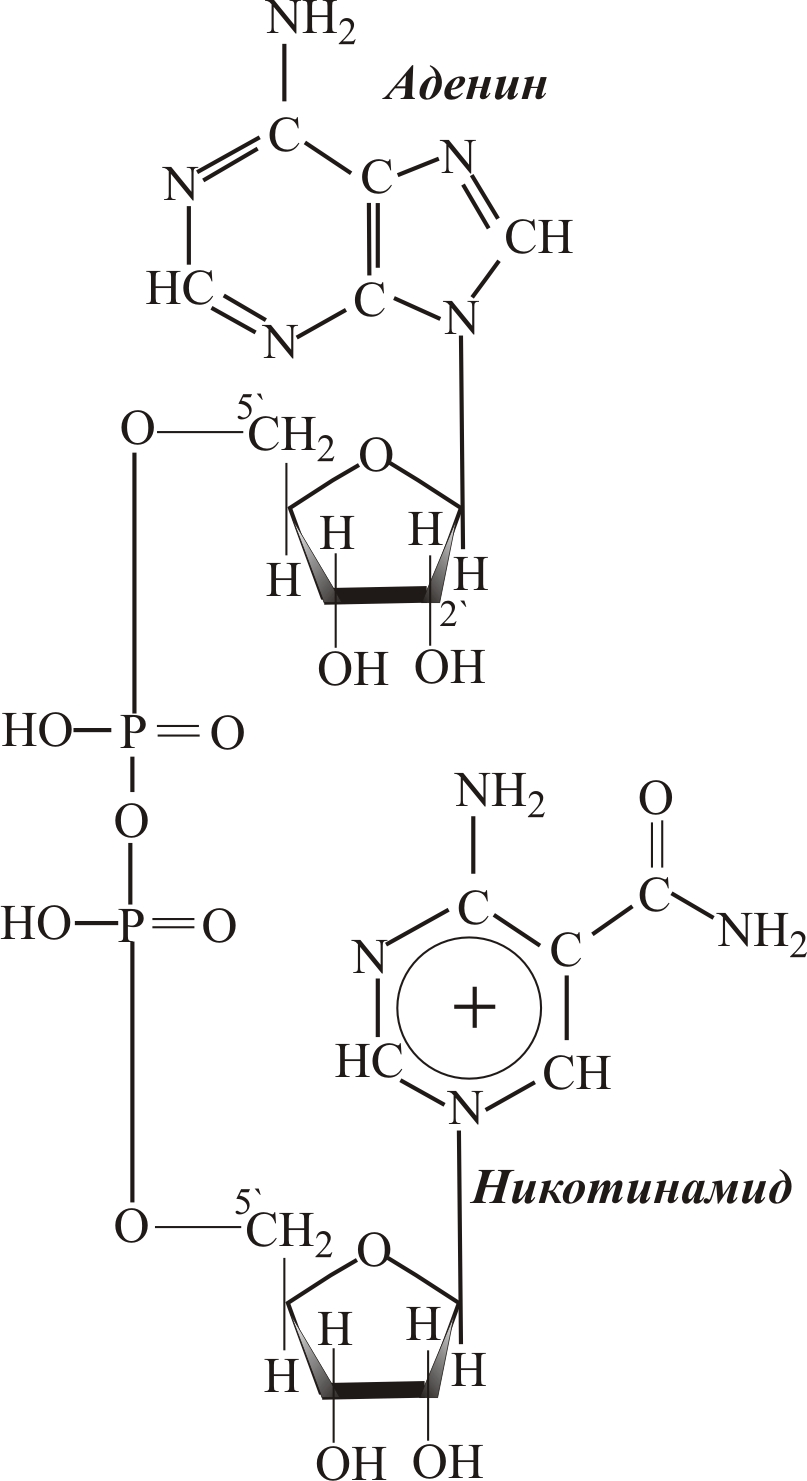
Коферменты, взаимодействующие с ферментами, служат промежуточными переносчиками различных групп атомов с одного субстрата на другой, в данном случае (при окислении) – для переноса восстановительных эквивалентов. В отличие от ферментов, которые обычно высокоспецифичны к своим субстратам, коферменты взаимодействуют со многими ферментами, обладающими раз-личной субстратной специфичностью. Растворимый кофермент присоединяется к ферменту во время реакции, химически изменяется, затем снова освобождается, а свою первоначальную форму приобретает во второй независимой реакции.
Рассмотрим действие растворимого кофермента ниацина НАД (никотинамидадениндинуклеотид, NAD) в окислительно-восстанови-тельных реакциях (рис. 5–7), который содержится в клетках в свободном состоянии. НАД относится к динуклеотидным коферментам. Он содержит два мононуклеотида: аденозин-5´-фосфат (верхняя часть формулы, рис. 5–7) и никотинамиднуклеотид (нижняя часть формулы). Два мононуклеотида связаны между собой ангидридной связью. При этом их фосфатные группы образуют 5´,5´-пирофосфатный мостик.
Никотинамид – это амид никотиновой кислоты (химическая формула на вставке рис. 5–8). Никотиновая кислота относится к группе витаминов.
НАД служит акцептором водорода (АсН2). Общая схема гидридного (Н–) переноса в окислительно-восстановительном процессе с образованием НАДН показана на рис. 5–8. В окислительно-восстановительных реакциях участвует только никотинамидное кольцо кофермента НАД (рис. 5–8, левая верхняя часть). В окисленной форме кольцо имеет ароматический характер, несет положительный заряд и обозначается НАД+. При окислении от восстановленного субстрата АН2 отделяются два атома водорода. На НАД+ переносится гидрид-ион Н–, содержащий два электрона и один протон.
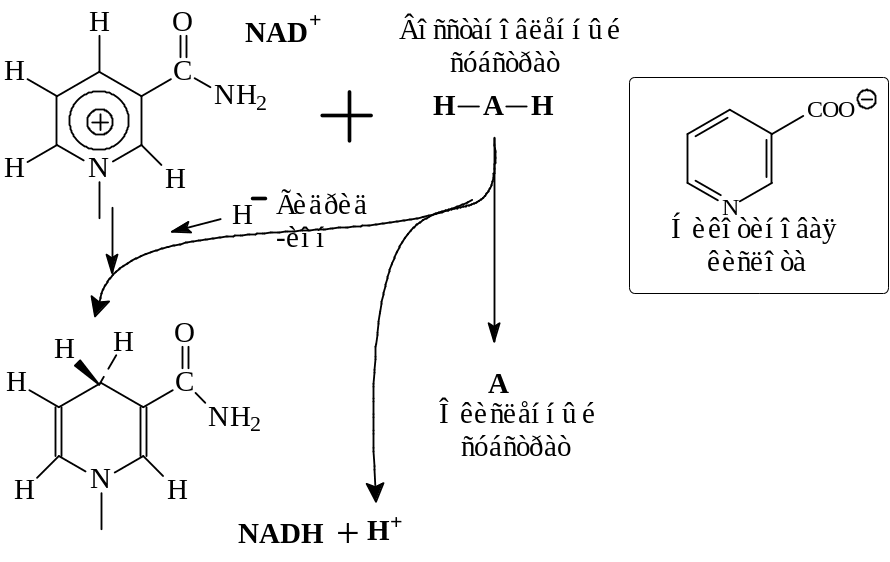
Рис. 5–8. Перенос гидрид-иона в окислительно-восстановительном процессе (5.7)
Акцептором гидрид-иона является атом углерода. При этом образуется алифатическая ациклическая СН2–группа, перестраиваются двойные связи кольца, и исчезает положительный заряд. Второй протон высвобождается в среду, и полная реакция восстановления кофермента НАД (с окислением субстрата АН2→А) записывается в виде:
НАД+ + АН2 → НАД∙Н + Н++А. (5.7)
§5.6. Энергетическое сопряжение в реакциях фосфорилирования
Фосфорилирование – это замещение любого атома (или группы атомов) на остаток фосфорной кислоты, которое, практически всегда, требует затрат энергии.
Если отщепление фосфата и высвобождение энергии АТФ (гидролиз) идет без сопряжения с эндоэргическим процессом, то это приводит лишь к выделению тепла. В клетке гидролиз идет с сопряжением, то есть одновременно с реакцией фосфорилирования биологических молекул, когда в ходе энергетически сопряженных реакций за счет отщепления фосфатной группы от АТФ или АДФ образуется промежуточный продукт. При этом биологическая молекула переходит в активное состояние и может вступать во вторую часть сопряженной реакции. Рассмотрим, например, реакцию образования глутамина из глутамата (рис. 5–9).
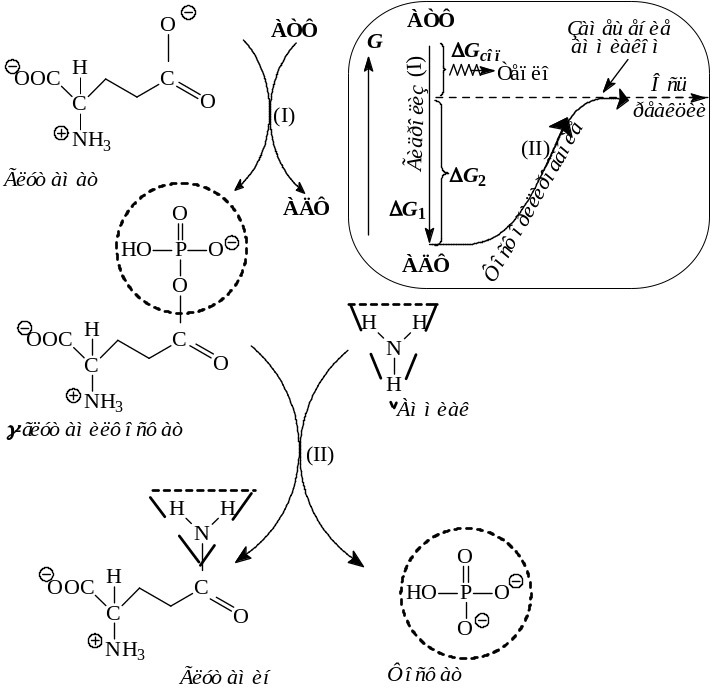
Рис. 5–9. Энергетическое сопряжение на примере реакции с участием глутамат-NH3-лигазы – глутаминсинтетазы (изомеразы, катализирующей превращения (образования связей С–N) в пределах одной молекулы)
В первой части сопряженной реакции (I) концевая фосфатная группа (в штриховом круге) переносится с АТФ на глутамат с образованием промежуточного продукта – смешанного ангидрида (γ-глутамилфосфата). На втором этапе сопряженной реакции (II) фосфатная группа промежуточного продукта вытесняется аммиаком NH3 (в штриховом треугольнике) с образованием глутамина и свободного фосфата. Изменения свободной энергии на обоих этапах сопряженного процесса (ΔG1, ΔG2) и суммарное изменение энергии (ΔGсоп) схематически изображены на вставке. Энергия ΔG1, выделяющаяся при реакции гидролиза АТФ→АДФ расходуется на фосфорилирование ΔG2 промежуточного продукта и частично ΔGсоп превращается в тепло. Поскольку
![]() ,
,
то в целом сопряженный процесс является экзоэргическим.
Обратный процесс (синтез АТФ из АДФ) – процесс рефосфорилирования (АДФ→АТФ или АМФ→АДФ→АТФ) требует затрат энергии и происходит в результате окислительных процессов. У человека скорость обмена АТФ составляет около 50 кг в сутки.
