
- •V. Энергетический обмен клетки
- •§5.1. Метаболические реакции
- •Энергетически сопряженные реакции
- •§5.2. Модель молекулярного источника энергии
- •§5.3. Высокоэнергетические соединения – макроэрги. Атф
- •§5.4. Экзоэргические реакции. Гидролиз
- •§5.5. Окислительно-восстановительные реакции
- •5.5.1. Окислительные процессы в биологии
- •5.5.2. Ферментативное окисление
- •§5.6. Энергетическое сопряжение в реакциях фосфорилирования
- •§5.7. Законы биоэнергетики
- •§5.8. Клеточное дыхание
- •5.8.1. Общая схема
- •5.8.2. Две стадии клеточного дыхания
- •I. Первая стадия клеточного дыхания
- •II. Второй этап клеточного дыхания
- •§5.9. F1f0-атФсинтаза
- •5.9.1. Структура
- •5.9.2. Основные функции
- •5.9.3. Принцип действия
- •5.9.4. Синтез атф
- •5.9.5. Гидролиз атф
- •5.9.6. F1f0-atФсинтаза как биорегулятор клетки
- •§5.10. Межмолекулярный перенос энергии в биоструктурах
- •5.10.1. Химический и физический способы переноса энергии
- •5.10.2. Фотовозбуждение сложных молекул
- •5.10.3. Индуктивно-резонансный механизм миграции энергии
- •5.10.4. Модели индуктивно-резонансной миграции энергии
- •Механическая модель
- •Квантово-механическая модель
- •5.10.5. Обменно-резонансный механизм
- •5.10.6. Экситонный механизм
- •5.10.7. Некоторые замечания о механизмах переноса энергии фотовозбуждения
- •§5.11. Перенос электрона. Электронно-конформационное взаимодействие
- •5.11.1. Электронно-колебательное взаимодействие
- •5.11.2. Перенос электрона в окислительно-восстановительных реакциях
- •5.11.3. Проводимость белков
- •5.11.4. Полупроводниковая концепция транспорта
- •5.11.5. Химический механизм переноса заряда
- •5.11.6. Биологическое значение переноса заряда
- •§5.12. Фотосинтез
- •§5.13. Эволюция биоэнергетики
- •5.13.1. Ультрафиолетовый фотосинтез атф
- •5.13.2. О производстве энергии в экстремальных условиях
- •§5.14. Искусственные молекулярные устройства, моделирующие процессы переноса
§5.11. Перенос электрона. Электронно-конформационное взаимодействие
В химии перенос электрона между молекулами рассматривается как окислительно-восстановительная реакция (см. с. 538). С точки зрения физики перенос электрона – это электронная проводимость. В отличие от химических окислительно-восстановительных реакций в растворах, происходящих при столкновениях молекул, имеющих избыток кинетической энергии, перенос электрона между донором и акцептором в белках происходит без непосредственного контакта этих групп (на расстояниях ~10Ả), хотя перенос может идти с большой скоростью ~1012 с–1, близкой к частоте атомных колебаний.
Основная особенность, отличающая транспорт электронов в белках от электропроводности, например, металлов, заключается в том, что перенос электронов в макромолекулах сопровождается изменением положений ядер атомов в белковых частях акцептора электрона. Это приводит к понижению электронного энергетического уровня у акцептора, что обеспечивает эффективность переноса электрона.
При изменении электронного (химического, зарядового) состояния функциональных групп макромолекулы, энергия реакции может сразу вся израсходоваться на возбуждение колебательных степеней свободы (см. ниже электронно-колебательное взаимодействие), а может часть энергии запасаться в напряжении конформационных степеней свободы. Скорость релаксации по конформационным степеням свободы значительно меньше скорости колебательной релаксации. Однако конформационное запасание энергии открывает возможность конформационных переходов и изменения реакционной способности функциональных групп.
Существует несколько способов переноса электрона. Основным из них является туннельный перенос.
5.11.1. Электронно-колебательное взаимодействие
Туннельный перенос электрона без непосредственного контакта донора и акцептора в биополимерах может производиться на большие расстояния порядка (10÷15)Å. Эффективный перенос электрона при туннелировании не требует тепловой активации и сохраняется при очень низких температурах, включая температуру кипения жидкого гелия (Т = 4,2 К). Интересно, что даже при комнатной температуре квантово-механическое туннелирование является основным механизмом переноса в белковой среде (с донора на акцептор).
Рассмотрим, как меняется колебательный
спектр ядер в донорно-акцепторном
комплексе
![]() при переносе электрона. Пусть в исходном
состоянии ядерные конфигурации у донора
и акцептора таковы, что электрон
локализован на доноре D–,
и комплекс записывается в виде
при переносе электрона. Пусть в исходном
состоянии ядерные конфигурации у донора
и акцептора таковы, что электрон
локализован на доноре D–,
и комплекс записывается в виде
![]() .
После переноса электрона комплекс
переходит в состояние
.
После переноса электрона комплекс
переходит в состояние
![]() .
При этом энергия комплекса и его
пространственная конфигурация изменяются.
Будем характеризовать равновесное
исходное состояние обобщенной
конформационной координатой RD,
определяющей некоторое эффективное
расстояние между ядрами в системе, а
равновесное конечное (после перехода
электрона) – RA.
Зависимость потенциальной энергии
комплекса от обобщенной координаты R
имеет вид потенциальной ямы, аналогичной
зависимости потенциальной энергии
взаимодействия двух взаимодействующих
частиц, как функции расстояния между
ними (т.1, с.156, рис. 3–2).
.
При этом энергия комплекса и его
пространственная конфигурация изменяются.
Будем характеризовать равновесное
исходное состояние обобщенной
конформационной координатой RD,
определяющей некоторое эффективное
расстояние между ядрами в системе, а
равновесное конечное (после перехода
электрона) – RA.
Зависимость потенциальной энергии
комплекса от обобщенной координаты R
имеет вид потенциальной ямы, аналогичной
зависимости потенциальной энергии
взаимодействия двух взаимодействующих
частиц, как функции расстояния между
ними (т.1, с.156, рис. 3–2).
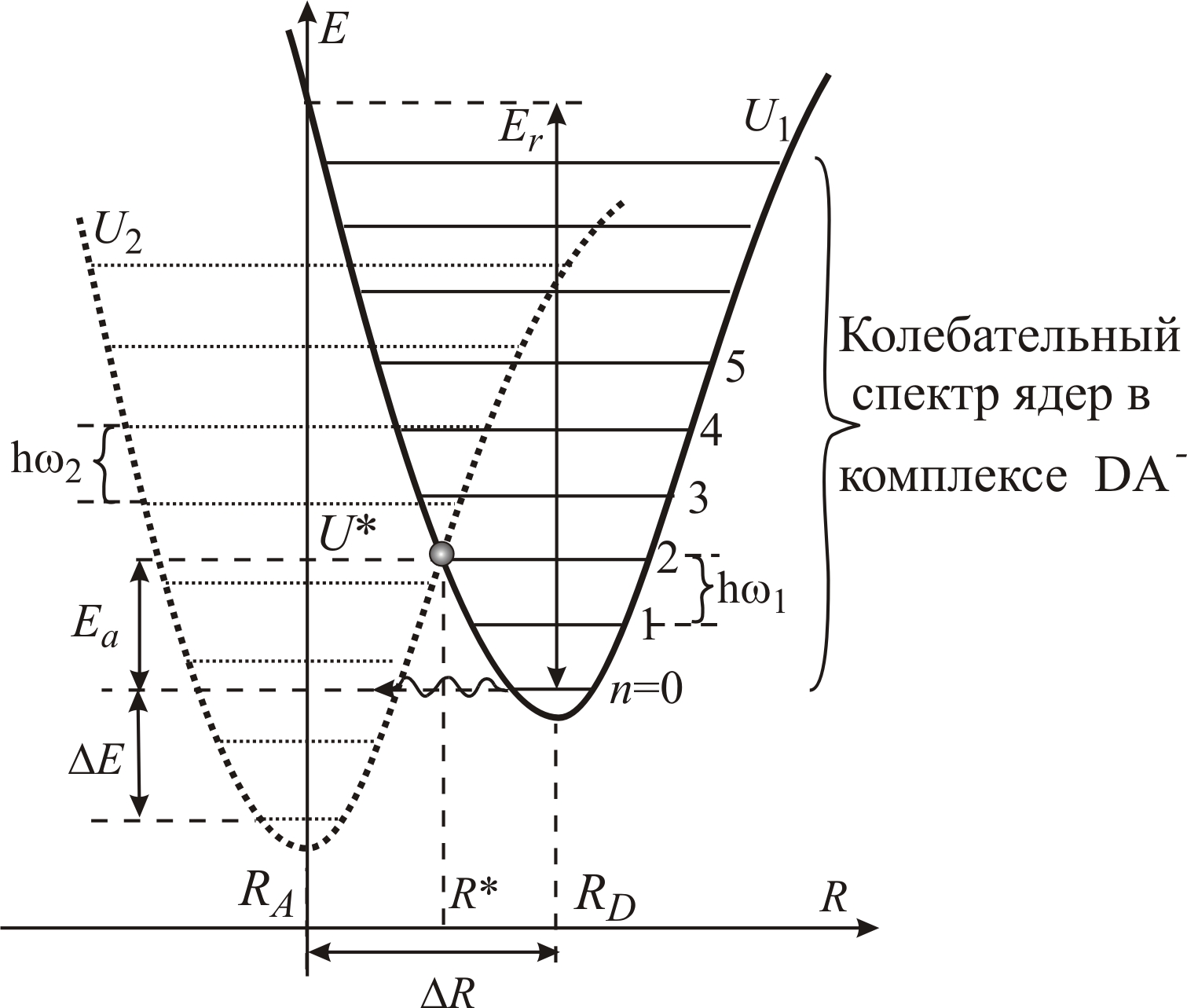
Рис. 5–26. Схема,
иллюстрирующая электронно-колебательное
взаимодействие при туннелировании
электрона (волнистая стрелка) от донора
к акцептору: U1
и U2
– потенциальные энергии, RD
и RA
– координаты равновесной конфигурации
комплексов D–A
и DA–,
соответственно; ΔR
– смещение положения равновесия ядер
при изменении электронного состояния
комплекса (при переходе электрона от
донора к акцептору); Ea
– энергия активации; ΔE
– тепловой
эффект реакции. Er
– энергия
реорганизации
системы, равная внешней работе, необходимой
для сдвига координат ядер
![]() при условии, что система остается на
начальном электронном терме Fe2+.
Волнистая линия –
туннелирование частиц комплекса из
одного состояния в другое
при условии, что система остается на
начальном электронном терме Fe2+.
Волнистая линия –
туннелирование частиц комплекса из
одного состояния в другое
Каждому состоянию и соответствуют минимумы потенциальной энергии U комплекса на графике U(R) (рис.5–26), расположенные при значениях R =RD и R = RА. Обе потенциальные ямы, соответствующие основным электронным состояниям и , заполнены дискретным рядом разрешенных энергетических уровней, представляющих собой квантованный колебательный спектр комплексов и . Основное равновесное состояние комплекса соответствует нижнему энергетическому уровню в потенциальной яме.
Вероятность квантово-механического перехода электрона между состояниями D–A и DA–, то есть частота обмена электроном между донором D и акцептором А, пропорциональна матричному элементу энергии взаимодействия:
![]() ,
,
где
![]() и
и
![]() – волновые функции электронов в
комплексах
и
,
U –потенциальная
энергия взаимодействия донора и
акцептора. Условие резонансного перехода
сохраняется, если разность энергий
начального
– волновые функции электронов в
комплексах
и
,
U –потенциальная
энергия взаимодействия донора и
акцептора. Условие резонансного перехода
сохраняется, если разность энергий
начального
![]() и конечного
и конечного
![]() состояний электрона удовлетворяет
условию:
состояний электрона удовлетворяет
условию:
![]() .
.
При резонансном переходе вероятность туннелирования слева направо и справа налево одинаковы, так что направленного переноса электрона из одного состояния в другое не происходит. Чтобы перенос был необратимым необходимо, чтобы за время пребывания электрона на акцепторе произошла диссипация энергии, что предотвратило бы обратный переход электрона по тому же пути к донору. Можно сказать, что закрепление электрона на акцепторе А происходит за счет потери части энергии электрона (~0,1 эВ).
Диссипация энергии означает уширение электронного энергетического уровня. Уширение уровня может произойти за счет дальнейшего туннелирования электрона в ближайшее окружение акцептора или за счет движения ядер. Последняя причина, как правило, играет основную роль.
Таким образом, необратимый переход
электрона (транспорт электрона)
осуществляется, благодаря перестройке
ядерной конфигурации комплекса. В
первый момент при переходе электрона
за время (10–12÷10–13) сек
ядра смещаются на расстояния меньше
0,1 Å в неравновесное конформационное
состояние. В результате изменения
заряда, состояние макромолекулы
оказывается конформационно-напряженным.
Малое смещение ядер индуцирует понижение
энергии системы и соответственно
понижение энергии электрона на акцепторе.
Избыток энергии электрона переходит в
тепло, увеличивая амплитуду колебаний
ядер (![]() ),
и способствует дальнейшей перестройке
пространственной конфигурации комплекса
в новое конформационно-равновесное
состояние. Переход сопровождается
смещением ядер по конформационной
координате из положения RD
в положение RA
(на расстояния порядка нескольких
ангстрем).
),
и способствует дальнейшей перестройке
пространственной конфигурации комплекса
в новое конформационно-равновесное
состояние. Переход сопровождается
смещением ядер по конформационной
координате из положения RD
в положение RA
(на расстояния порядка нескольких
ангстрем).
Вероятность (а, следовательно, и константа
скорости) перехода D–А→DA–
приближенно может быть представлена в
виде суммы двух слагаемых, связанных
с перестройкой ядерной
системы: вероятности
![]() квантово-механической подбарьерной
перестройки, не зависящей от температуры,
и вероятности
квантово-механической подбарьерной
перестройки, не зависящей от температуры,
и вероятности
![]() термоактивированного надбарьерного
перехода ядерной системы:
термоактивированного надбарьерного
перехода ядерной системы:
![]() . (5.47)
. (5.47)
Здесь
![]() – вероятность надбарьерной перестройки
ядер туннелирования при Т→,
Еa – энергия
активации, равная разности колебательной
энергии ядер E и высоты
энергетического барьера:
– вероятность надбарьерной перестройки
ядер туннелирования при Т→,
Еa – энергия
активации, равная разности колебательной
энергии ядер E и высоты
энергетического барьера:
![]() .
.
Термическая активация ядерной
системы должна быть такой, чтобы при
движении ядер достигалась точка R*.
В этом случае активационная составляющая
вероятности ядерной перестройки
определяется фактором Больцмана
![]() ,
то есть величиной энергии активации
,
то есть величиной энергии активации
![]() .
Если при движении ядер достигается
точка R* (Еа = 0)
пересечения электронно-колебательных
термов U1 и U2,
в которой потенциальные энергии
комплексов D–A
и DA– одинаковы,
то переход ядер происходит за время,
равное периоду колебаний. При таком
переходе не изменяется полная
электронно-колебательная энергия
системы, перестройка электронной
волновой функции: D–A
↔ DA– происходит
без дополнительной энергии. Еще раз
подчеркнем, что даже при комнатных
температурах термическая активация
требуется только для перестройки
ядерной системы, а электрон
переносится с донора на акцептор
туннельным путем.
.
Если при движении ядер достигается
точка R* (Еа = 0)
пересечения электронно-колебательных
термов U1 и U2,
в которой потенциальные энергии
комплексов D–A
и DA– одинаковы,
то переход ядер происходит за время,
равное периоду колебаний. При таком
переходе не изменяется полная
электронно-колебательная энергия
системы, перестройка электронной
волновой функции: D–A
↔ DA– происходит
без дополнительной энергии. Еще раз
подчеркнем, что даже при комнатных
температурах термическая активация
требуется только для перестройки
ядерной системы, а электрон
переносится с донора на акцептор
туннельным путем.
Туннельное смещение ядер, аналогичное электронному туннелированию, зависит от степени перекрывания ядерных волновых функций и характерно для низких температур. Чисто безактивационное туннелирование преобладает при Т < 100 К.
Вероятность w0 туннелирования частицы под барьером при одном столкновении с ним увеличивается при уменьшении высоты (U*–E) и ширины потенциального барьера l:
![]() (формула Гамова),
(формула Гамова),
где М – масса, Е энергия туннелирующей частицы.
При увеличении
![]() величина
величина
![]() и ширина
и ширина
![]() потенциального барьера растут. Для
частиц с массой
потенциального барьера растут. Для
частиц с массой
![]() при высоте и длине барьера, соответственно,
при высоте и длине барьера, соответственно,
![]() ,
l~1Å вероятность
туннелирования близка к единице.
,
l~1Å вероятность
туннелирования близка к единице.
При туннелировании энергия частицы сохраняется. Это значит, что частица преодолевает барьер по горизонтальной линии (волнистой стрелке на рис. 5–26), соответствующей значению энергии частицы в исходном состоянии. Общее время перестройки из состояния RD в равновесное состояние RA составляет (10–3÷10–6) с.
Рис. 5–27.
Зависимость логарифма скорости окисления
цитохрома с
в фотосинтезирующих бактериях от
обратной температуры, описывающая
высокотемпературную (надбарьерную) и
низкотемпературную (туннельную)
перестройку ядерной системы при
туннелировании электрона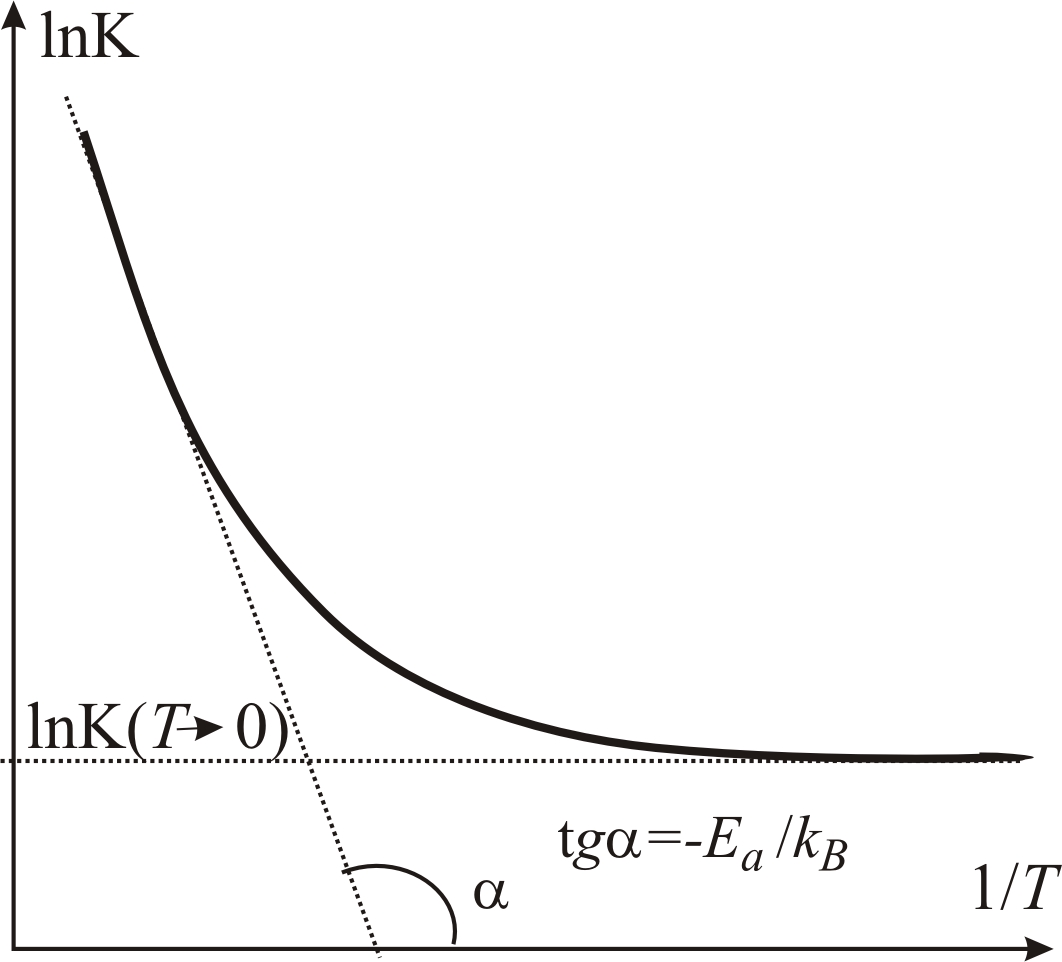
![]() ,
l≈1,2 нм). Для
порфириновых молекул при расстояниях
≤0,1 нм барьер практически отсутствует.
,
l≈1,2 нм). Для
порфириновых молекул при расстояниях
≤0,1 нм барьер практически отсутствует.
Таким образом, перестройка ядерной конфигурации комплекса и переход электрона – взаимосвязанные, сопряженные процессы. Сопряжение транспорта электронов в белках с перестройкой ядерной системы и диссипацией части электронной энергии называется электронно-конформационным взаимодействием. При изменении конформации белковые группы смещаются на расстояния (до нескольких десятков нм) заметно превышающие амплитуды тепловых колебаний атомов (~1 нм). Электронно-конформационное взаимодействие является основой функционирования макромолекул белков. Функциональная активность непосредственно связана с изменением электронного состояния белков, которое индуцирует определенные конформационные переходы в новые равновесные состояния, соответствующее минимумам конформационной энергии для измененных электронных состояний.
