
- •1.Биологическая роль кислорода в организме человека. Применение препаратов в медицине
- •2. Биологическая роль углерода в организме человека. Применение препаратов в медицине
- •3. Биологическая роль натрияи калия в организме человека. Применение препаратов в медицине.
- •4. Биологическая роль кальция в организме человека. Применение препаратов в медицине.
- •6. Биологическая роль железа в организме человека. Применение препаратов в медицине.
- •7. Биологическая роль цинка в организме человека. Применение препаратов в медицине.
- •Пиритион цинк активированный (Pyrithionezinc). Синонимы:Скин-кап
- •Цинка сульфат (Zincsulfate)
- •Поверхностное натяжение, поверхностная активность. Уравнение Гиббса. Пав, особенности строения, примеры, применение. Схема строения клеточной мембраны
- •Адсорбция на границе раздела твердое тело – газ. Изотерма адсорбции. Уравнение Ленгмюра.
- •Адсорбция на границе твердое тело – раствор. Правило Ребиндера. Изотерма адсорбции.Уравнение Ленгмюра.Гемосорбция, энтеросорбция.
- •Адсорбция электролитов. Правило Панета-Фаянса.
- •Хроматографические методы исследования. Классификация. Применение в медицине.
- •Общая характеристика вмс. Классификация. Применение в медицине. Коллоидная защита
- •Изоэлектрическая точка белка. Изменение свойств белков в изоэлектрическом состоянии
- •1.Координационная теория а. Вернера. Состав и классификация комплексных соединений
- •По заряду комплекса
- •По числу мест, занимаемых лигандами в координационной сфере
- •По природе лиганда
- •Свойства коллоидных растворов
- •Классификацияколлоидныхрастворовпоагрегатному состоянию дисперсной фазы и дисперсионной среды. Примеры.
- •Охарактеризовать методы получения коллоидных растворов.
- •Методы диспергирования
- •Методы конденсации
- •Методы очистки коллоидных растворов. Схема диализа.Гемодиализ.
- •Молекулярно-кинетические свойства коллоидных растворов.
- •Электрокинетические свойства коллоидных растворов. Применение электрофореза в медицине
- •Факторы устойчивости коллоидных растворов. Коагуляция. Порог коагуляции. Правило Шульце-Гарди.
Адсорбция на границе твердое тело – раствор. Правило Ребиндера. Изотерма адсорбции.Уравнение Ленгмюра.Гемосорбция, энтеросорбция.
Адсорбция на границе твердое тело - раствор сложна из-за физической неоднородности поверхности твердых тел (наличием дефектов поверхности - трещин, дислокаций, выходом разных граней кристалла на поверхность и так далее).
Кроме того, адсорбция из растворов на твердом адсорбенте осложняется наличием третьего компонента - растворителя, молекулы которого могут также адсорбироваться на поверхности адсорбента.
Чем хуже адсорбируется растворитель на адсорбент, тем лучше адсорбция растворенного вещества.
Так как для твердых адсорбентов отсутствуют достаточно точные методы непосредственного определения поверхностного натяжения, уравнения Гиббса для них не применимо. В большинстве случаев невозможно непосредственно определить удельную поверхность твердого адсорбента, поэтому используют в основном эмпирические зависимости.
Мерой адсорбционной энергии может служить теплота адсорбции. Известно, что при адсорбции уксусной кислоты на угле теплота адсорбции падает с увеличением степени заполнения по экспоненте, то есть поверхность угля при адсорбции на ней уксусной кислоты является экспоненциально неоднородной.
Модель идеального двухмерного раствора адсорбата и растворителя приводит к уравнению Лэнгмюра (1)
 или
=
или
=  илиГ
= Г
(2)
илиГ
= Г
(2)
Если поверхностный слой нельзя считать идеальным, то в уравнение (2) следует ввести коэффициенты активности адсорбата и растворителя. Если поверхность нельзя считать однородной, то для описания опытных данных по адсорбции из жидких растворов следует использовать уравнение изотермы Темкина
= I/fln(K0P ) (3)
или Фрейндлиха, заменив P на С:
= CP или = СP , (4)
где f- показатель неоднородности; К0 - адсорбционный коэффициент на наиболее сильно адсорбирующих центрах; С и - константы: 0 <<1.
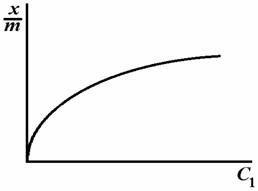
Рис.1. Вид изотермы адсорбции уксусной кислоты на угле
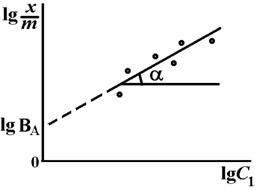
Рис.2. Логарифмическая изотерма адсорбции
Адсорбция зависит как от природы адсорбента, так и от природы адсорбируемого вещества вследствии ее избирательности.
Если в природе содержится не одно, а несколько веществ, то они будут адсорбироваться в соответствии с их адсорбционной способностью. На адсорбцию из растворов сильных электролитов влияют знак и количество свободных ионов в растворе.
Правило Ребиндера: чем больше разность полярности фаз, тем больше поверхностное натяжение на их границе раздела. Разность полярностей двух фаз (ΔП) - маленькая величина, она указывает на сближение свойств этих фаз, на усиление взаимодействия, на увеличение растворимости их друг в друге, а значит и на снижение поверхностного натяжения.
Энтеросорбция – это метод лечения различных заболеваний, основанный на способности энтеросорбентов связывать и выводить из организма различные экзогенные вещества, микроорганизмы и их токсины, эндогенные промежуточные и конечныe продукты обмена, способные накапливаться или проникать в полость ЖКТ в ходе течения различных заболеваний, а энтеросорбенты (ЭСБ) – препараты медицинского назначения, обладающие высокой сорбционной емкостью, не разрушающиеся в ЖКТ и способные связывать экзо– и эндогенные вещества, входящие в состав химуса и выделяющиеся в полость ЖКТ через его стенки, путем ад– и абсорбции, ионообмена или комплексообразования. Энтеросорбция является составной частью эфферентной терапии (от латинского efferens— выводить), то есть группы лечебных мероприятий, конечной целью которых является прекращение действия токсинов различного происхождения и их элиминация из организма. Кроме энтеросорбции, в эту группу входят гемодиализ, перитонеальный диализ, плазмаферез, гемосорбция и некоторые другие.
Гемосо́рбция (от греч. haema кровь + лат. sorbere поглощать) — метод лечения, направленный на удаление из крови различных токсических продуктов и регуляцию гемостаза путем контакта крови с сорбентом вне организма. Это разновидность процесса сорбции, при котором частицы поглощаемого вещества и поглотители вступают в химические взаимодействия. Гемосорбция — метод внепочечного очищения крови от токсических веществ путем адсорбции яда на поверхности сорбента. В качестве сорбентов используют активированный уголь (гемокарбоперфузия) или ионообменные смолы, предназначенные для очищения крови от определенных групп химических веществ.
Показанием к гемосорбции являются многие острые отравления лекарственными препаратами (барбитуратами, элениумом, ноксироном) и химическими ядами (хлорированными углеводородами, фосфорорганическими соединениями); острые поражения печени, протекающие с выраженной интоксикацией, особенно в стадии прекомы и комы. Кроме того, гемосорбция как дополнительный метод лечения может быть применена у больных системной красной волчанкой, холодовой крапивницей, псориазом, пищевой полиаллергией, бронхиальной астмой, семейной гиперлипидемией (холестеринемией)
