
- •6.070800 «Экология и охрана окружающей среды»
- •Введение
- •1 Производство синтетического аммиака
- •1.1 Методы производства азота и водорода
- •1.2 Промышленный катализ
- •1.3 Очистка природных газов от соединений серы
- •1.4 Конверсия метана
- •1.5 Конверсия оксида углерода (II)
- •1.6 Технологическая схема производства конвертированного газа
- •1.7 Очистка конвертированного газа от диоксида углерода
- •1.8 Тонкая очистка конвертированного газа от кислородсодержащих соединений
- •1.9 Технологическая схема очистки конвертированного газа от кислородсодержащих соединений
- •1.10 Синтез аммиака из смеси азота и водорода
- •1.11 Синтез метанола из оксида углерода и водорода
- •2 Производство неорганических кислот
- •2.1 Производство азотной кислоты
- •2.2 Производство серной кислоты
- •3 Производство кальцинированной соды
- •3.1 Принципиальная схема производства соды аммиачным
- •3.2 Аммонизация очищенного рассола
- •3.3 Карбонизация аммонизированного рассола
- •3.4 Кальцинация гидрокарбоната натрия
- •3.5 Регенерация аммиака в производстве кальцинированной соды
- •4 Производство минеральных удобрений
- •4.1 Производство карбамида
- •4.2 Производство нитрата аммония
- •4.3 Производство сульфата аммония
- •4.4 Производство нитрата калия
- •4.5 Производство суперфосфата
- •Рекомендованная литература
4.2 Производство нитрата аммония
Нитрат аммония – азотное удобрение, в котором доля азота составляет 35 %. Является безбалластным и одним из наиболее эффективных азотных удобрений. При этом стоимость перевозки содержащегося в нитрате аммония азота ниже, чем при перевозке других азотных удобрений (за исключением карбамида и жидкого аммиака).
Нитрат аммония NH4NO3, традиционно неправильно называемый аммиачной селитрой (правильнее называть аммонийной селитрой), при атмосферном давлении в интервале от – 50 °С до температуры плавления 169,6 °С существует в пяти кристаллических формах I—V, различающихся структурой, удельным объемом и другими свойствами кристаллов. На политермической диаграмме системы NH4NO3 – Н2О (рисунок 4.3) показаны температурные интервалы стабильности I—IV кристаллических форм.
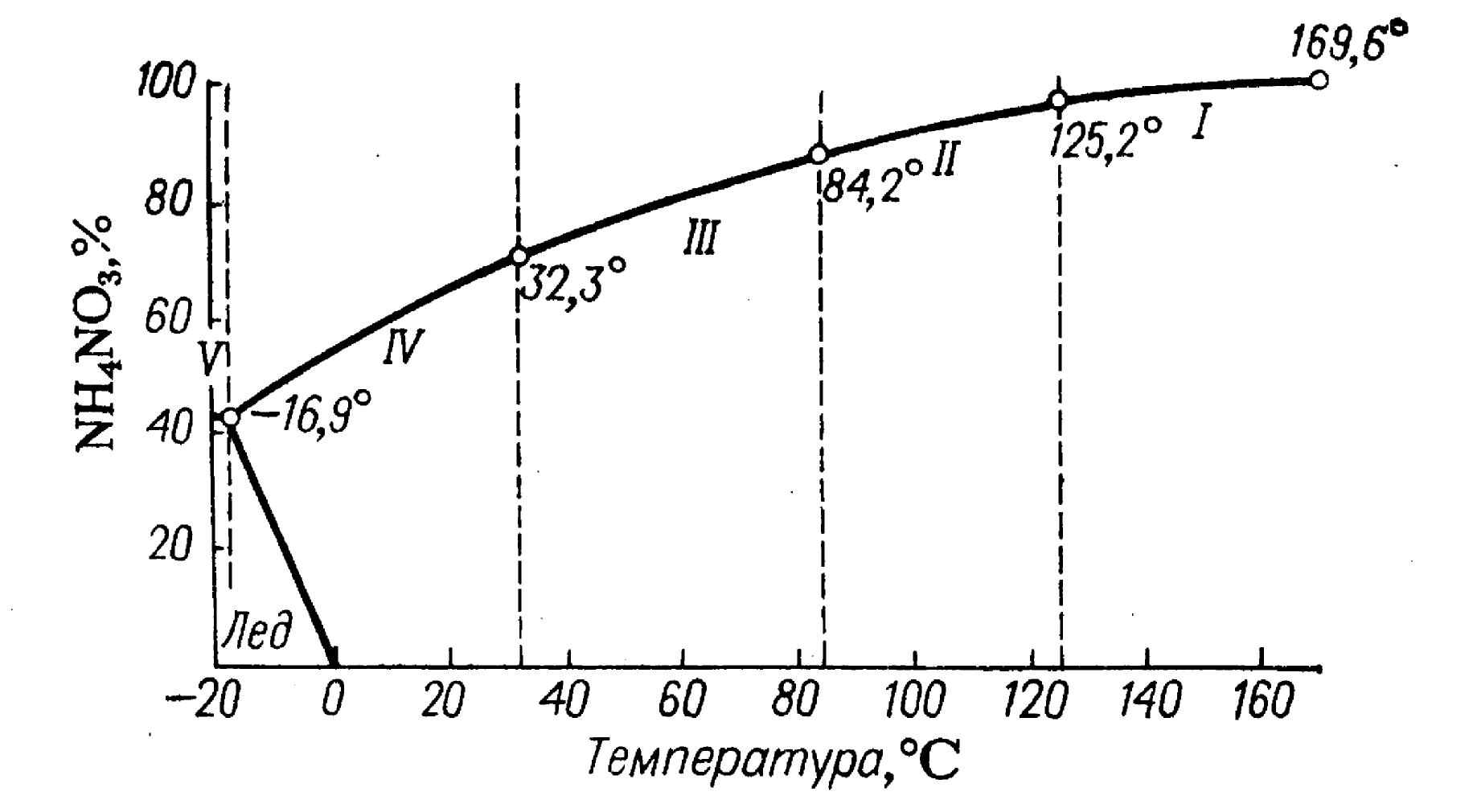
Формы кристаллов: I— кубическая; II — тетрагональная; III— ромбическая моноклинная; IV — ромбическая бипирамидальная; V — тетрагональная
Рисунок 4.3 – Растворимость нитрата аммония в воде
Модификация нитрата аммония V стабильна ниже -16,9 °С. Температурные границы и скорость взаимопревращений модификаций нитрата аммония зависят от влажности селитры и от наличия в ней других примесей.
4.2.1 Основные стадии производства нитрата аммония
Основными стадиями производства гранулированного нитрата аммония являются:
- нейтрализация азотной кислоты аммиаком;
- выпаривание раствора нитрата аммония;
- гранулирование плава нитрата аммония;
- охлаждение и обработка гранул;
- очистка газовых выбросов и сточных вод;
- упаковка готового продукта.
Получение нитрата аммония основано на нейтрализации аммиаком азотной кислоты:
NH3 (г) + HNO3 (ж) = NH4NO3 (тв) + 144,9 кДж.
При нейтрализации азотной кислоты, содержащей 47-60 % HNO3 (являющей сырьем в производстве), образуется раствор нитрата аммония, который для получения твердого продукта необходимо выпаривать. В процессе выпарки используется теплота нейтрализации. Количество теплоты, выделяющейся при реакции, зависит от концентрации исходной азотной кислоты: чем меньше концентрация кислоты, тем меньше выделяется теплоты. Как следует из данных рисунка 4.4, при соответствующей организации производственного процесса за счет теплоты реакции можно выпарить основную массу воды, вводимой с азотной кислотой, и получить высококонцентрированный раствор и даже плав нитрата аммония.
Отвод теплоты нейтрализации из реакционной зоны необходим не только с целью ее использования для выпарки раствора, но и потому, что чрезмерное повышение температуры раствора недопустимо. Это привело бы к разложению азотной кислоты и нитрата аммония, т. е. к потере азота. Последнее осложняет утилизацию теплоты реакции в самом нейтрализаторе. Поиск путей решения этой задачи способствовал разработке разных способов производства нитрата аммония, различающихся технологическим режимом и аппаратурным оформлением. В наиболее старых способах производства теплота реакции вообще не использовалась, а отводилась в водяном холодильнике, через который раствор нитрата аммония проходил, циркулируя между нейтрализатором и абсорбером аммиака. Затем появились способы, в которых раствор нитрата аммония из нейтрализатора подавали в вакуум-испарители, где он вскипал, оказываясь перегретым.
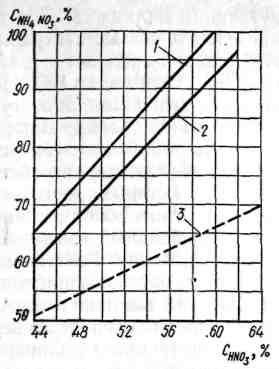
1- температура 343 К; 2- температура 293 К; 3- без использования теплоты реакции
Рисунок 4.4 – Зависимость концентрации растворов нитрата аммония от концентрации азотной кислоты
Этот же принцип положен в основу способов производства, в которых нейтрализация производится при температуре 180-200 °С под давлением 0,35-0,6 МПа, а самоиспарение раствора — при меньшем или при атмосферном давлении. При этом соковый пар используют для дальнейшей выпарки раствора от 75-80 до 95-99 % нитрата аммония в вакуум-аппаратах. Все эти способы исключают кипение раствора в зоне реакции. В распространенном способе производства нитрата аммония отвод теплоты реакции осуществляют в самом нейтрализаторе, где одновременно с нейтрализацией происходит кипение и упаривание раствора. Реакционный аппарат назван ИТН (использователь теплоты нейтрализации).
Нейтрализацию азотной кислоты аммиаком, разбавленным другими газами (например, при утилизации продувочных и танковых газов – отходов производства синтетического аммиака), осуществляют при температуре 90-100 °С в скрубберных или тарельчатых аппаратах колонного типа, орошаемых циркулирующим раствором нитрата аммония, в который вводится азотная кислота. Вытекающий горячий раствор поступает в вакуум-испаритель, где при остаточном давлении 13-20 кПа охлаждается до температуры кипения (70-75 °С), затем часть его возвращают на орошение колонного нейтрализатора, а другую часть направляют на выпаривание.
В современных высокопроизводительных агрегатах производства нитрата аммония под давлением, близким к атмосферному, в нейтрализаторе получают раствор с концентрацией нитрата аммония 92-93 % при температуре 428-438 К, который затем доупаривают. Преимуществом нейтрализации под атмосферным давлением является простота схемы, возможность использования газообразного аммиака и двукратного использования теплоты реакции нейтрализации.
Нитрат аммония - весьма гигроскопичен. Из-за большой растворимости в воде, значительного температурного коэффициента растворимости, гигроскопичности и полиморфных превращений нитрат аммония сильно слеживается, что затрудняет его применение. Используются разные средства борьбы со слеживаемостью:
Выпуск продукта в гранулированном виде с минимальным (не более 0,2 %) содержанием влаги и охлаждение гранул, чтобы образовалась форма IV, стабильная при температуре ниже 32,3 °С.
Применение кондиционирующих добавок, вводимых в раствор нитрата аммония до его кристаллизации, - нитрата магния, получаемого растворением магнезита в азотной кислоте; нитратов кальция и магния, получаемых разложением доломита; сульфата аммония или эквивалентного количества серной кислоты; смесей фосфорной и серной кислот (или их аммонийных солей); смесей ортоборной кислоты, диаммонийфосфата и сульфата аммония. Механизм действия перечисленных добавок может быть различным. Добавка нитрата магния способствует связыванию свободной воды плава вследствие образования кристаллогидрата Mg(NO3)2∙6H2O. Она замедляет переход модификации II в III и обеспечивает метастабильный переход II → IV, что увеличивает прочность гранул. Введение в плав нерастворимых веществ приводит к образованию гранул с мелкокристаллической структурой, повышенными плотностью и прочностью.
Обработка гранул поверхностно-активными веществами, способными образовывать гидрофобные пленки. Для этой цели применяют 40 % раствор диспергатора НФ, получаемого конденсацией сульфокислот нафталина с водным раствором формальдегида, а также жирные кислоты и их амины.
Опудривание гранул тонкоизмельченными малогигроскопичными веществами — диатомитом, талькомагнезитом, вермикулитом, мелом, каолином и т.д.
Эффективным средством для предотвращения увлажнения и уменьшения слеживаемости нитрата аммония является упаковка соли в плотную, хорошо герметизированную тару, например в полиэтиленовые или ламинированные бумажные мешки. Применение средств, повышающих качество продукта, позволяет осуществлять его бестарное хранение и транспортировку (насыпью).
4.2.2 Технологическая схема производства нитрата аммония
В промышленности широко применяется только метод получения аммонийной селитры из синтетического аммиака (или аммиаксодержащих газов) и разбавленной азотной кислоты. Метод получения селитры из аммиака коксового газа и разбавленной азотной кислоты перестали применять как экономически невыгодный метод. Кроме того, вырабатывающаяся по этому методу аммонийная селитра всегда содержала значительное количество примесей (пиридинов, фенолов, смол и др.).
На рисунке 4.5 представлена технологическая схема агрегата АС-72М по производству нитрата аммония.
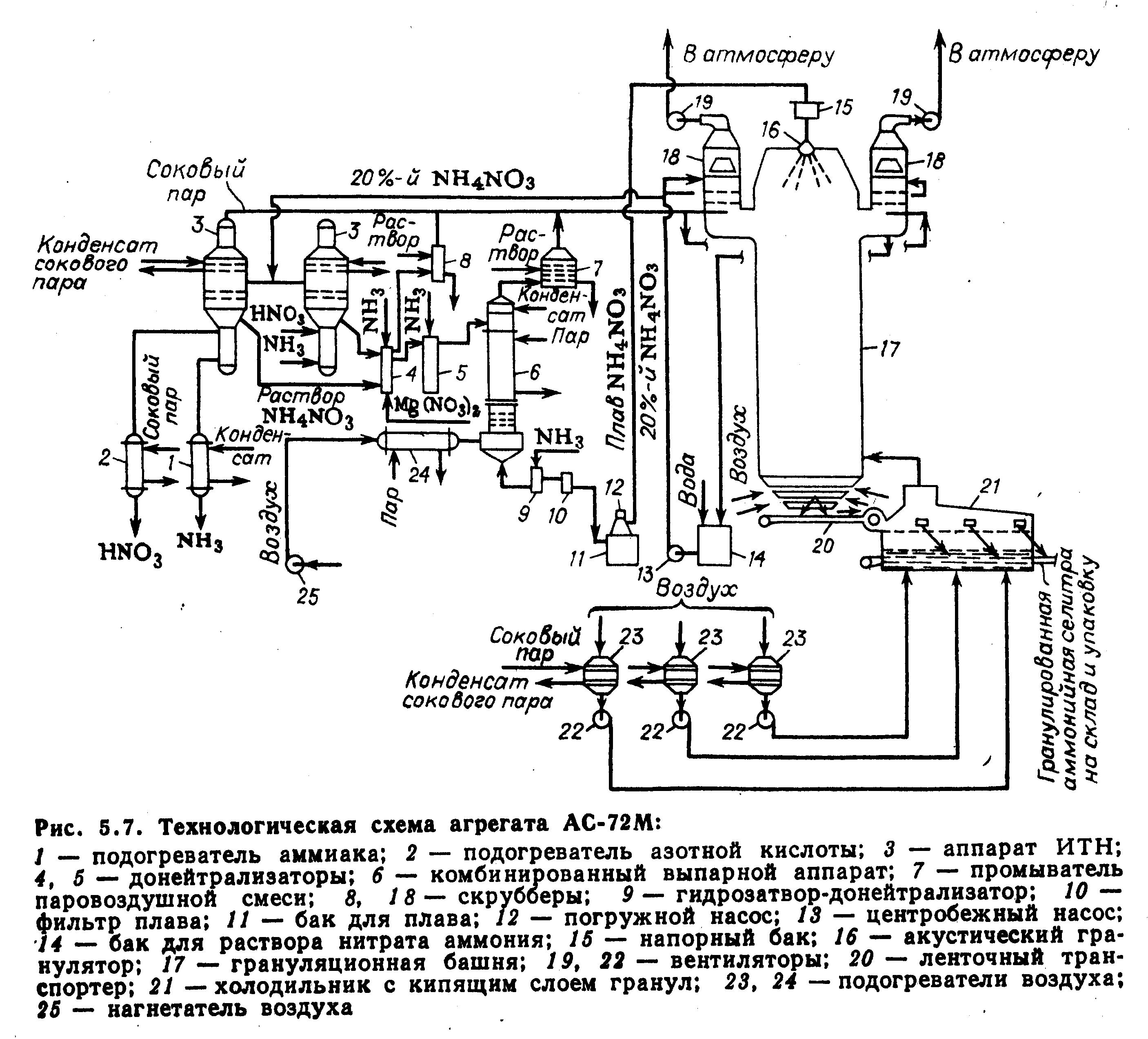
Рисунок 4.5 – Технологическая схема производства нитрата аммония
Газообразный аммиак, пройдя подогреватель 1, где нагревается до температуры 120-160 °С, и 58-60 %-я азотная кислота из подогревателя 2 с температурой 80-90 °С поступают в два параллельно работающих аппарата ИТН 3. В них поддерживается давление близкое к атмосферному. Для уменьшения потерь связанного азота с соковым паром (в виде NH3, HNO3, NH4NO3, NO2) реакцию ведут в слабокислой среде, так как при избытке азотной кислоты давление пара азотной кислоты над раствором нитрата аммония меньше, чем давление аммиака при его избытке в растворе. Концентрация азотной кислоты в уходящем из аппарата растворе (2-5 г/л) регулируется автоматически. Температура этого раствора 150-170 °С, а содержание в нем нитрата аммония 89-92 %.
Раствор нитрата аммония, вытекающий из аппаратов ИТН, нейтрализуется аммиаком в двух донейтрализаторах - основном 4 и контрольном 5. Сюда же вводят кондиционирующую добавку – 30- 40 %-й раствор нитрата магния, приготовленный растворением каустического магнезита МgО в азотной кислоте. С концентрацией 0,1-0,5 г/л избыточного аммиака раствор нитрата аммония поступает на доупаривание в комбинированный выпарной аппарат 6. Отсюда плав через гидрозатвор-донейтрализатор 9 и фильтр 10 направляется в приемный бак 11, а из него с помощью погружного насоса 12 по трубопроводу с антидетонационной насадкой перекачивается в напорный бак 15, находящийся над грануляционной башней 17.
Из напорного бака плав подается в грануляционную башню через три виброакустических гранулятора 16.
Корпус грануляционной башни высотой 63,5 м снаружи укреплен растяжками из углеродистой стали и подвешен на опорах. Через отверстия в нижней части в башню засасывается наружный воздух и воздух из аппарата кипящего слоя 21, в котором гранулы досушиваются и доохлаждаются. Высота падения капель плава в башне не превышает 50 м. Падая в потоке воздуха, они затвердевают, превращаются в гранулы. Температура плава, подаваемого на гранулирование, на 5-7 °С превышает температуру его кристаллизации. Чем больше в плаве остаточной воды, тем ниже температура отвердевания гранул, наступающего после кристаллизации ~ 90 % вещества. Плав селитры с влажностью 0,2 % начинает кристаллизоваться при температуре ~167 °С, а полностью затвердевает при температуре ~ 140 °С.
Из нижней конусной части башни гранулы поступают на ленточный транспортер 20, подающий их в трехсекционный аппарат 21 для доохлаждения в кипящем слое с автономной подачей воздуха в каждую секцию. Это позволяет регулировать процесс охлаждения в зависимости от температуры поступающих гранул и воздуха. Температура гранул после холодильника летом 40-50 °С, зимой - 20-30 °С. При гранулировании и последующем охлаждении в потоках воздуха гранулы подсушиваются, их влажность на 0,1-0,15 % меньше влажности поступающего в башню плава. Готовый продукт содержит более 99,8 % нитрата аммония. Если относительная влажность атмосферного воздуха больше 60 %, его пропускают через подогреватели 23 (также, как и воздух, подаваемый в доупарочный аппарат 6).
Аппараты кипящего слоя можно применять не только для охлаждения гранул, но и для гранулирования раствора. При подаче в кипящий слой 80-85 %-го раствора нитрата аммония вода выпаривается в потоке горячего воздуха.
Из верхней части башни воздух поступает в шесть скрубберов 18, где отмывается от пыли нитрата аммония и аммиака циркулирующим 20 %-м раствором нитрата аммония и вентиляторами 19 выбрасывается в атмосферу. Через эти же скрубберы проходят и газы из выпарного аппарата после промывателя 7 и донейтрализатора после скруббера 8.
