
- •6.070800 «Экология и охрана окружающей среды»
- •Введение
- •1 Производство синтетического аммиака
- •1.1 Методы производства азота и водорода
- •1.2 Промышленный катализ
- •1.3 Очистка природных газов от соединений серы
- •1.4 Конверсия метана
- •1.5 Конверсия оксида углерода (II)
- •1.6 Технологическая схема производства конвертированного газа
- •1.7 Очистка конвертированного газа от диоксида углерода
- •1.8 Тонкая очистка конвертированного газа от кислородсодержащих соединений
- •1.9 Технологическая схема очистки конвертированного газа от кислородсодержащих соединений
- •1.10 Синтез аммиака из смеси азота и водорода
- •1.11 Синтез метанола из оксида углерода и водорода
- •2 Производство неорганических кислот
- •2.1 Производство азотной кислоты
- •2.2 Производство серной кислоты
- •3 Производство кальцинированной соды
- •3.1 Принципиальная схема производства соды аммиачным
- •3.2 Аммонизация очищенного рассола
- •3.3 Карбонизация аммонизированного рассола
- •3.4 Кальцинация гидрокарбоната натрия
- •3.5 Регенерация аммиака в производстве кальцинированной соды
- •4 Производство минеральных удобрений
- •4.1 Производство карбамида
- •4.2 Производство нитрата аммония
- •4.3 Производство сульфата аммония
- •4.4 Производство нитрата калия
- •4.5 Производство суперфосфата
- •Рекомендованная литература
4.1 Производство карбамида
Карбамид (полный амид угольной кислоты), или мочевина, СО(NH2)2 является концентрированным безбалластным удобреним. В чистом карбамиде содержится 46,6 % азота – больше, чем в других азотных удобрениях (кроме чистого аммиака). Азот карбамида легко усваивается растениями.
В качестве химического соединения карбамид стал известен после открытия его в 1773 г. И. Руэллем. Синтез карбамида из цианата аммония осуществил в 1828 г. Ф. Велер по реакции:
![]()
Промышленность выпускает карбамид в кристаллическом (для технических целей) и гранулированном (для сельского хозяйства) видах.
Современный способ получения карбамида основан на реакции А.Б. Базарова, открытой им в 1868 году. Уравнение реакции следующее:
2NH3 + CO2 = CO(NH2 )2 + H2O + 130,1 кДж.
4.1.1 Физико-химические основы процесса
Синтез карбамида осуществляется в две стадии. Вначале из диоксида углерода и аммиака образуется карбамат аммония:
CO2 + 2NH3 = NH4 O – CO – NH2 + 159 кДж.
Затем происходит его дегидратация:
NH4 O – CO – NH2 ↔ CO(NH2 )2 + H2O – 28,1 кДж.
Степень превращения диоксида углерода в карбамид зависит от температуры, давления, соотношения компонентов реакции, продолжительности процесса и некоторых других факторов.
При одновременном протекании обеих стадий синтеза карбамида теплота образования карбамата аммония компенсирует эндотермический эффект реакции его дегидратации и обеспечивает необходимый разогрев смеси до оптимальной температуры синтеза карбамида.
Реакция образования карбамата аммония протекает быстро и практически до конца. Реакция же дегидратации карбамата аммония, определяющая выход карбамида, обратима. В соответствии с принципом Ле Шателье, повышение температуры благоприятствует протеканию реакции дегидратации карбамата аммония, однако при этом возможно его разложение.
Превращение карбамата аммония в карбамид происходит в жидкой фазе. В соответствии с этим процесс синтеза необходимо вести при высоких значениях температуры и давления. Высокое давление также подавляет процесс разложения карбамата аммония на аммиак и диоксид углерода.
На диаграмме состояния трехфазной системы NH4CO2NH2 - CO(NH2)2 – (CO2 + NH3) (см. рисунок 4.1) имеется область температур и давлений, при которых карбамид СО(NH2)2 находится в жидкой фазе. В этой области может реально протекать реакция образования карбамида. Минимальные параметры проведения реакции соответствуют температуре плавления карбамата аммония 425 К и давлению 8,33 МПа. С повышением давления расширяется область температур, при которых существует жидкая фаза.
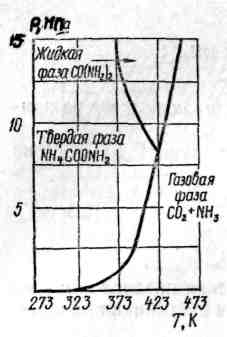
Рисунок 4.1 - Диаграмма состояния трехфазной системы NH4CO2NH2 - CO(NH2)2 – (CO2 + NH3)
В интервалах приведенных давлений и температур (таблица 4.3) большое влияние на выход карбамида оказывает соотношение компонентов реакции.
Таблица 4.3 - Выход карбамида по диоксиду углерода в зависимости от температуры, давления и мольного соотношения компонентов реакции
Давле-ние, МПа |
Состав плава, % масс. |
Соотношение NH3:CO2 |
Равновесный выход CO(NH2 )2 , % |
|||
NH3 |
СO2 |
CO(NH2 )2 |
H2O |
|||
При температуре 460 К |
||||||
18,5 |
24 |
19 |
41 |
16 |
2,5 |
60,5 |
20,9 |
33 |
14 |
40 |
13 |
2,7 |
63,7 |
25,8 |
41 |
10 |
36 |
13 |
4,3 |
73,1 |
31,1 |
47 |
8 |
32 |
13 |
5,3 |
74,3 |
Как следует из данных таблицы 4.3, при указанных выше давлениях и температурах наибольшее значение для выхода карбамида имеет введение избытка аммиака, при этом целесообразно применять мольное соотношение NH3:CO2 равным 4-4,5. Избыточный аммиак уменьшает вредное действие выделившейся в процессе воды, связывает ее и тем самым равновесие реакции превращения карбамата аммония в карбамид сдвигается в сторону последнего. По этой же причине замедляется разложение карбамата аммония с образованием побочных продуктов. При наличии избытка аммиака снижается и коррозионное действие плава.
Степень конверсии карбамата аммония при давлении 20 МПа и температуре 430 К описывается следующими данными:
Избыток аммиака, % |
0 |
45,2 |
76,5 |
96 |
173 |
280 |
Степень конверсии, % |
43,5 |
58,5 |
67,0 |
70,6 |
80,2 |
81,2 |
Реакция образования карбамата аммония при обычной температуре протекает медленно. С повышением температуры и давления скорость этой реакции возрастает. Скорость реакции дегидратации карбамата аммония также увеличивается с повышением температуры.
Выделяющаяся в процессе синтеза карбамида вода понижает температуру плавления карбамата аммония и служит автокатализатором, значительно увеличивая скорость реакции. Образующаяся вначале процесса вода увеличивает степень конверсии так как способствует появлению жидкой фазы. Однако, по мере накопления в плаве нескольких процентов воды она начинает замедлять скорость реакции в сторону образования СО (NH2)2. Для увеличения скорости реакции целесообразно удалять избыточную воду, однако в условиях синтеза карбамида это трудно осуществимо.
Понижению температуры плавления системы «карбамид - карбамат аммония» способствует также образование гидрокарбоната и карбоната аммония.
Для предотвращения накопления инертных газов (азот, водород, оксид углерода (II)) и для полного использования аммиака и диоксида углерода в производстве карбамида используют в основном циклические схемы. В связи с этим большое значение приобретает очистка диоксида углерода и аммиака. Для синтеза карбамида диоксид углерода используют в основном в виде экспанзерного газа - отхода очистки азотоводородной смеси, получаемой конверсией метана и оксида углерода (II). Предложено несколько методов удаления сероводорода, водорода и оксида углерода (II) из экспанзерного газа.
Исходя из технико-экономических предпосылок, синтез карбамида ведут при температурах 460-473 К, давлении 18-21 МПа и соотношении NH3:CO2 = 4-4,5. При этих условиях и времени пребывания реагентов в колонне синтеза в пределах 50-60 минут выход карбамида достигает 55-65 %.
4.1.2 Технологическая схема установки синтеза карбамида
Современные установки производства карбамида работают по замкнутым схемам, по которым продукты дистилляции полностью возвращаются на синтез карбамида. Рециркуляцию газов дистилляции можно осуществлять разными способами:
- с газовым рециклом — продукты дистилляции возвращаются в газообразной форме;
- с частичным или полным жидкостным рециклом — в цикл возвращают жидкий аммиак или растворы (суспензии) углеаммонийных солей.
Непосредственный возврат в цикл синтеза газовой смеси аммиака и диоксида углерода, получаемой при дистилляции, требует ее сжатия до давления синтеза при высокой температуре во избежание образования твердого карбамата аммония. Работа компрессоров в этих условиях затруднена, они подвергаются сильной коррозии. Поэтому в способах с газовым рециклом требуется предварительно разделять газы дистилляции, обрабатывая их селективными абсорбентами для извлечения аммиака и диоксида углерода. Например, промывая газы в абсорбере раствором нитрата карбамида, из них можно извлечь аммиак; оставшийся в газовой фазе диоксид углерода может быть использован вновь. При регенерации поглотительного раствора в десорбере выделяется аммиак, который возвращают в цикл синтеза.
Процессы с жидкостным рециклом получили наибольшее распространение. В них газы дистилляции поглощают водой и образовавшийся концентрированный раствор углеаммонийных солей возвращают на синтез карбамида. Наиболее совершенными являются процессы, в которых дистилляцию плава, т. е. разложение карбамата аммония и отгонку аммиака, осуществляют в токе аммиака или диоксида углерода при давлении синтеза.
На принципиальной схеме (рисунок 4.2) изображена система с полным жидкостным рециклом.
Аммиак, поступающий из хранилища 1, сжимается компрессором 2 и через холодильник 3 направляется в реактор 5. Туда же подается диоксид углерода, сжатый компрессором 4. Выходящую из реактора 5 смесь дросселируют до давления 2-2,5 МПа и направляют в сепаратор-испаритель 6, а затем в первый аппарат для разложения карбамата - дистиллятор 7, соединенный с сепаратором 8. Отходящие газы из аппаратов 6 и 8 поступают в межтрубную часть второго аппарата для разложения карбамата 10, где они абсорбируются раствором карбамата аммония, выходящим из абсорбера 12.
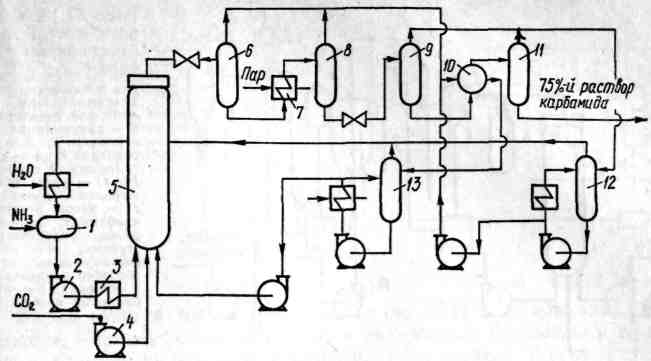
Рисунок 4.2 – Схема производства карбамида с полным жидкостным рециклом
Выделяющаяся при этом теплота используется для дальнейшего разложения смеси, поступающей в трубную часть аппарата 10 через сепаратор-испаритель 9, работающий под давлением 0,1 МПа. В нем происходит дальнейшее отделение газов от раствора, поступающего из аппарата 8. Остаточные количества аммиака и диоксида углерода отделяют от раствора карбамида в сепараторе 11. Газовые потоки из аппаратов 9 и 11 направляют в абсорбер 12. Раствор из межтрубного пространства аппарата 10 под давлением 2 МПа подают в абсорбер 13, в котором остатки диоксида углерода переходят в раствор. Полученный раствор карбамата аммония рециркулируется в реактор. Аммиак из верхней части абсорбера 13 сжижают и возвращают в хранилище. Оптимальный технологический режим: давление 22 МПа, температура 473 К, соотношение NH3:СО2:Н2О = 5:1:0,8.
Раствор карбамида, получаемый после дистилляции плава, далее подвергается выпариванию с последующей кристаллизацией (или гранулированием) продукта и его сушкой. Отогнанный при дистилляции плава непрореагировавший аммиак возвращается в цикл синтеза карбамида или перерабатывается в аммиачную селитру. Количество получаемой при этом селитры изменяется в зависимости от избытка аммиака и способа дистилляции плава карбамида.
