
- •6.070800 «Экология и охрана окружающей среды»
- •Введение
- •1 Производство синтетического аммиака
- •1.1 Методы производства азота и водорода
- •1.2 Промышленный катализ
- •1.3 Очистка природных газов от соединений серы
- •1.4 Конверсия метана
- •1.5 Конверсия оксида углерода (II)
- •1.6 Технологическая схема производства конвертированного газа
- •1.7 Очистка конвертированного газа от диоксида углерода
- •1.8 Тонкая очистка конвертированного газа от кислородсодержащих соединений
- •1.9 Технологическая схема очистки конвертированного газа от кислородсодержащих соединений
- •1.10 Синтез аммиака из смеси азота и водорода
- •1.11 Синтез метанола из оксида углерода и водорода
- •2 Производство неорганических кислот
- •2.1 Производство азотной кислоты
- •2.2 Производство серной кислоты
- •3 Производство кальцинированной соды
- •3.1 Принципиальная схема производства соды аммиачным
- •3.2 Аммонизация очищенного рассола
- •3.3 Карбонизация аммонизированного рассола
- •3.4 Кальцинация гидрокарбоната натрия
- •3.5 Регенерация аммиака в производстве кальцинированной соды
- •4 Производство минеральных удобрений
- •4.1 Производство карбамида
- •4.2 Производство нитрата аммония
- •4.3 Производство сульфата аммония
- •4.4 Производство нитрата калия
- •4.5 Производство суперфосфата
- •Рекомендованная литература
3.5 Регенерация аммиака в производстве кальцинированной соды
3.5.1 Физико-химические основы процесса
Регенерация аммиака из фильтровой и других жидкостей содового производства осуществляется в отделении дистилляции. Обычно часть растворенного аммиака связана с диоксидом углерода, поэтому при разложении карбонатов аммония вместе с аммиаком отгоняется и возвращается в производство диоксид углерода.
Гидрокарбонаты аммония гидролизуются в растворе. При этом мало растворимый диоксид углерода выделяется в газовую фазу, а хорошо растворимый аммиак остается в растворе, сдвигая равновесие в сторону образования средней соли:
NH4НСO3 + Н2O → NH4OН + Н2O + СО2
NН4НСO3 + NH4ОН → (NH4)2СO3 + Н2О (3.10)
2NН4НСO3(р) → (NН4)2СO3(р) + СO2 (г) + Н2O (ж) - 30,4 кДж.
Таким образом, на 1 моль образующегося диоксида углерода затрачивается 30,4 кДж тепла. Диоксид углерода начинает выделяться в газовую фазу уже при тмпературах 35-40 °С. При аналогичном разложении более стабильной средней соли по реакции:
(NH4)2СO3 (р) → 2NН3(р) + СO2 (г) + Н2O (ж) - 100,8 кДж (3.11)
затрачивается 100,8 кДж на образование 1 моль диоксида углерода, выделение которого в газовую фазу наблюдается только при температурах 65-70 °С.
Опыт показывает, что при нагревании фильтровой жидкости указанного выше состава в газовую фазу выделяется (н.д.):
Температура, °С |
50 |
60 |
70 |
80 |
Диоксид углерода |
5,7 |
10,8 |
16,1 |
23,0 |
Аммиак |
0,1 |
0,2 |
0,8 |
2,1 |
Следовательно, при температуре 80 °С выделяется 62 % диоксида углерода и только ~9 % аммиака от содержащихся в жидкости. Вследствие высокой растворимости аммиака его нельзя удалить из жидкости путем нагревания даже до температуры 100 °С.
Для снижения растворимости аммиака и удаления его в газовую фазу необходимо снизить давление аммиака в газовой фазе. Для этого на содовом заводе используется водяной пар, который, барботируя через жидкость, нагревает ее, и, выделяясь в газовую фазу, разбавляет газ, снижает парциальное давление аммиака, и согласно закону Генри способствует его удалению из жидкости. Переход аммиака из водного раствора в газовую фазу требует затраты 34,8 кДж/моль.
Присутствие диоксида углерода в жидкости снижает равновесное давление аммиака над жидкостью и тем самым затрудняет его отгонку. По этой же причине ухудшается отгонка диоксида углерода в присутствии в растворе аммиака.
Таким образом, скорость и полнота отгонки аммиака из жидкости зависит от температуры, давления аммиака в газовой фазе и от состава жидкости.
Для регенерации аммиака из хлорида аммония необходимо действие более сильной щелочи, которая могла бы вытеснить ион аммония из хлорида. В содовом производстве для этой цели используется известковое молоко:
2NH4С1 (р) + Са (ОН)2 (тв.) → СаС12 (р) + 2NН3 (р) + 2Н2O(ж) + 24,4 кДж.
Скорость этой реакции определяется скоростью растворения гидроксида кальция Са(ОН)2, т. е. зависит от степени дисперсности известкового молока. Высокая степень дисперсности имеет особое значение в конце разложения хлорида аммония, когда концентрация последнего и избыток гидроксида кальция малы, а концентрация хлорида кальция или ионов кальция, затрудняющих растворение гидроксида кальция, велика. Аммиак, образующийся при разложении хлорида аммония, отгоняется путем дистилляции при нагревании жидкости до температуры 95-115 °С острым паром.
В процессе дистилляции до момента разложения хлорида аммония раствор представляет собой систему NН3 - СO2 - Н2O - NаС1 - NH4С1, после разложения хлоридом аммония известковым молоком и удаления диоксида углерода система имеет вид NН3 - Н2O -NаС1 - СаС12.
Перед подачей известкового молока необходимо тщательно разложить карбонат аммония и удалить из раствора диоксид углерода. В противном случае карбонат аммония будет взаимодействовать с известковым молоком:
(NH4)2СO3(р) + Са(ОН)2(тв.) → СаСO3(тв.) + 2NН3(р) + 2Н2O(ж) - 8 кДж,
что приведет к потерям диоксида углерода и перерасходу известкового молока.
В фильтровой жидкости присутствует некоторое количество сульфата натрия, образующегося на стадии очисткы сырого рассола. При наличии в растворе ионов кальция(в хлориде кальция) протекает реакция:
Na2SO4 (р) + СаС12 (р) → СаSO4 (тв.) + 2NaС1 (р) - 13,8 кДж.
Кристаллизация и выделение сульфата кальция в процессе дистилляции вызывает нежелательные осложнения. Образующаяся соль отлагается на внутренних поверхностях аппаратов и трубопроводов, снижает их пропускную способность, а, следовательно, и производительность, увеличивает гидравлическое сопротивление, что сопряжено с необходимостью периодического, весьма трудоемкого, удаления образовавшихся инкрустаций гипса. При температурах ниже 97 °С гипс кристаллизуется в виде дигидрата - СаSO4 ×2Н2O, выше температуры 97 °С — в виде полугидрата СаSO4×1/2Н2O. В присутствии хлоридов натрия и кальция температура кристаллизации полугидрата СаSO4×1/2Н2O снижается от 97 до 93-95 °С. Выпадающий дигидрат сульфата кальция при температуре выше критической переходит в полугидрат, растворимость которого при увеличении температуры снижается. Этот процесс перекристаллизации способствует отложению твердой соли на внутренних поверхностях аппаратов.
3.5.2 Технологическая схема отделения регенерации аммиака
Общее количество аммиака, циркулирующего в производстве, составляет около 530 кг/т соды. Из них примерно 450 кг регенерируется из фильтровой жидкости по схеме так называемой большой дистилляции, представленной на рисунке 3.5. На некоторых заводах схемы несколько изменены, но эти изменения не носят принципиального характера.
Фильтровая жидкость из напорного бака 6 через расходомер 5 поступает в трубки кожухотрубного теплообменника 4 - конденсатора дистилляции КДС - и движется в нем сверху вниз. В межтрубном пространстве конденсатора дистилляции КДС противотоком жидкости движется горячая парогазовая смесь, выходящая из теплообменника дистилляции ТДС 2. В результате теплообмена фильтровая жидкость нагревается и гидрокарбонат аммония, находящийся в жидкости, разлагается. Выделяющийся диоксид углерода снижает интенсивность теплопередачи, поэтому он удаляется из трубок и присоединяется к основному потоку газа, выходящего из межтрубного пространства конденсатора дистилляции КДС.
Парогазовая смесь, проходя межтрубное пространство, охлаждается и из нее конденсируется водяной пар. В образующемся конденсате растворяется часть аммиака и диоксида углерода из газа. Конденсат удаляется из конденсатора дистилляции КДС для отдельной регенерации аммиака по схеме малой дистилляции. В случае необходимости этот конденсат можно передавать непосредственно в теплообменник дистилляции ТДС.
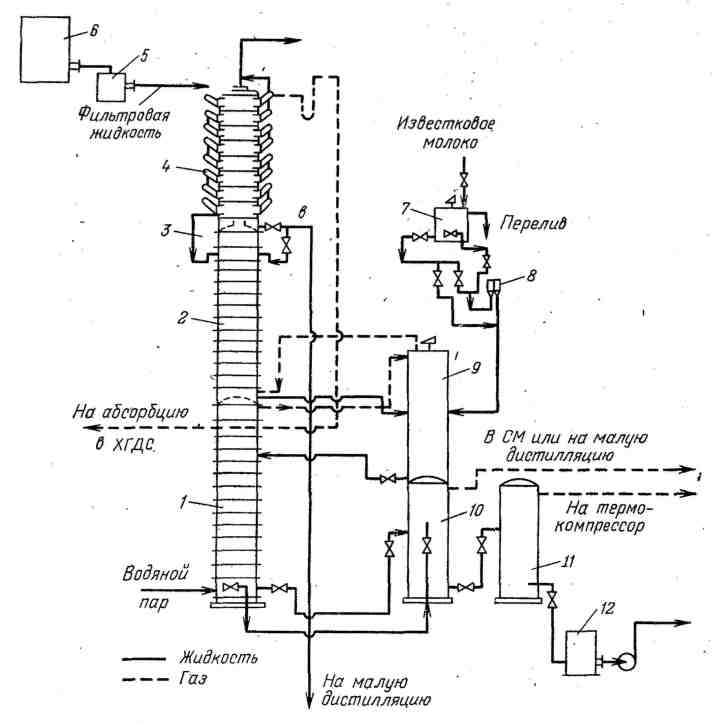
Рисунок 3.5 – Технологическая схема отделения дистилляции
Газ из конденсатора дистилляции КДС направляют для дополнительного охлаждения и осушки в холодильник газа дистилляции ХГДС, находящийся в отделении абсорбции. В результате охлаждения газа также образуется конденсат, содержащий аммиак и диоксид углерода, его направляют далее на малую дистилляцию.
После конденсатора дистилляции фильтровая жидкость поступает через внешний перелив 3 в теплообменник дистилляции ТДС 2 и движется сверху вниз, нагреваясь при непосредственном контакте с поднимающейся из дистиллера ДС 1 горячей парогазовой смесью. При этом карбонаты аммония практически полностью разлагаются с выделением диоксида углерода в газовую фазу. В теплообменнике 2 заканчивается также разложение небольших количеств гидрокарбоната и карбоната натрия при их взаимодействии с хлоридом аммония. Разложение карбонатов и удаление диоксида углерода из жидкости является основным назначением теплообменника дистилляции.
После удаления диоксида углерода жидкость смешивается в смесителе 9 с известковым молоком, поступающим из мешалки 7 через расходомер 8. В результате взаимодействия известкового молока с хлоридом аммония образуются аммиак и хлорид кальция. Оставшееся в жидкости небольшое количество карбоната аммония также реагирует с гидроксидом кальция, что приводит к излишнему расходу известкового молока и потере диоксида углерода.
Жидкость из смесителя 9 поступает в дистиллер 1 для отгонки аммиака. В нижнюю часть дистиллера ДС подают острый пар, который нагревает жидкость. При этом выделяется аммиак, его равновесное давление над раствором повышается, а парциальное давление в парогазовой фазе понижается. Последнее способствует десорбции аммиака из жидкости. Парогазовая смесь из дистиллера ДС поступает в теплообменник дистилляции ТДС, предварительно пройдя верхнюю часть смесителя, не заполненную жидкостью и выполняющую роль брызгоуловителя.
Для использования тепла горячую жидкость из дистиллера ДС направляют в первый испаритель ИС-1 10, где в результате снижения давления до атмосферного выделяется водяной пар, используемый в схеме малой дистилляции. При «горячем» режиме, когда температура жидкости в смесителе превышает 93 °С, а на выходе из дистиллера ДС составляет 115 °С, для более полного использования тепла жидкости ее направляют из первого испарителя ИС-1 во второй испаритель ИС-2 11. Здесь за счет вакуума, создаваемого термокомпрессором, выделяется дополнительное количество водяного пара с пониженным давлением и температурой, используемого на стадии малой дистилляции.
Из второго испарителя ИС-2 дистиллерная жидкость идет в пескоуловитель 12 для сепарации крупных частиц гипса и карбоната кальция, отделившихся со стенок дистиллера, а затем с помощью центробежных насосов откачивается в накопитель отбросов (по цвету откачиваемой суспензии называемый «белым морем»).
В отделении дистилляции также регенерируется аммиак из указанных выше конденсатов и так называемой слабой жидкости, образующейся в процессе охлаждения и очистки от содовой пыли газа содовых печей. Аммиачные конденсаты и слабую жидкость целесообразно перерабатывать отдельно от фильтровой жидкости.
3.6 Перспективы развития производства кальцинированной соды
Пути совершенствования производства кальцинированной соды аммиачным способом включают следующие направления:
- внедрение малоотходных комплексов по производству кальцинированной соды, хлорида кальция (либо закачивание осветленной дистиллерной жидкости в нефтяные горизонты), мелиоранта, консерванта, минеральных кормовых добавок и др.;
- разработка и внедрение технологической линии производства соды мощностью 1000-1200 т соды в сутки, оснащенной колоннами с дырчатыми противоточными и перекрестно-точными контактными элементами, пленочными, пластинчатыми и горизонтально трубчатыми теплообменниками и конденсаторами, высокоэффективными вакуум-фильтрами и кальцинаторами;
- разработка и внедрение карбонизационной колонны с пластинчатыми (или вертикально-трубчатыми) холодильными царгами, устанавливаемыми попеременно с перекрестно-точными дырчатыми контактными элементами с двойным переливом, а также с двойным вводом аммонизированного рассола;
- создание системы «карбонизационная колонна — гидроциклон — центрифуга», обеспечивающая получение гидрокарбоната натрия с минимальной влажностью;
- внедрение для коррозионной защиты оборудования диффузионно-защищенных сталей и чугуна и исключение применения титана и нержавеющих сталей в качестве конструкционных материалов для изготовления аппаратов содового производства;
- разработка и внедрение способа сокращения объема дистиллерной жидкости за счет получения известковой суспензии репульпированием сухого гидроксида кальция (пушонки) дистиллерной жидкостью, непосредственным гашением кусковой извести дистиллерной жидкостью, прямого взаимодействия сухой извести со свободной от диоксида углерода фильтровой жидкостью (например, подача сухой извести в смеситель); выбор способа зависит от конкретных условий его внедрения;
- энергетическое совершенствование содового производства.
