
- •6.070800 «Экология и охрана окружающей среды»
- •Введение
- •1 Производство синтетического аммиака
- •1.1 Методы производства азота и водорода
- •1.2 Промышленный катализ
- •1.3 Очистка природных газов от соединений серы
- •1.4 Конверсия метана
- •1.5 Конверсия оксида углерода (II)
- •1.6 Технологическая схема производства конвертированного газа
- •1.7 Очистка конвертированного газа от диоксида углерода
- •1.8 Тонкая очистка конвертированного газа от кислородсодержащих соединений
- •1.9 Технологическая схема очистки конвертированного газа от кислородсодержащих соединений
- •1.10 Синтез аммиака из смеси азота и водорода
- •1.11 Синтез метанола из оксида углерода и водорода
- •2 Производство неорганических кислот
- •2.1 Производство азотной кислоты
- •2.2 Производство серной кислоты
- •3 Производство кальцинированной соды
- •3.1 Принципиальная схема производства соды аммиачным
- •3.2 Аммонизация очищенного рассола
- •3.3 Карбонизация аммонизированного рассола
- •3.4 Кальцинация гидрокарбоната натрия
- •3.5 Регенерация аммиака в производстве кальцинированной соды
- •4 Производство минеральных удобрений
- •4.1 Производство карбамида
- •4.2 Производство нитрата аммония
- •4.3 Производство сульфата аммония
- •4.4 Производство нитрата калия
- •4.5 Производство суперфосфата
- •Рекомендованная литература
3 Производство кальцинированной соды
Углекислая сода (карбонат натрия) была известна еще в глубокой древности. Издавна соду получали из золы морских и солончаковых растений и извлекали из рапы природных содовых озер. Ее использовали в стеклоделии и в качестве моющего средства. К концу XVIII в. эти источники уже не могли удовлетворить возрастающую потребность в соде. В 1775 г. французский фармацевт Н. Леблан предложил получать соду прокаливанием смеси сульфата натрия, измельченного мела или известняка и угля согласно реакции:
Na2SO4 + СаСO3 + 2С → Nа2CO3 + СаS + 2СO2.
Из полученного плава соду выщелачивали водой, а раствор упаривали, выделяя карбонат натрия в твердом виде. В шламе оставался сульфид кальция, являющийся отходом производства.
Так как в природе натрий встречается чаще в виде хлорида натрия, необходимый для производства соды сульфат натрия было предложено получать взаимодействием хлорида натрия и серной кислоты.
Способ Н. Леблана сыграл большую роль в развитии химической промышленности и разработке сырьевых баз. Вокруг содовых заводов концентрировались производства и других продуктов. Разработка способа получения сульфата натрия повлекла за собой развитие производства серной кислоты, а за ней и азотной, поскольку серную кислоту получали лишь нитрозным способом с помощью азотной кислоты. Отход содового производства – хлороводород - перерабатывали на хлор и хлорные продукты: белильную известь и бертолетовую соль. Из отхода – сульфида кальция - получали элементарную серу. Огарок после обжига медистого серного колчедана, служившего сырьем для получения серной кислоты, использовали для производства медного купороса и других солей меди. Сама сода использовалась как исходный продукт для получения многих натриевых соединений, например NаНСО3, NаОН, Nа2SO3, NаНSO3 и др.
Содовые заводы стали центрами зарождавшейся химической промышленности. В немалой степени содовые заводы содействовали также развитию сырьевых баз по добыче таких видов сырья, как серный колчедан, мел, известняк, поваренная соль, сульфат натрия, чилийская селитра, из которой в те годы готовили азотную кислоту.
В 1861 г. бельгийским инженером Э. Сольве был разработан и осуществлен в промышленном масштабе аммиачный способ получения соды, отличавшийся следующими преимуществами: более высоким качеством получаемого продукта, непрерывностью процесса, лучшими условиями труда и меньшим расходом рабочей силы, снижением расхода тепла, а следовательно, и топлива, возможностью применения растворов хлорида натрия, более дешевых, чем твердая поваренная соль, необходимая при способе Н. Леблана. В целом «аммиачная сода» получалась более дешевой и лучшего качества.
3.1 Принципиальная схема производства соды аммиачным
способом
Взаимная связь отдельных основных операций содового завода, работающего по методу Э. Сольве, показана на рисунке 3.1.
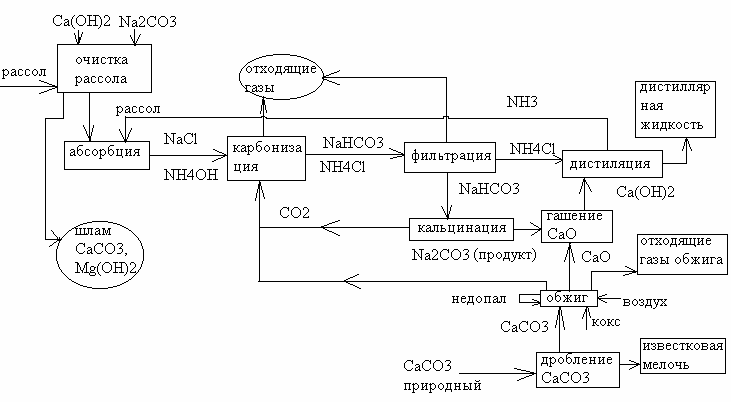
Рисунок 3.1 – Принципиальная технологическая схема производства кальцинированной соды аммиачным способом
В аммиачном способе кальцинированную соду получают через гидрокарбонат аммония:
NH4HСО3 + NaCl → NaHСО3 + NH4Cl.
На содовых заводах гидрокарбонат аммония получают из аммиака и диоксида углерода непосредственно в водных растворах хлорида натрия, т. е. с химической точки зрения процесс получения гидрокарбоната натрия можно объединить в виде одной реакции:
NaCl + NН3 + СO2 + Н2O → NaHСО3 + NH4Cl.
Так как диоксид углерода плохо растворяется в воде в отсутствие аммиака, то практически сначала раствор хлорида натрия (рассол) насыщают аммиаком, а затем полученный аммонизированный рассол обрабатывают диоксидом углерода, т. е. процесс проводят в две ступени. Первая ступень (поглощение аммиака) протекает в отделении аммонизации-абсорбции, а вторая (поглощение диоксида углерода) - в отделении карбонизации.
Выпавший в процессе карбонизации осадок гидрокарбоната натрия NаНСО3 отфильтровывают, и далее он разлагается с получением соды:
2NaHСО3 → Nа2СO3 + СO2 + Н2O.
В зависимости от конструкции печи температура разложения бикарбоната натрия NaНСО3 находится в пределах 160-180 °С. Процесс разложения бикарбоната натрия протекает в отделении кальцинации. Выделяющийся диоксид углерода повторно используют в процессе карбонизации.
Кроме основных процессов на содовых заводах осуществляется ряд побочных, не имеющих непосредственного отношения к получению кальцинированной соды. Образующийся по реакции хлорид аммония завод может выпускать как дополнительный готовый продукт. Однако обычно на содовых заводах аммиак регенерируют из хлорида аммония и возвращают обратно в производство. С этой целью гидрокарбонатный маточник, содержащий хлорид аммония NH4Cl, обрабатывают известковым молоком:
2 NH4Cl + Са(OН)2 → 2NН3 + 2Н2O + СаСl2.
Образующийся аммиак отгоняют из раствора и направляют в отделение абсорбции. Раствор хлорида кальция является отходом производства. Эта операция регенерации аммиака протекает в отделении дистилляции. На некоторых заводах раствор хлорида кальция используется для получения продукционного хлорида кальция СаС12.
Для получения известкового молока необходим оксид кальция СаО, который на содовых заводах получают путем обжига карбонатного сырья (мела или известняка) в известково-обжигательных печах при температуре 1100-1200 °С. Образующийся по реакции диоксид углерода:
СаСО3 → СаО + СO2
используют в процессе карбонизации, а оксид кальция (негашеная известь СаО) гасят избытком воды с получением известкового молока:
СаО + Н2O → Са(ОН)2.
И, наконец, на всех содовых заводах производится предварительная очистка водного раствора хлорида натрия (сырого рассола) от примесей - солей кальция и магния с помощью карбоната натрия и известкового молока. В процессе очистки образуются плохо растворимые гидроксид магния и карбонат кальция, выпадающие в осадок:
MgС12 + Са(ОН)2 → Мg(ОН)2 + СаСl2
СаС12 + Nа2СO3 → СаСО3 + 2NaСl.
