- •6.070800 «Экология и охрана окружающей среды»
- •Введение
- •1 Производство синтетического аммиака
- •1.1 Методы производства азота и водорода
- •1.2 Промышленный катализ
- •1.3 Очистка природных газов от соединений серы
- •1.4 Конверсия метана
- •1.5 Конверсия оксида углерода (II)
- •1.6 Технологическая схема производства конвертированного газа
- •1.7 Очистка конвертированного газа от диоксида углерода
- •1.8 Тонкая очистка конвертированного газа от кислородсодержащих соединений
- •1.9 Технологическая схема очистки конвертированного газа от кислородсодержащих соединений
- •1.10 Синтез аммиака из смеси азота и водорода
- •1.11 Синтез метанола из оксида углерода и водорода
- •2 Производство неорганических кислот
- •2.1 Производство азотной кислоты
- •2.2 Производство серной кислоты
- •3 Производство кальцинированной соды
- •3.1 Принципиальная схема производства соды аммиачным
- •3.2 Аммонизация очищенного рассола
- •3.3 Карбонизация аммонизированного рассола
- •3.4 Кальцинация гидрокарбоната натрия
- •3.5 Регенерация аммиака в производстве кальцинированной соды
- •4 Производство минеральных удобрений
- •4.1 Производство карбамида
- •4.2 Производство нитрата аммония
- •4.3 Производство сульфата аммония
- •4.4 Производство нитрата калия
- •4.5 Производство суперфосфата
- •Рекомендованная литература
2 Производство неорганических кислот
Серная и азотная кислоты, производство которых будет рассмотрено в данном разделе, по объему производства и сферам применения занимают первые два места среди кислот. Они являются одними из основных продуктов химической промышленности и применяются в различных отраслях промышленности.
2.1 Производство азотной кислоты
Области применения азотной кислоты весьма разнообразны. Большая часть ее (до 75-80 %) расходуется на производство азотных и комплексных минеральных удобрений, разнообразных нитратов; 10-15 % идет на получение взрывчатых веществ и ракетного топлива, остальное количество потребляется производством красителей, органическим синтезом. используется в цветной металлургии для травления металлов.
Азотная кислота известна человечеству с VIII века. Она была первой минеральной кислотой, которую использовали в ремесленной практике. Первое упоминание о ней содержится в трудах арабского ученого Гебера (778 год), который привел способ получения азотной кислоты перегонкой смеси селитры с квасцами. Получение азотной кислоты нагреванием смеси селитры с квасцами или купоросом было описано итальянским ученым В. Бирингуччо (1540 год) и Г. Агриколой (1556 год). В 1648 году И. Глаубер получил азотную кислоту нагреванием селитры с серной кислотой, а в 1763 году М.В. Ломоносов исследовал и описал этот метод ее получения.
Первые исследования процесса синтеза азотной кислоты из аммиака относятся к началу XIX века. В 1800 году А. Фуркруа наблюдал образование оксидов азота при пропускании смеси аммиака с воздухом через раскаленную трубку. В 1839 году Кюльман получил оксиды азота окислением аммиака на платиновом катализаторе, высказав при этом предположение, что «могут наступить времена, когда это превращение в экономическом отношении станет возможным». Вначале XX века условия окисления аммиака детально изучаются В. Оствальдом и И.И. Андреевым, делаются попытки освоить этот метод в промышленных условиях. В 1907 году В. Оствальд создает опытно-промышленную установку для получения азотной кислоты каталитическим окислением аммиака. В 1916 году на основе теоретических исследований И.И. Андреева создается опытная установка, а в 1917 году в г. Юзовка был введен в строй первый завод по производству азотной кислоты из аммиака коксового газа мощностью 10000 тонн в год.
Независимо от конкретной технологической схемы принципиальная схема производства разбавленной азотной кислоты включает шесть основных операций (см. рисунок 2.1).
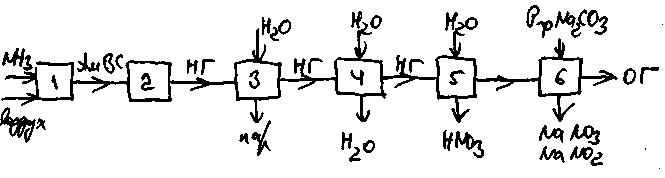
1 — очистка аммиака и воздуха, их смешение; 2 — окисление аммиака на катализаторе; 3, 4 — охлаждение нитрозных газов с использованием теплоты процесса окисления; 5 — окисление оксида азота (II) и образование азотной кислоты; 6 — очистка (нейтрализация) отходящих газов.
АмВС — аммиачно-воздушная смесь, НГ — нитрозные газы, ОГ — отходящие газы
Рисунок 2.1 - Структурная схема производства азотной кислоты
Аммиак и воздух, очищенные от примесей, смешиваются и направляются на стадию окисления аммиака. Разогретая за счет теплоты реакций газовая смесь (нитрозные газы) охлаждается в котле-утилизаторе с выработкой технологического пара и холодильнике, где происходит частичное окисление оксида азота (II) до оксида азота (IV). Дальнейшее окисление его осуществляется одновременно с образованием азотной кислоты в процессе абсорбции оксида азота (IV) водой. Отходящие газы, содержащие остаток не вступившего в реакцию оксида азота (IV), очищают нейтрализацией раствором карбоната натрия или другим способом, после чего выбрасывают в атмосферу.
Процесс производства азотной кислоты средней концентрации контактным окислением аммиака состоит из двух основных стадий: получения оксида азота (II) и переработки его в азотную кислоту. На этой последней стадии происходит окисление NO до высших оксидов азота с последующим поглощением их водой.
Первая стадия - окисление аммиака в оксид азота (II) - в общем виде описывается реакцией:
4NH3 + 5O2 = 4NO + 6H2O.
Вторая стадия - окисление оксида азота (II) в высшие оксиды и переработка их в азотную кислоту - может быть представлена в виде уравнений:
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO.
Суммарная реакция без учета побочных реакций, протекающих с образованием элементарного азота, может быть представлена уравнением
NH3 + 2O2 = HNO3 + H2O + 421,2 кДж.
2.1.1 Контактное окисление аммиака
При окислении аммиака в зависимости от катализатора и условий ведения процесса можно получить оксид азота (II), элементарный азот, а иногда и оксид азота (I).
При контактном окислении аммиака возможны следующие реакции:
4NH3 + 5O2 = 4NO + 6H2O + 907,3 кДж.
4NH3 + 4O2 = 2N2O + 6H2O +1104,9 кДж.
4NH3 + 3O2 = 2N2 + 6H2O + 1269,1 кДж.
Установлено, что по мере образования оксида азота (II) из аммиака он способен окислять аммиак по реакции:
4NH3 + 6NO = 5N2 + 6H2O
Следует отметить, что приведенные выше реакции окисления аммиака являются суммарными и не отражают происходящих при этом элементарных каталитических процессов.
Согласно термодинамическим расчетам изменения свободной энергии, все реакции могут идти практически до конца. Таким образом, при окислении аммиака, как в процессе, который может протекать в нескольких направлениях, состав конечных продуктов определяется прежде всего избирательной способностью катализатора.
Катализатор из платинового сплава в настоящее время является наилучшим для избирательного окисления аммиака в оксид азота (II). Выход оксида азота (II) при контактном окислении аммиака на платине в области температур 1070-1120 К может достигать 97-98 % при атмосферном давлении и 96-97 % при ведении процесса в пределах 1150-1200 К под давлением 0,8 МПа.
При окислении аммиака на платине образуются промежуточные вещества:


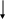
N2O3 + O → промежуточные вещества→ NO → N2 + H2O
По данным различных исследователей, такими промежуточными соединениями могут быть: имидогруппа NH, диимид N2H2, атомарный азот N, амидогруппа NH2, нитроксил HNO, гидроксиламин NH2OH.
В соответствии с адсорбционно-химической теорией катализа механизм каталитического окисления аммиака можно представить следующим образом (см. рисунок 2.2).
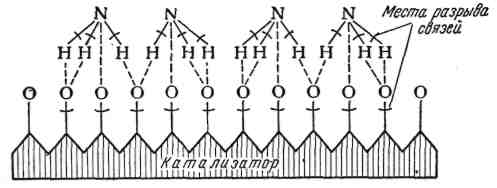
Рисунок 2.2 – Схема процесса окисления аммиака на поверхности платины
Кислород и аммиак диффундируют из газовой смеси к поверхности катализатора. При стехиометрическом соотношении О2 : NH3 = 5:4 скорость процесса контролируется диффузией кислорода к поверхности катализатора, в данном случае платины. Вследствие недостатка кислорода окисление аммиака на открытой поверхности платины происходит без образования кислородных соединений азота до элементарного азота. При избытке кислорода в газе (сверх стехиометрического количества) контролирующей стадией процесса является скорость переноса аммиака к поверхности платины, покрытой кислородом. При 393-573 К кислород прочно связывается с поверхностью платины, образуя несколько молекулярных слоев.
Ввиду наличия на поверхности платины атомов со свободными валентностями, в первую очередь происходит активированная адсорбция кислорода, определяемая электронной связью. Вследствие химического взаимодействия кислорода с поверхностью платины ослабляется связь между атомами О2 и образуется переходный комплекс адсорбции (катализатор - кислород). В последующей стадии активированной адсорбции аммиака образуется новый комплекс (катализатор - кислород - аммиак).
На различных катализаторах молекулы кислорода и аммиака могут образовывать различные типы связей с поверхностью и, в зависимости от условий, давать разные промежуточные продукты реакции, в том числе перечисленные выше. Далее происходит перераспределение электронных связей, в результате чего атомы азота и водорода, соединяясь с кислородом, образуют воду и оксид азота (II). Вновь образовавшиеся устойчивые химические соединения (NO и Н2О) обладают меньшей адсорбционной способностью по отношению к платине, чем кислород и аммиак, в связи с чем их молекулы десорбируются с поверхности катализатора.
Как правило, при избытке кислорода на поверхности катализатора происходит образование молекул NO, при недостатке кислорода образуются молекулы азота.
Все этапы превращения аммиака в оксид азота (II), в том числе и промежуточные стадии, протекают на поверхности катализатора. Оксид азота (II) может образоваться только на поверхности катализатора, и в этом состоит его существенное значение для окисления аммиака, тогда как азот образуется и в объеме, вне поверхности катализатора.
Платина - дорогой катализатор, однако она в течение длительного времени сохраняет высокую активность, достаточно устойчива, обладает механической прочностью, легко регенерируется, быстро накаляется, расход ее на единицу продукции незначителен.
На современных заводах платину для катализаторов применяют в виде сеток. Такая форма платинового катализатора дает возможность использовать наиболее простой тип контактных аппаратов. При использовании катализаторных сеток из сплава платины с родием (до 10 % Rh) выход оксида азота (II) увеличивается на 2,5-3 % по сравнению с выходом на чистой платине, кроме того, уменьшаются потери катализатора. Введение в сплав палладия способствует повышению прочности катализатора. В нашей стране применяется катализатор, состоящий из 93 % платины, 3 % родия и 4 % палладия.
Реакция окисления аммиака на платине начинается при 420 К, при дальнейшем повышении температуры увеличивается выход оксида азота (II) и одновременно ускоряется реакция. В интервале температур 1150-1200 К выход оксида азота (II) достигает уже 96-98 %. С переходом на режим повышенных температур схема производства азотной кислоты усложняется, но при этом увеличивается скорость окисления аммиака.
Необходимый температурный режим может быть обеспечен за счет теплоты реакции окисления аммиака. Теоретическое повышение температуры газа на 1 % окисленного аммиака в смеси составляет около 70 К. Применяя аммиачно-воздушную смесь, содержащую 10 % аммиака, можно вести процесс при 980 К за счет выделения теплоты реакции. Для достижения более высокой температуры следует предварительно подогревать воздух или аммиачно-воздушную смесь, либо увеличивать содержание аммиака в газовой смеси.
Содержание аммиака в аммиачно-воздушной смеси ограничивается концентрацией кислорода в воздухе. Расход кислорода на проведение собственно окисления аммиака в оксид азота (II) определяется реакцией:
4NH3 + 5O2 = 4NO + 6H2O + 907,3 кДж.
По этой реакции на 1 моль аммиака требуется 1,25 моль кислорода, а максимальное содержание NH3 в аммиачно-воздушной смеси составляет:
![]()
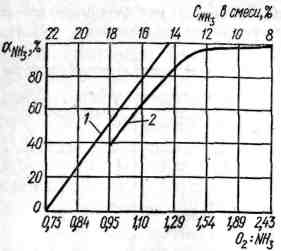
Однако при мольном соотношении О2 : NH3 = 1,25 степень превращения аммиака в оксид азота (II) незначительна. Для увеличения выхода оксид азота (II) оксида азота (II) требуется определенный избыток кислорода, что, естественно, вызывает необходимость уменьшения содержания NH3 в аммиачно-воздушной смеси (ниже 14,4 %).
1 – теоретическая; 2 - практическая Рисунок 2.3 – Зависимость степени окисления аммиака от соотношения О2:NH3 |
Как следует из рисунка 2.3, резкое снижение степени контактирования происходит при соотношении О2: NH3 < 1,7, т. е. при содержании 11,5 % аммиака в аммиачно-воздушной смеси. При соотношении О2:NH3 > 2 степень контактирования NH3 повышается незначительно. Таким образом, избыток кислорода по сравнению со стехиометрическим количеством должен составлять не менее 30 %. |
Кроме активности катализатора, соотношения О2 : NH3 в смеси и температуры контактирования степень превращения аммиака в оксид азота (II) зависит и от скорости газового потока или обратной ей величины - времени пребывания аммиачно-воздушной смеси в зоне катализа (время контактирования). При температуре 1150-1170 К оптимальное время контактирования составляет 0,8 ∙ 10-4 – 1,0 ∙ 10-4 с.
Платиновый катализатор чрезвычайно чувствителен ко всем загрязнениям, обычно находящимся в воздухе и аммиаке. Поэтому для сохранения высокой активности катализатора существенное значение имеет чистота используемых аммиака и воздуха.
Одним из условий достижения высокой степени контактирования является полная однородность аммиачно-воздушной смеси, поступающей на катализаторные сетки. Тщательное смешение газов позволяет не только достигать высокой степени контактирования, но и предотвращает возможность взрыва. Конструкция и объем смесителя обязаны в полной мере обеспечивать хорошее перемешивание газов без проскока аммиака на катализатор отдельными струями.
В производстве азотной кислоты методом контактного окисления аммиака применяют повышенное давление. Это связано с необходимостью увеличения скоростей последующего окисления оксида азота (ІІ) и образования азотной кислоты. Следует отметить,что повышение давления до 0,75 МПа незначительно сказывается на величине степени окисления аммиака, но при этом увеличивается производительность установки, повышается компактность системы. Недостатком применения высокого давления являются большие потери катализатора.
2.1.2 Окисление оксида азота (ІІ)
Нитрозные газы, полученные путем контактного окисления аммиака, содержат в основном оксид азота (II), из которого при дальнейшем окислении образуются высшие оксиды азота.
По устойчивости в ряду термодинамической устойчивости оксиды азота располагаются в такой последовательности:
При 273 К - N2О4 > N2О > N2О5 > NО2 > N2О3 > NO
При 1170 К - NO > N2О > NО2 > N2О3 > N2О4 > N2О5
Последовательное образование высших оксидов азота из оксида азота (ІІ) осуществляется по реакциям:
2NO + O2 ↔ 2NO2
NO + NO2 ↔ N2O3
2NO2 ↔ N2O4 .
С понижением температуры равновесие этих реакций смещается вправо. При низких температурах и времени, достаточном для установления равновесия, а также при избытке кислорода можно ожидать превращения всех оксидов азота в N2O4. При недостатке кислорода или неустановившемся равновесии в нитрозных газах могут одновременно содержаться перечисленные выше оксиды азота, т. е. NO, N2O3, NO2 и N2O4.
Зависимость равновесной степени окисления оксида азота (ІІ) от температуры и давления при начальной концентрации 9,92 % оксида азота (ІІ) и 5,68 % кислорода в газе показана на рисунке 2.4.
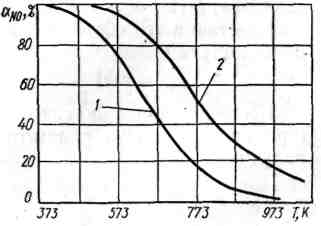
1- давление в системе – 0,1 МПа; 2- давление в системе – 0,8 МПа
Рисунок 2.4 - Зависимость равновесной степени окисления оксида азота (ІІ) от температуры и давления
Из данных рисунка 2.4 следует, что понижение температуры и повышение давления газа смещают равновесие реакции вправо. При температурах ниже 200 °С реакцию окисления оксида азота (ІІ) при давлении 0,1 МПа можно рассматривать как реакцию, протекающую необратимо в сторону образования оксида азота (IV). При температурах выше 700 °С происходит почти полная диссоциация оксида азота (IV) на оксид азота (ІІ) и кислород.
Особенностью данной реакции окисления является повышение ее скорости с понижением температуры. Энергия активации для данной реакции, вычисленная по уравнению Аррениуса, имеет отрицательное значение, равное - 7,5 кДж/моль. Отрицательное значение энергии активации элементарной реакции находится в противоречии с представлениями классической теории соударений. Вероятность одновременного соударения трех молекул очень мала. Поэтому реакция образования оксида азота (IV) может быть осуществлена по схеме двух бимолекулярных реакций (ступеней):
NO + O2 = NO ∙ O2
NO ∙ O2 + NO = 2NO2 .
При указанном двухстадийном механизме допускается, что первая реакция протекает очень быстро, причем с повышением температуры ее скорость увеличивается. С повышением температуры равновесие смещается влево, в сторону распада NO ∙ O2. Вторая реакция протекает более медленно. Таким образом, с понижением температуры концентрация NO ∙ O2 увеличивается. Это приводит к ускорению второй реакции, которая является определяющей для скорости суммарного процесса.
Таким образом, для ускорения медленно протекающей реакции окисления оксида азота (ІІ) в оксида азота (ІV) необходимыми условиями являются: понижение температуры, высокие давления и возможно более высокие концентрации оксида азота (ІІ) и кислорода в газовой смеси.
2.1.3 Переработка оксидов азота в разбавленную азотную кислоту
Переработку оксидов, полученных окислением оксида азота (ІІ), в разбавленную азотную кислоту в промышленности осуществляют путем абсорбции оксидов из газовой фазы водой или водным раствором азотной кислоты. Для этого нитрозные газы охлаждают и направляют в поглотительные башни или абсорбционные колонны, где происходят окисление оксида азота (ІІ) и поглощение образовавшихся оксидов азота. В зависимости от условий охлаждения и окисления в газовой фазе могут находиться оксиды азота различной степени окисления. Все они, за исключением оксида азота (II), реагируют с водой. При этом протекают следующие реакции:
2NO2 + H2O = HNO3 + HNO2 + 116,1 кДж
N2O4 + H2O = HNO3 + HNO2 + 59,2 кДж
N2O3 + H2O = 2HNO2 + 55,4 кДж.
Азотистая кислота, образующаяся при абсорбции, малоустойчива и разлагается:
3HNO2 = HNO3 + 2NO + H2O – 75,87 кДж.
Суммарная реакция представится в виде:
3NO2 + H2O = 2HNO3 + NO + 136,2 кДж
Из NO2 и N2O4 образуются эквивалентные количества азотной и азотистой кислот. Практически безразлично, какой из оксидов реагирует с водой - NO2 или N2O4, поскольку скорость их взаимного превращения очень велика, а количество образующихся из NO2 и N2O4 азотистой и азотной кислот одинаково. Большинство исследователей, определяя те или иные параметры процесса окисления оксида азота (II), пересчитывают N2O4 в NO2. Такой условный пересчет практически вполне допустим, так как при заданной температуре соотношение количеств NO2 и N2O4 вполне определенно.
Главными факторами, определяющими большую скорость образования азотной кислоты из оксида азота (IV), являются проведение процесса абсорбции под давлением при пониженных температурах с применением богатых по содержанию оксидов азота нитрозных газов и создание условий для более полного соприкосновения газа с жидкостью.
Процесс абсорбции оксидов азота водой связан с растворением в ней оксидов NO2, N2O4 и N2O3 и с образованием азотной и азотистой кислот. В газовой фазе в результате взаимодействия паров воды с оксидами азота образуются также незначительные количества азотной и азотистой кислот.
Скорость окисления вторичного оксида азота (ІІ), растворенного в жидкой фазе, при барботажном режиме увеличивается с повышением концентрации азотной кислоты, нитрозности газа и с увеличением его линейной скорости. Расчеты показывают, что в колоннах ситчатого типа, работающих под давлением, доля гомогенного окисления вторичного оксида азота (II) в газовой фазе составляет 85-90 %, доля гетерогенного окисления NO в жидкой фазе равна 10-15 %.
Равновесная степень поглощения оксида азота (IV) растворами азотной кислоты при 308 К представлена на рисунке 2.5. Из этой диаграммы следует, что при парциальном давлении оксида азота (IV) 0,01 МПа получение азотной кислоты, имеющей концентрацию более 60 % HNО3, практически затруднительно при использовании нитрозных газов с низким парциальным давлением оксидов азота.
Из анализа данных, приведенных на рисунке 2.6, следует, что с повышением давления при поглощении оксидов азота удельные абсорбционные объемы сильно уменьшаются. В перспективе предстоит переход на абсорбцию оксидов азота при повышенном давлении (порядка 1,1-2,5 МПа). Поскольку толщина стенок абсорбционной колонны увеличивается пропорционально давлению в первой степени, с повышением давления капитальные затраты на абсорбционную установку значительно снижаются.
Применение повышенного давления позволяет достичь высокой степени поглощения нитрозных газов и добиться санитарной нормы их содержания в выхлопном газе (0,005 % об.).
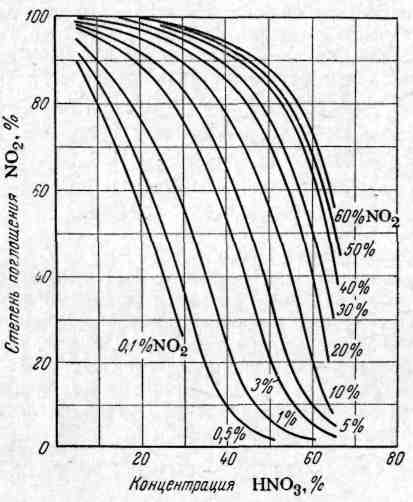
Рисунок 2.5 – Зависимость равновесной степени абсорбции оксида азота (IV) от концентрации азотной кислоты при 308 К и общем атмосферном давлении
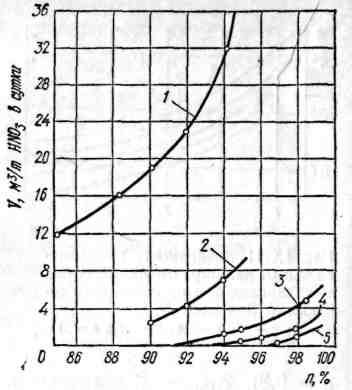
1 – давление 0,1 МПа; 2 – давление 0,17 МПа; 3 – давление 0,35 МПа;
4 – давление 0,5 МПа; 5 – давление 0,7 МПа
Рисунок 2.6 – Зависимость удельного абсорбционного объема от степени абсорбции оксидов азота азотной кислотой и давления
Уменьшение размеров абсорбционных колонн позволяет также снизить удельные капитальные затраты и амортизационные отчисления. Поэтому повышение мощности агрегатов приводит к снижению затрат на строительство азотнокислотных систем.
2.1.4 Технологическая схема производства разбавленной азотной
кислоты
В приведенной выше принципиальной схеме производства разбавленной азотной кислоты стадии окисления аммиака и переработки нитрозных газов различаются режимами проведения процессов. Для первой стадии оптимальными условиями являются высокая температура и относительно низкое давление, для второй стадии - низкая температура и высокое давление, что следует из физико-химических закономерностей этих процессов. Поскольку определяющим параметром является давление, все существующие технологические схемы производства разбавленной азотной кислоты делятся на три типа:
- при атмосферном давлении (тип I),
- при высоком давлении (тип II),
- с двумя ступенями давления (комбинированные схемы) (тип III).
Характеристики и особенности этих типов технологических схем приведены в таблице 2.1.
Таблица 2.1 – Характеристики систем
NH3 → NO → NO2 → HNO3 |
Тип системы |
Степень превращения
|
Особенности процесса |
|
Давление на всех стадиях равно 0,1 МПа |
I |
0,90 |
Большой абсорбционный объем; необходимость улавливания |
|
Давление на всех стадиях более 0,1 МПа |
II |
0,98 |
Высокие потери катализатора |
|
Давление на I стадии равно 0,1 МПа |
Давление на II стадии более 0,1 МПа |
III |
0,96-0,98 |
Устранены недостатки I и II типа |
Вследствие малой производительности, громоздкости аппаратуры, значительных потерь аммиака, малой степени абсорбции и, как следствие, необходимости в дорогостоящих очистных сооружениях, установки, работающие при атмосферном давлении, потеряли свое значение и не строятся.
Схема установки производства разбавленной азотной кислоты, работающей под общим давлением 0,73 MПa, приведена на рисунке 2.7. Производительность установки составляет 360 т/сутки в пересчете на моногидрат.
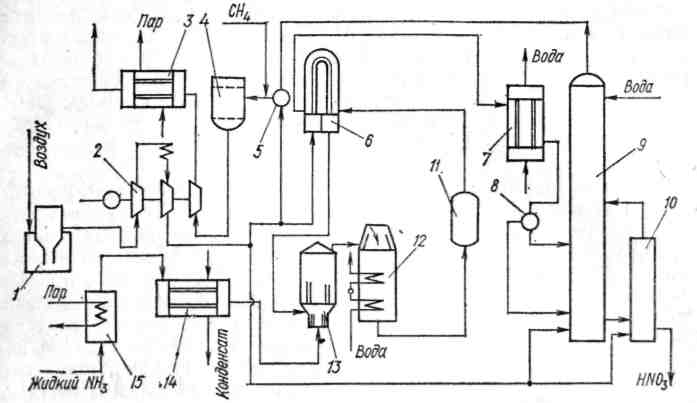
Рисунок 2.7 – Технологическая схема производства разбавленной азотной кислоты под общим давлением 0,73 МПа
Воздух через фильтр 1 поступает в двухступенчатый турбокомпрессор 2 и затем сжатый до 0,73 МПа разделяется на три части. Основная часть воздуха подогревается в теплообменнике 6 до температуры 470 К и поступает в смеситель 13.
Жидкий аммиак испаряется в испарителе 15, подогревается в паро-теплообменнике 14 и поступает в смеситель 13. Полученная в смесителе 13 воздушно-аммиачная смесь, содержащая 11,5 % об. аммиака, направляется в контактный агрегат 12, где при температуре контактирования 1200 К с принятой степенью контактирования 96 % происходит окисление аммиака. Пар, получаемый в котле-утилизаторе, расположенном непосредственно в контактном агрегате, имеет давление 1,7 МПа и температуру 500 К.
Полученный нитрозный газ проходит окислитель 11, затем подогреватель воздуха 6 и направляется в холодильник 7, в котором происходят охлаждение нитрозного газа до 320 К и конденсация паров воды. При этом получается 40 %-й раствор азотной кислоты. В сепараторе 8 полученный конденсат отделяется от нитрозного газа.
Нитрозный газ поступает в нижнюю часть абсорбционной колонны 9, а конденсат - на вышерасположенную тарелку, где образуется примерно 47 %-й раствор кислоты. Вода поступает в верхнюю часть абсорбционной колонны с 50 тарелками. В абсорбционную колонну 9 подается добавочный воздух. Степень абсорбции оксидов азота равна 99-99,5 %.
Полученная кислота (56-60 %-й раствор азотной кислоты) поступает в продувочную колонну 10. В продувочную колонну также подается воздух с температурой около 400 К.
В смесителе 5 выхлопные газы смешиваются с третьей частью воздуха после компрессора, затем с природным газом и поступают в реактор 4. Здесь происходит полное взаимодействие кислорода с метаном и последующее восстановление оксидов азота до азота. Катализатором служит палладий, нанесенный на подложку (оксид алюминия). Температура катализа составляет 1000 К. В дальнейшем газ расширяется в газовой турбине и с температурой около 680 К поступает в паровой котел 3, после чего выбрасывается в выхлопную трубу. Температура газа после газовой турбины равна 680 К. Содержание оксида азота (II) в выхлопных газах – не более 0,005 % об.
2.1.5 Перспективы развития азотнокислотного производства
Исключительное значение азотной кислоты для многих отраслей народного хозяйства и оборонной техники и большие объемы производства обусловили интенсивную разработку эффективных и экономически выгодных направлений совершенствования азотнокислотного производства. К таким направлениям относятся:
- создание систем высокой единичной мощности (до 400 тыс. т/год), работающих по комбинированной схеме;
- разработка высокоактивных избирательно действующих неплатиновых катализаторов окисления аммиака;
- возможно более полное использование энергии сжатых отходящих газов и низкопотенциальной теплоты процессов путем создания полностью автономных энерготехнологических схем;
- создание замкнутого оборота охлаждающей воды;
- решение проблемы очистки отходящих газов с утилизацией оксидов азота путем внедрения адсорбционно-десорбционного метода очистки на силикагеле и цеолитах;
- возможно более полное удаление остатков оксидов азота из отходящих газов с использованием в качестве восстановителей горючих газов и аммиака.