
- •Сравнительная характеристика внехромосомных факторов наследственности
- •Изменчивость бактерий
- •Сравнительная характеристика изменчивости
- •Генотипическая изменчивость
- •Фенотипическая изменчивость
- •Практическое использование изменчивости
- •Медицинская биотехнология и генная инженерия
- •Геномика
- •Учение об инфекционном процессе инфекционные заболевания в патологии человека
- •Инфекционный процесс и факторы, влияющие на него
- •Особенности микроорганизма-возбудителя:
- •Вид возбудителя.
- •Факторы, влияющие на восприимчивость макроорганизма:
- •Состояние конститутивных (врожденный иммунитет) и индуцибельных (приобретенный иммунитет) иммунных механизмов.
- •Возраст.
- •Индивидуальная восприимчивость.
- •Наследственная предрасположенность.
- •Перенесенные заболевания и другие факторы, подавляющие защитные функции организма.
- •III. Условия (факторы) внешней среды, в которых взаимодействуют макро- и микроорганизм:
- •Классификации инфекционных заболеваний
- •В зависимости от хозяина:
- •По природе возбудителя:
- •В зависимости от степени выраженности клинических проявлений:
- •По длительности течения (по продолжительности взаимодействия возбудителя с макроорганизмом):
- •По кратности заражения (инфицирования):
- •Инфекция с однократным заражением организма.
- •По числу видов возбудителей:
- •По пути проникновения возбудителя (инфицирования):
- •По месту заражения:
- •Внебольничная.
- •По источнику инфекции:
- •Характеристика механизмов и путей передачи инфекции
- •В зависимости от поражаемых систем органов:
- •По степени распространения возбудителя в организме хозяина:
- •Генерализованная (общая) — микроорганизм распространяется (диссеминирует) из ворот инфекции лимфогенным, гематогенным путем или по отросткам нейронов:
- •По распространению и охвату территории:
- •Периоды инфекционного заболевания
- •Характеристика периодов инфекционного заболевания
- •Патогенность
- •Потенциальность — может реализоваться при определенных условиях:
- •Полидетерминантность — контролируется совокупностью хромосомных генов и мобильных генетических элементов (плазмид, транспозонов, умеренных фагов).
- •Качественная категория.
- •Генотип патогенного микроорганизма фенотипически проявляется вирулентностью. Вирулентность
- •Количественная категория. Определение вирулентности. Качественное определение вирулентности проводится прямым (биопроба) или косвенным (наличие ферментов вирулентности) способами.
- •Факторы патогенности
- •Колонизацию — размножение бактерий на поверхности клеток макроорганизма;
- •Инвазию — проникновение бактерий через слизистые и соединительнотканные барьеры макроорганизма в подлежащие ткани;
- •Переход возбудителя к другому хозяину.
- •У Грам– бактерий — пили I и общего типов;
- •Капсульные полисахариды клебсиелл, поверхностные белки, лпс;
- •Гемагглютинины вирусов.
- •Нативные — существующие изначально;
- •Приобретенные — появляются при определенных условиях (Ig, альбумины, фибронектин).
- •Активная подвижность лептоспир, обеспечивающая проникновение в макроорганизм через неповрежденные кожу и слизистые оболочки;
- •Внедрение бледной трепонемы через микротравмы кожи и слизистых.
- •Полисахаридными капсулами s. Pneumoniae, h. Influenzae, t. Pallidum, к. Pneumoniae;
- •Поверностным полисахаридом p. Aeruginosa;
- •Белком a s. Aureus, который связывается с Fc-фрагментом IgG и блокирует его опсонинсвязывающую способность;
- •Ферменты агрессии микрорганизмов:
- •Другие:
- •I. По молекулярной организации экзотоксины делятся на 2 группы:
- •II. По степени связи с бактериальной клеткой экзотоксины делятся на 3 класса:
- •Характеристика бактериальных токсинов
- •Различные клинические формы инфекционных заболеваний, вызываемые разными патогенными штаммами одного вида бактерий, связаны с их способностью продуцировать различные типы токсинов.
- •Активация комплемента по альтернативному пути;
- •Поликлональная стимуляция и пролиферация в-лимфоцитов, синтез Ig m;
- •Сравнительная характеристика бактериальных экзотоксинов и эндотоксинов
- •Генетический контроль факторов патогенности
- •Синдром системного воспалительного ответа
- •Химиопрофилактика и химиотерапия инфекционных заболеваний этапы становления химиотерапии
- •Классификация антимикробных средств
- •Группы химиопрепаратов
- •Антибиотики. Антибиотики
- •Требования к антибиотикам
- •Классификация
- •1. По антимикробному спектру действия:
- •2. По происхождению:
- •3. По типу действия:
- •4. По направленности действия:
- •5. По химическому строению:
- •Классификация и спектр активности пенициллинов
- •Классификация и спектр активности аминогликозидов
Практическое использование изменчивости
Данная способность бактерий может использоваться в следующих целях:
получение аттенуированных вакцинных штаммов;
получение антибиотиков;
изучение механизмов антибиотикорезистентности;
биотехнология (получение диагностических, лечебных и профилактических препаратов с помощью генно-инженерных методов);
разработка биологического оружия (с этой целью отбираются вирулентные штаммы микроорганизмов, резистентные к антимикробным веществам);
изменчивость патогенных микроорганизмов — основная движущая сила в развитии и совершенствовании систем защиты человека от чужеродной генетической информации. Микроорганизмы — важный фактор естественного отбора в человеческой популяции.
Медицинская биотехнология и генная инженерия
Биотехнология — прикладное научное направление, занимающееся созданием биологических продуктов с использованием методов генной инженерии.
Быстрое развитие биотехнология получила во второй половине ХХ в. благодаря развитию науки и экономической выгодности: с помощью микроорганизмов многие вещества получать в тысячи раз дешевле, чем синтезировать химически.
В настоящее время с помощью генно-инженерных методов получают диагностические, лечебные и профилактические препараты, в т. ч. вакцины, антигены, диагностикумы, гормоны (инсулин), антибиотики, иммуномодуляторы, интерфероны, цитокины, моноклональные антитела.
Генная инженерия — направление биотехнологии, позволяющее целенаправленно изменять наследственный материал живых существ.
Открытие, лежащее в основе методов генной инженерии, было сделано В. Арбером в конце 50-х – начале 60-х гг. XX в. Он установил, что бактерии пытаются защитить себя от действия бактериофагов: с помощью ферментов-рестриктаз они разрезают ДНК вирусов, проникших в бактерию, на фрагменты и делают вирус неактивным. Десять лет спустя Г. Боуэр показал, что действие рестриктаз высокоспецифично: они разрезают ДНК в строго определенных местах по одним и тем же основаниям, причем место фрагментации одной цепи смещено по отношению к другой на 4 пары оснований. При этом неровном разрезе возникают два выступающих конца, которые притягиваются друг к другу благодаря наличию водородных мостиков. Поэтому их называют «липкими» концами. Другой фермент — ДНК-лигаза — может, расходуя АТФ, легко вновь соединить липкие концы.
Если с помощью рестриктаз вырезать фрагменты ДНК из разных организмов, то они будут иметь подходящие друг к другу липкие концы, которые в присутствии ДНК-лигазы можно легко соединить. В результате образуются гибридные молекулы из ДНК различных организмов. Таким образом, чужеродная наследственная информация «встраивается» в исходную ДНК.
В качестве векторов для переноса генов в генной инженерии используют плазмиды и бактериофаги.
Метод клонирования заключается в том, что выделенный ген вводится в состав вектора. Затем вектор трансфецируется в быстро размножающуюся, неприхотливую бактерию-хозяина для репликации. Поскольку бактерии делятся очень быстро, то введенная чужеродная ДНК быстро удваивается, т. е. происходит ее клонирование. Путем клонирования любой фрагмент ДНК может быть размножен в бактериях в миллиарды раз, а потом с помощью рестриктаз снова выделен. Так была найдена возможность получения как нужных фрагментов ДНК в больших количествах, так и определенных генов, которые, будучи встроенными в микроорганизмы, направляют синтез новых белков (рис. 77).
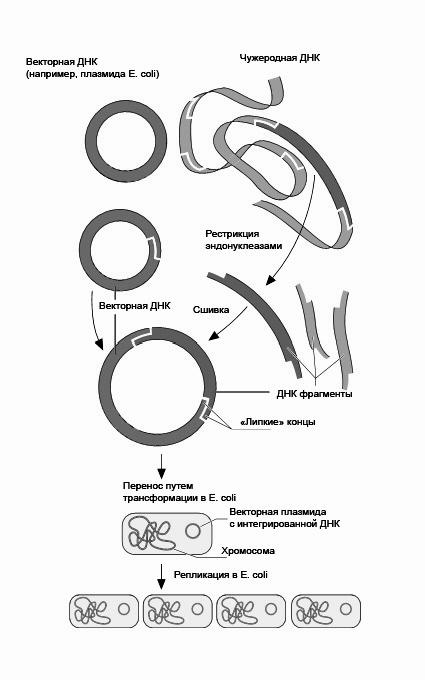
Рис. 77. Клонирование ДНК
Цели генной инженерии:
модификация естественных генов человека, животных, микроорганизмов (удаление генов вирулентности и получение аттенуированных вакцинных штаммов);
синтез новых генов (перенос генов в геном других микроорганизмов) и изучение закономерности экспрессии генов;
получение генно-инженерных продуктов и использование их в клинической практике.
Используемые технологии:
Создание трансгенных организмов с заданными свойствами. Основная проблема — неясность отдаленных последствий применения трансгенных организмов.
Гибридизация клеток и получение моноклональных антител, отличающихся высокой специфичностью действия. Сегодня моноклональные антитела широко используется в диагностических исследованиях (определение иммунофенотипа клеток), начинается их использование с лечебной целью.
Использование рекомбинантных микроорганизмов, продуцирующих гормоны (инсулин, продуцируемый E. coli), вакцины (HBs-антиген, продуцируемый дрожжами-сахаромицетами — вакцина против гепатита В), цитокины (рекомбинантный интерферон, продуцируемый E. coli).
