
- •1 Исходные данные
- •2 .1 Проверка данных химического анализа воды
- •2.2 Выбор технологических процессов очистки воды
- •2.3 Выбор общей технологической схемы очистки воды и определение состава основных сооружений
- •2.4 Выбор вида и определение доз реагентов
- •2.5 Расчет и конструирование основных сооружений станции
- •2.6 Реагентное хозяйство и склады реагентов
- •3. Определение себестоимости очистки воды
- •1 Исходные данные…………………………………………………………...
1 Исходные данные
Исходные данные представлены местоположением объекта проектирования, требуемой производительностью станции очистки воды, данные по качеству природной воды (температура, вкус и запах, цветность, содержание кальция, магния, натрия, калия, сульфатов, хлоридов, бикарбонатов), материал загрузки сооружений очистки. Все данные представлены в задании.
2 .1 Проверка данных химического анализа воды
Проверка данных химического анализа воды может быть выполнена двумя методами: аналитическим и графическим.
Аналитический метод заключается в установлении равенства суммы
катионов и анионов, выраженных в мг-экв/л
∑К+=∑А- (2.1) ∑К+= Ca2++Mg2++Na+( K+)=3,3+3+1,3=7,6 мг-экв/л
∑A-=HCO3-+Cl-+SO4-=1,2+3,4+3=7,6 мг-экв/л
7,6 мг-экв/л=7,6 мг-экв/л
Рисунок 2.1. Графический метод проверки данных анализа
Проверка данных анализа графическим методом выполняется в виде
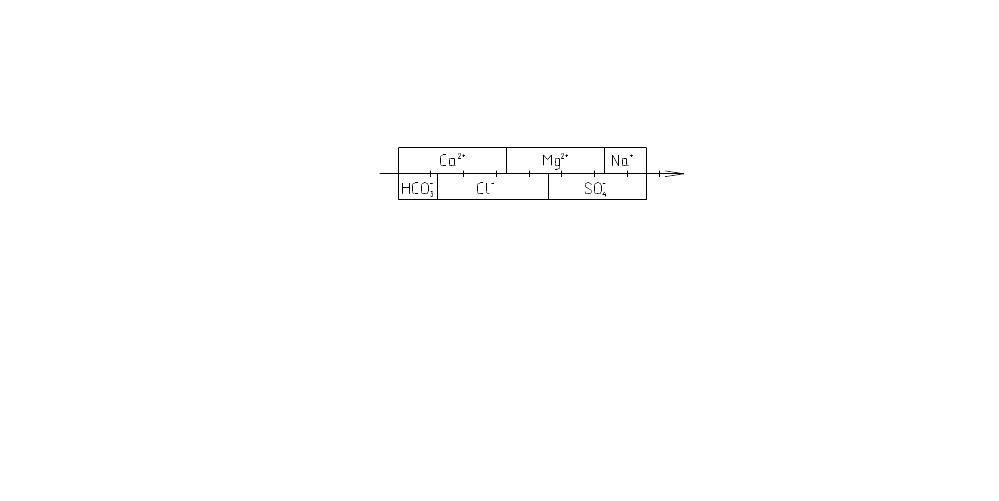 двух
параллельных соприкасающихся полос,
на которых откладывается количество
мг-экв/л катионов и анионов. Графический
метод представлен на рисунке 2.1.
двух
параллельных соприкасающихся полос,
на которых откладывается количество
мг-экв/л катионов и анионов. Графический
метод представлен на рисунке 2.1.
3. Определение общей жесткости воды выполняется по формуле
Жо= Ca2++ Mg2+, (2.2)
где Ca2+ и Mg2+ - содержание катионов кальция и магния, выраженных в мг-экв/л
Жо=3,3+3=6,3 мг-экв/л
4. Карбонатная жесткость (щелочность воды) рассчитывается по формуле
Жк=Щ=[ HCO3-], (2.3)
где HCO3- - содержание в воде карбонатных ионов, выраженных в мг-экв/л
Жк=1,2 мг-экв/л
5. Общее солесодержание воды в мг/л определяется по формуле
P=∑[ Ca2++Mg2++Na+( K+)+ HCO3-+Cl-+SO4-] (2.4)
Перевод концентраций химических веществ, выраженных в эквивалентных единицах мг-экв/л, в объёмные, выраженные в мг/л, осуществляется в по формуле
M= C· Э, (2.5)
где С – концентрация вещества, мг-экв/л,
Э – эквивалентный вес химических веществ, мг/(мг-экв)
Данные перевода представлены в таблице 1.
Таблица 1. Определение концентрации химических веществ, выраженных в мг/л
Наименование |
С, мг-экв/л |
Э, мг/(мг-экв) |
М, мг/л |
Ca2+ |
3,3 |
20,1 |
67,32 |
Mg2+ |
3 |
12,1 |
36,3 |
Na+( K+) |
1,3 |
23,0 |
29,9 |
HCO3- |
1,2 |
61,02 |
73,22 |
Cl- |
3,4 |
35,46 |
120,56 |
SO4- |
3 |
48,01 |
144,03 |
Подставляя полученные данные в формулу 2.4
P=67,32+36,3+29,9+73,22+120,56+144,03=471,33 мг/л
