
- •Готовимся к федеральному интернет-экзамену
- •Тобольск
- •Оглавление
- •Введение
- •Форма и структура экзаменационной работы
- •Блок «общая и неорганическая химия» Тема заданий : «Строение атома и периодическая система».
- •Тема заданий : «Химическая связь и строение вещества»
- •Блок «аналитическая химия» Тема заданий: «Теоретические основы аналитической химии»
- •Блок «физическая химия» Тема заданий: «окислительно-восстановительные и электрохимические процессы»
- •Тема заданий: «Химическая кинетика и катализ».
- •Блок «коллоидная химия»
- •Блок «высокомолекулярные соединения» Тема заданий: «Методы получения полимеров»
- •Тема заданий: «Органические и неорганические полимеры»
- •Тема заданий: «Строение и свойства полимеров»
- •Заключение рекомендуемая литература
- •Периодическая система
- •Дисперсные системы
- •Качественные реакции:
- •626150, Г. Тобольск, ул. Знаменского, 58.
Заключение рекомендуемая литература
1.Коровин И.В. Общая химия. М.;2000.
2.Глинка Н.Л. общая химия. Л.; 1986.
3.Общая химия./Под редакцией Е.М.Соколовской, Л.С.Гузея. М.;МГУ, 1989.
4.Ахметов Н.С. общая и неорганическая химия. М.;1988.
5.
ПРИЛОЖЕНИЕ

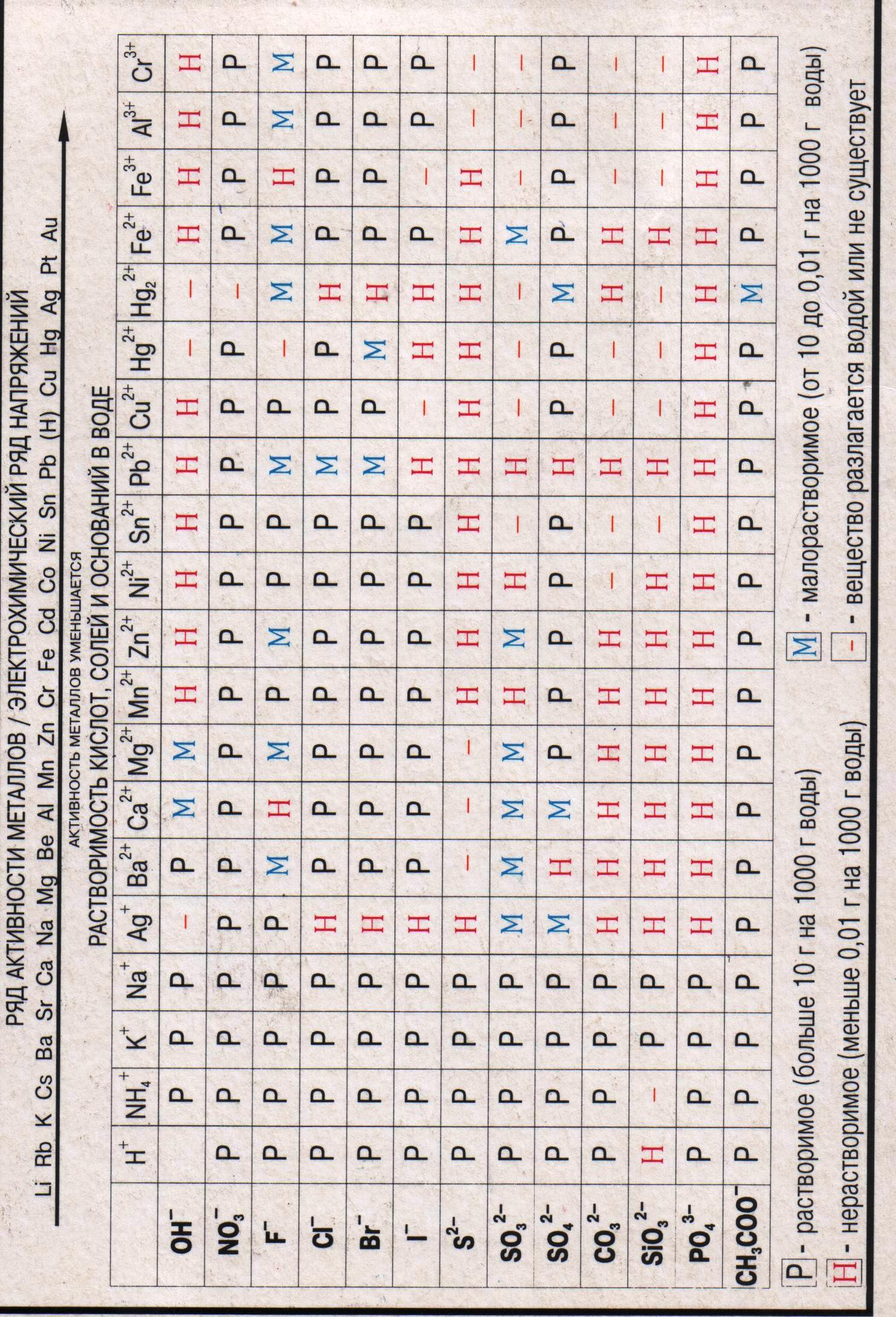
Периодическая система
Э |
|||||
К ислотные свойства возрастают |
|||||
С ила оснований убывает |
|||||
М еталлические свойства ослабевают |
|||||
Э |
М |
Р |
К ислотные свойства возрастают |
С ила кислот возрастает |
О |
Дисперсные системы
Тип дисперсной системы |
Фазовое состояние |
Примеры систем |
|
Дисперсионной среды |
Дисперсной фазы |
||
аэрозоли |
Г |
ж |
Туман, облака |
г |
т |
Пыль, дым |
|
лиозоли |
Ж |
Г |
пены |
ж |
ж |
Эмульсии (молоко) |
|
ж |
т |
Суспензии (краски) |
|
Твёрдые золи |
т |
г |
Пористые тела (хлеб) |
т |
ж |
Самоцветные камни |
|
т |
т |
Металлические и солевые сплавы |
|
Качественные реакции:
Распознаваемые ионы и вещества |
Реактивы |
Признаки |
1.Катионы: H+
|
Индикаторы |
Лакмус красный Метилоранж красный Фенолфталеин бесцветный |
NH4+
|
Щелочь при t
|
Бесцветный газ с резким запахом, вызывающий посинение лакмуса |
Ag+ |
HCl и Cl-(cоль) |
Белый творожистый осадок |
Na+ |
Пламя |
Желтое |
K+ |
Пламя |
Фиолетовое |
Ca2+
|
Пламя
|
Кирпично-красное
|
Ba2+ |
H2SO4 и SO4- |
Белый осадок, нерастворимый в воде и кислотах |
Cu2+ |
Щелочь |
Голубой осадок |
Zn2+ |
Щелочь |
Бесцветный осадок, растворимый в щелочи |
Fe2+ |
Щелочь |
Бледно-зеленый осадок |
Fe2+ |
Красная кровяная соль |
Синий осадок |
Fe3+ |
Щелочь CNS (соль) Желтая кровяная соль |
Бурый осадок Кроваво-красное окрашивание Синий осадок |
Al3+ |
Щелочь |
Белый осадок, растворимый в избытке щелочи |
Cr3+
|
Щелочь
|
Серо-зеленый осадок, растворимый в избытке щелочи |
2.Анионы: OH-
|
Индикаторы
|
Лакмус синий Метилоранж желтый Фенолфталеин малиновый |
Cl-
|
AgNO3
|
Белый творожистый осадок, нерастворимый в кислотах |
NO3-
|
H2SO4 и Cu при нагревании |
Бурый газ с запахом |
S2- |
Pb2+ (соль) |
Черный осадок |
SO42- |
Ba2+ (соль) |
Белый осадок |
SO32-
|
Сильные кислоты
|
Бесцветный газ с резким запахом, помутнение известковой воды |
CO32-
|
Сильные кислоты
|
Бесцветный газ без запаха, помутнение известковой воды |
SiO32- |
Сильные кислоты |
Студенистый осадок |
PO43-
|
AgNO3
|
Желтый осадок, растворимый в сильных кислотах |
3.Вещества: I2 |
Крахмал |
Синее окрашивание |
Cl2
|
Иодкрахмальная бумажка |
Синее окрашивание
|
Cu2+ |
Аммиак |
Ярко-синего раствора |
Al2(SO4)3 |
Метиловый оранжевый |
Розовый цвет |
Na2CO3 |
Лакмус |
Синий лакмус |
Cu2+ |
Сероводород |
Черный цвет (осадок) |
Д

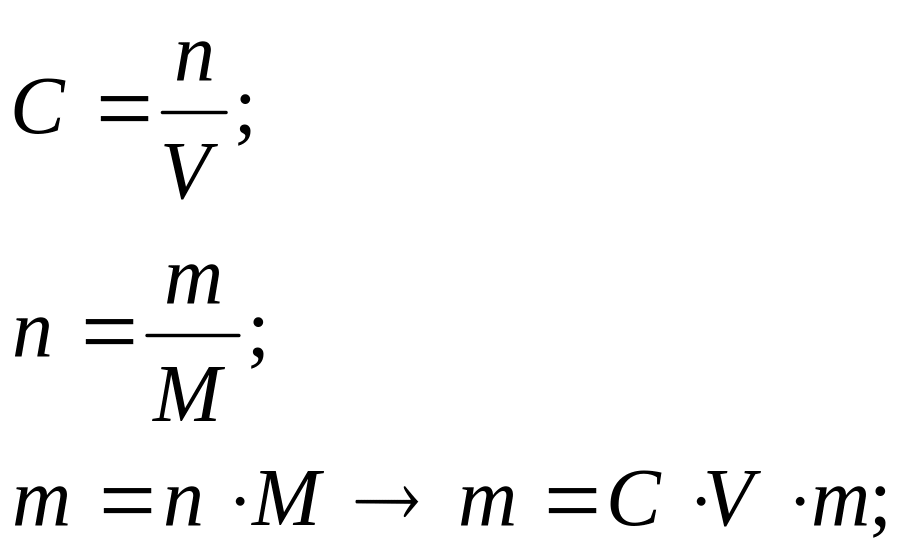



 ано:
Дано:
Дано: Дано:
ано:
Дано:
Дано: Дано:
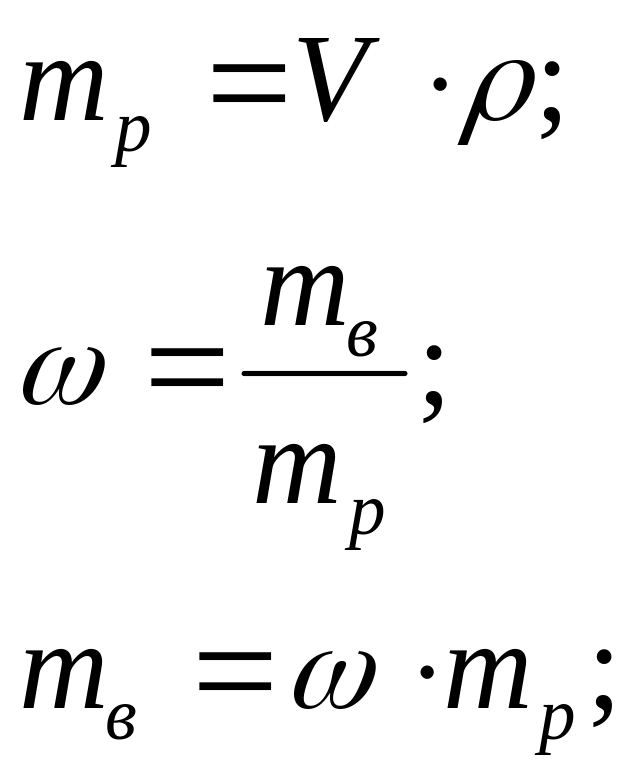

![]()
![]()


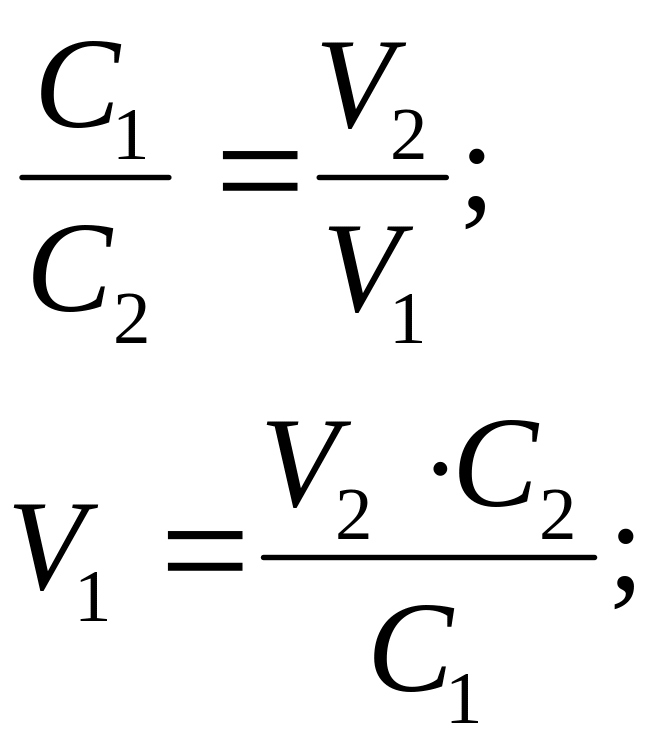
V V=л;
ρ С=м;
ω
![]()

![]()

![]()

![]()





Д
ω
![]()
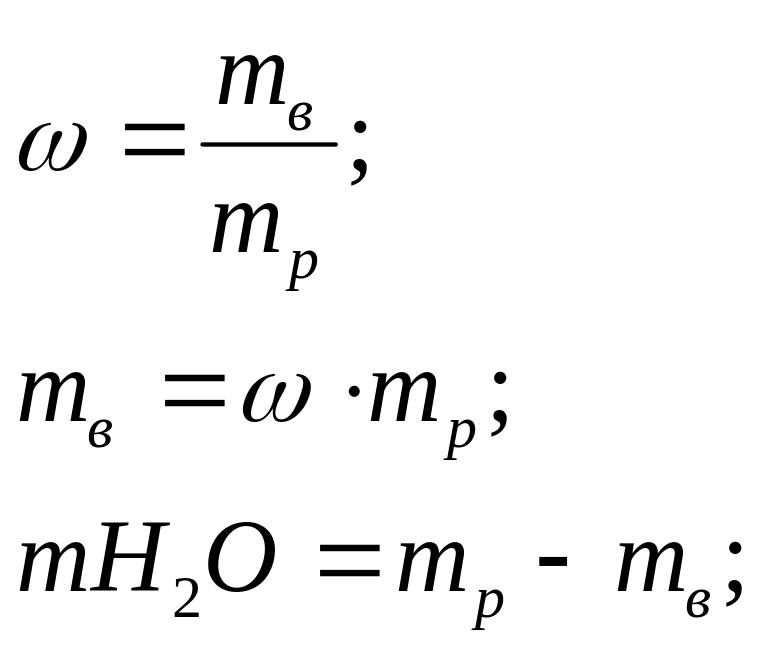
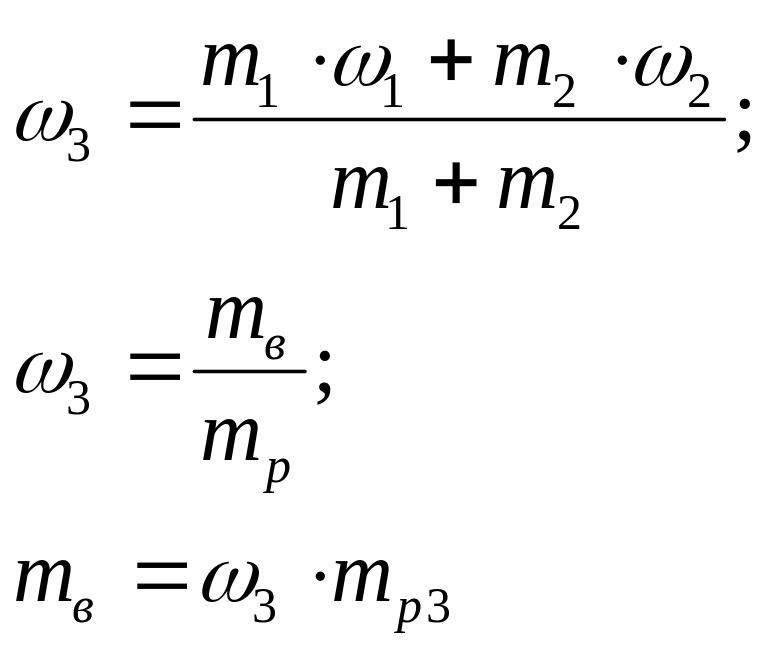

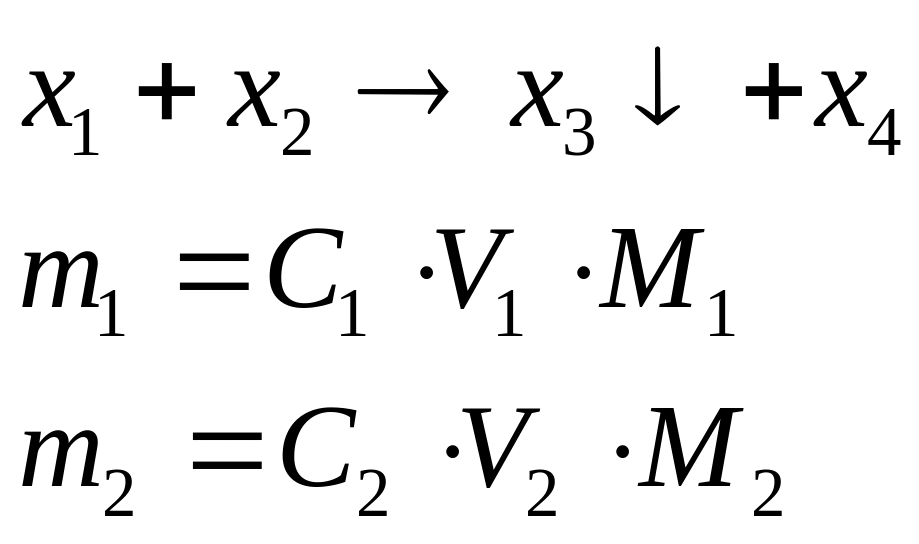
 ано:
Дано: Дано: Дано:
ано:
Дано: Дано: Дано:
![]()
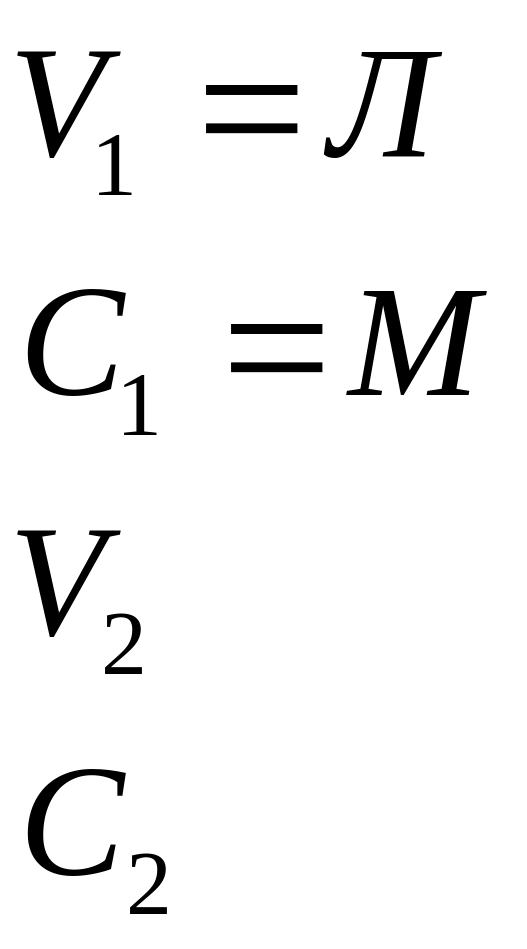
![]()
![]()

![]()
решаем по меньшей массе
![]()
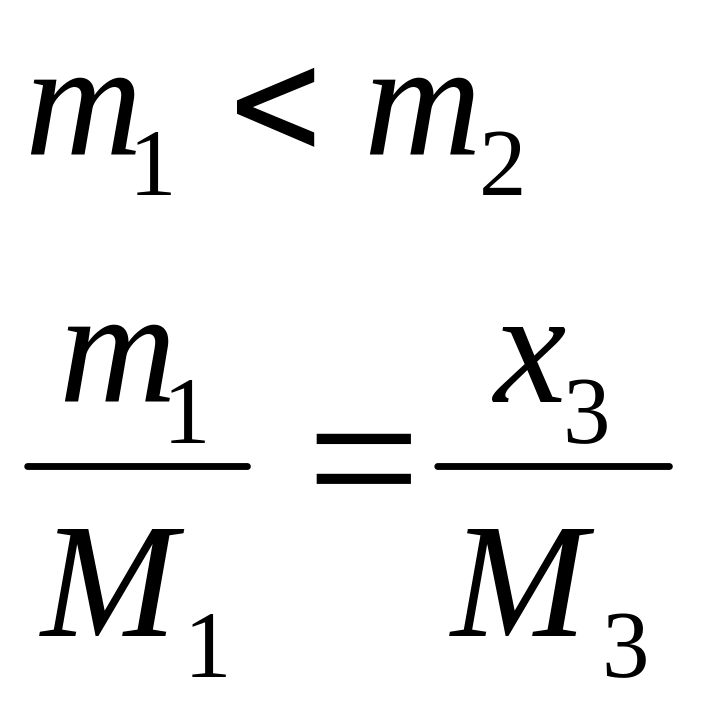




Д ано:
ано:
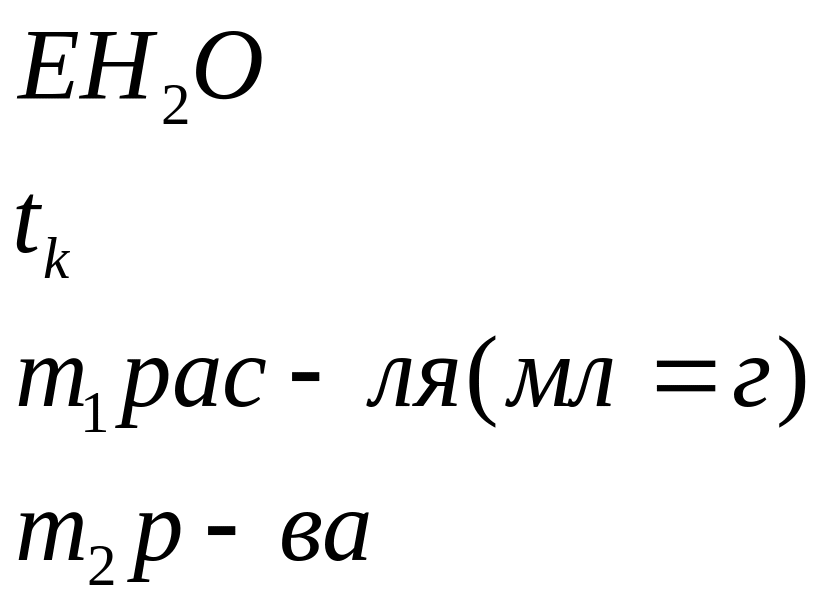


 mостатка
-?
mостатка
-?
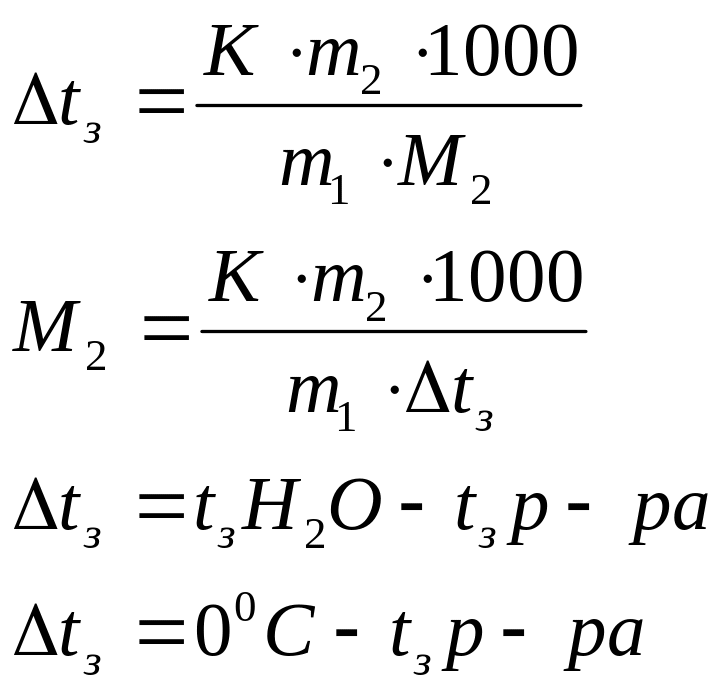
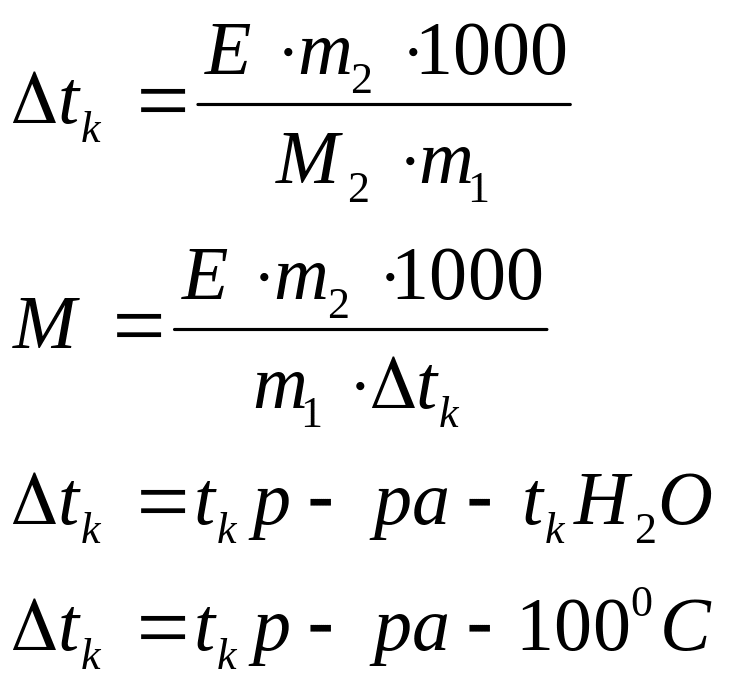
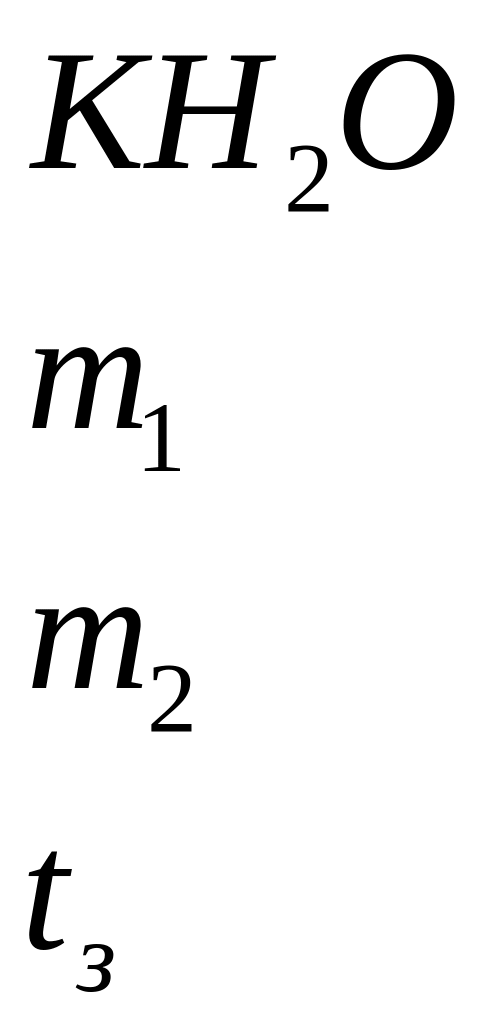
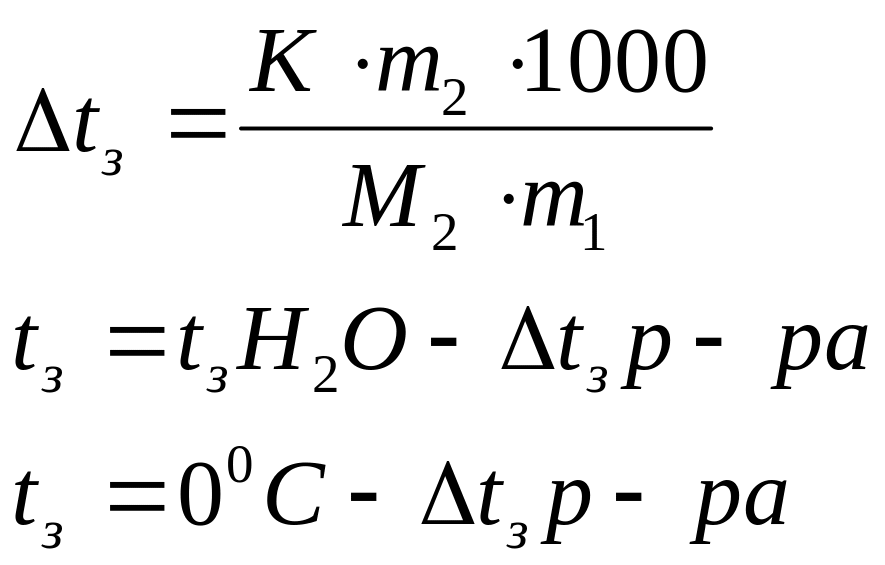

Дано:
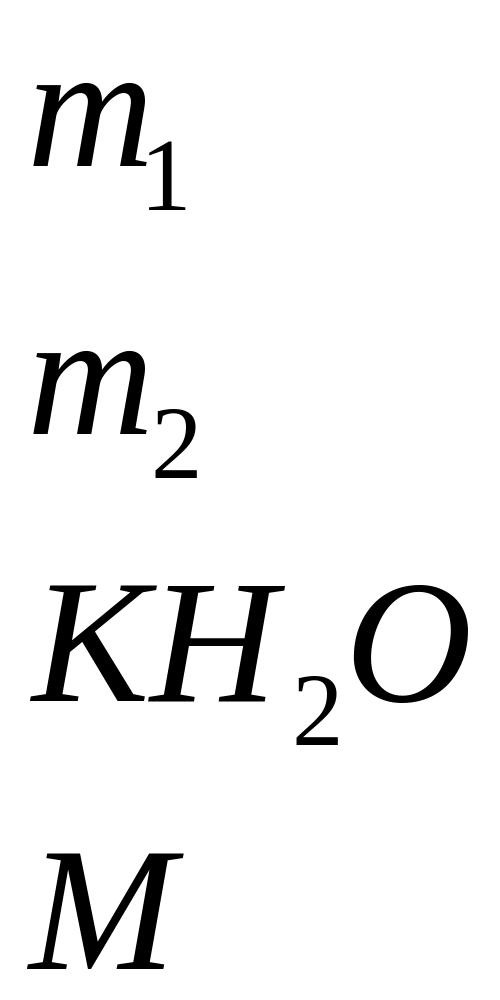
![]()

![]()
Д


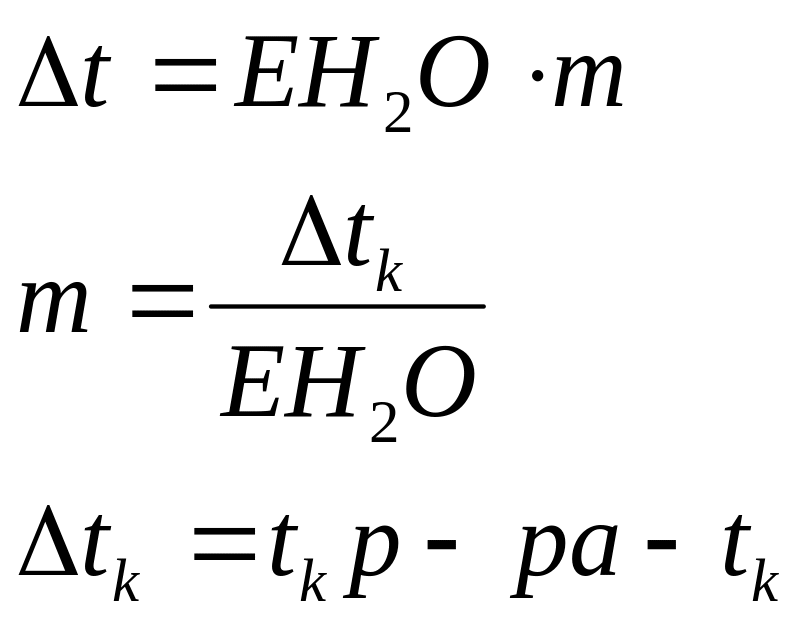

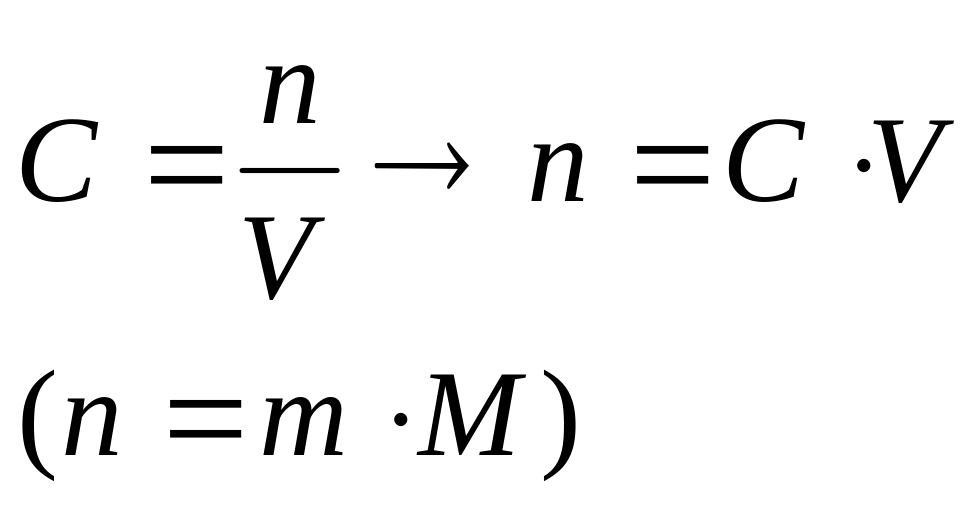

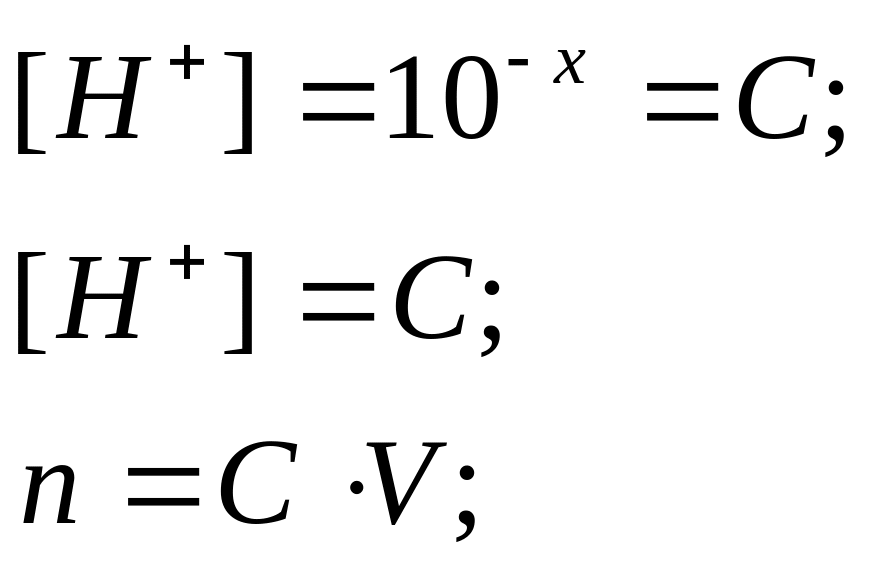
 ано: Дано: Дано: Дано:
ано: Дано: Дано: Дано:
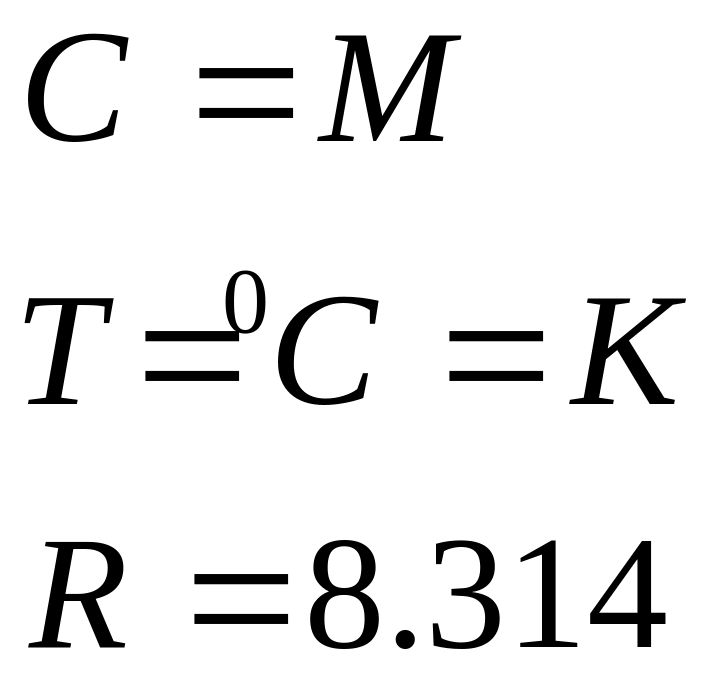
![]()
![]()
осматическое С=М
n-?
mконцентр-? n-?
π- ?



Д
![]()
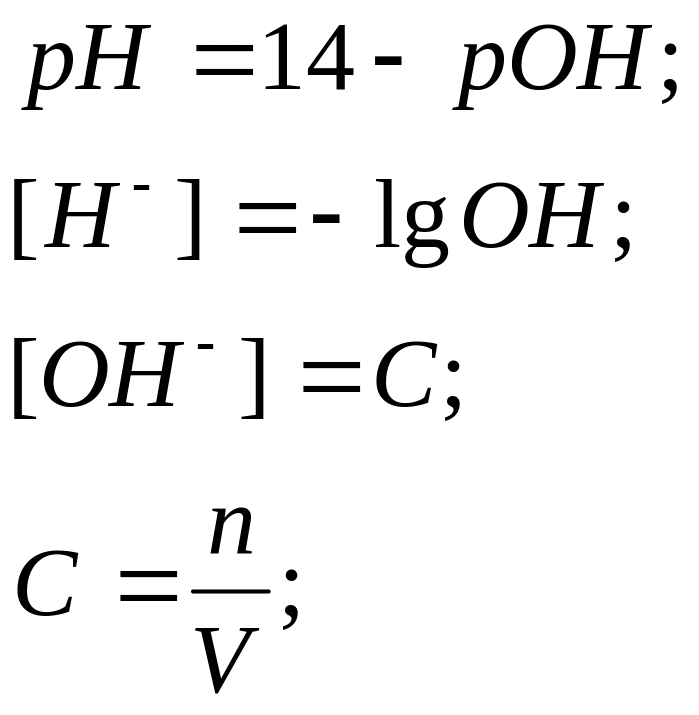
![]()
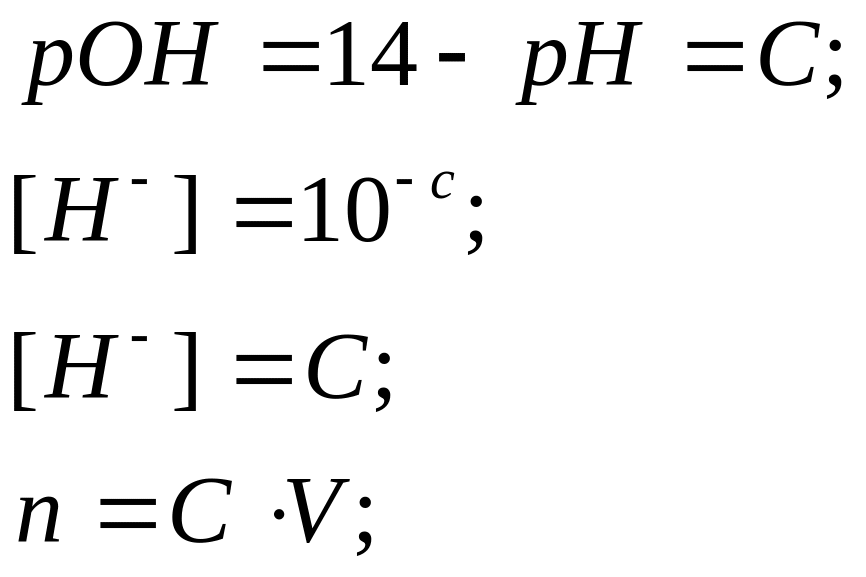
pH-?
pH-?
n-?![]()

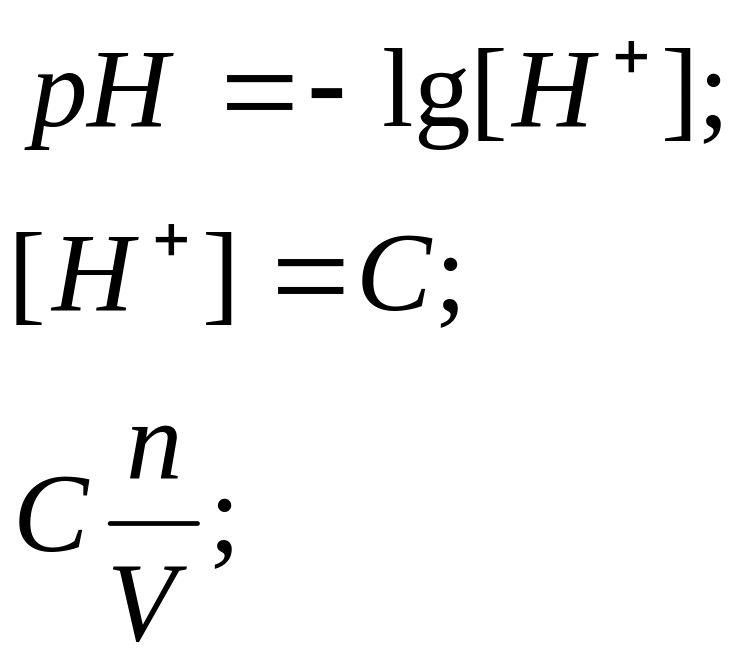
Учебно-методическое пособие
АВТОРЫ
ГОТОВИМСЯ К ФЕДЕРАЛЬНОМУ ИНТЕРНЕТ-ЭКЗАМЕНУ
Технический редактор_____________________
Компьютерная верстка____________________
Лицензия на издательскую деятельность
ЛР №040287 от 25 июля 1997 года
Отпечатано с оригинал-макета. Подписано в печать 2008 г.
Формат 60 Х 84 1/16 Усл.печ.л. 10,7 Тираж 100 экз. Заказ №_____
Отпечатано в минитипографии
Тобольского государственного педагогического института

 лектроотрицательность
увеличивается
лектроотрицательность
увеличивается лектроотрицательность
увеличивается
лектроотрицательность
увеличивается еталлические
свойства усиливаются
еталлические
свойства усиливаются адиус
атомов увеличивается
адиус
атомов увеличивается кислительная
способность уменьшается
кислительная
способность уменьшается