
- •Свойства химических элементов, а также образованных ими веществ находятся в периодической зависимости от заряда ядра атома.
- •Химические свойства
- •Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •Окисление
- •Исчерпывающее окисление
- •Восстановление (гидрирование)
- •Озонирование
- •Химические свойства
- •Нахождение в природе
- •Получение
- •Номенклатура алкинов
- •Изомерия
- •Химические свойства
- •1. Реакции присоединения
- •II Кислотные свойства
- •Классификация неорганических веществ
- •Химические свойства
- •Химические свойства
- •Химические свойства спиртов.
- •Номенклатура спиртов [править]Систематическая номенклатура
- •[Править]Рациональная и тривиальная номенклатура
- •Физические свойства спиртов.
- •Основные положения теории химического строения а.М. Бутлерова
- •Положение металлов в периодической таблице
- •Химические свойства
- •3 Реакция полимеризации
- •Номенклатура
- •Изомерия
- •[Править]Гомологический ряд
- •Химические свойства карбоновых кислот.
- •Химические свойства спиртов.
- •Номенклатура спиртов [править]Систематическая номенклатура
- •[Править]Рациональная и тривиальная номенклатура
- •Химические свойства
- •Галогенирование
- •Гидрогалогенирование
- •Гидратация
- •Окисление
- •Исчерпывающее окисление
- •Восстановление (гидрирование)
- •Озонирование
- •Номенклатура
- •Изомерия
- •Гомологический ряд
Положение металлов в периодической таблице
Если в периодической таблице элементов Д.И.Менделеева провести диагональ от бериллия к астату, то слева внизу по диагонали будут находиться элементы-металлы (к ним же относятся элементы побочных подгрупп), а справа вверху – элементы-неметаллы. Элементы, расположенные вблизи диагонали (Be, Al, Ti, Ge, Nb, Sb и др.), обладают двойственным характером.
К элементам - металлам относятся s - элементы I и II групп, все d- и f - элементы, а также p- элементы главных подгрупп: III (кроме бора), IV (Ge, Sn, Pb), V (Sb,Bi) и VI (Po). Наиболее типичные элементы – металлы расположены в начале периодов (начиная со второго).
№2.Альдегиды,гомологический ряд, номенклатура, химические свойства.
Альдегиды (от лат. alcohol dehydrogenatum — спирт, лишённый водорода) — класс органических соединений, содержащих карбонильную группу (С=О) с однималкильным или арильным заместителем.
Альдегиды и кетоны весьма схожи, различие заключается в том, что последние имеют при карбонильной группе два заместителя. Поляризация двойной связи «углерод-кислород» по принципу мезомерного сопряжения позволяет записать следующие резонансные структуры:
![]()
Подобное разделение зарядов подтверждается физическими методами исследования и во многом определяет реакционную способность альдегидов, как выраженных электрофилов. В общем случае химические свойства альдегидов аналогичны кетонам, однако альдегиды проявляют бо́льшую активность, что связано с большей поляризацией связи. Кроме того, для альдегидов характерны реакции, не характерные для кетонов, например гидратация в водном растворе: у метаналя в связи с ещё большей поляризацией связи — полная, а у других альдегидов — частичная:
![]()
Простейшие альдегиды имеют резкий характерный запах (например, бензальдегид — запах миндаля).
Под действием гидроксиламина превращаются в оксимы:
![]()
Химические свойства
Высокая реакционноспособность связана с наличием высокополярной связи С=О. Проявляют свойства органических оснований.
Восстановление. Альдегиды способны к восстановлению, основной продукт восстановления — первичные спирты.
![]()
Присоединение синильной кислоты. Используется для удлинения углеродной цепи.
![]()
Присоединение гидросульфита натрия. Используется для выделения альдегидов из растворов.
![]()
Присоединение спиртов с образованием полуацеталей (при избытке спирта и хлороводороде образуются ацетали)
2 Окисление. Альдегиды легко (значительно легче, чем спирты) окисляются в соответствующие карбоновые кислоты.
Реакция «серебряного зеркала».
![]()
Реакция «медного зеркала». Окислителем здесь выступает свежеприготовленный гидроксид меди(II). Образуется кирпично-красный осадок оксида Cu(I)
![]()
3 Реакция полимеризации
Формальдегид образует параформальдегид (n=8-100) при длительном стоянии или испарении.
![]()
При циклизации образуются триоксан (n = 3) и тетраоксиметилен (n = 4).
4 Реакция поликонденсации При нагревании альдегида с фенолом в кислой или щелочной среде образуются фенолформальдегидные смолы.
Номенклатура:
CH2O - формальдегид
CH3-CHO - ацетальдегид
CH3-CH2-CHO - пропиональдегид
CH3-CH2-CH2-CHO - бутиральдегид
(CH3)2-CH-CHO - изобутиральдегид
CH3-(CH2)3-CHO - валеральдегид
(CH3)2CH-CH2-CHO - изовалеральдегид
CH2=CH-CHO - акролеин (акрилальдегид)
CH3-CH=CH-CHO - кротональдегид
С6H5-CHO - бензальдегид
ГОМОЛОГИЧЕСКИЙ РЯД:
Простейший альдегид, называемый муравьиным альдегидом или формальдегидом, содержит альдегидную группу, связанную с атомом водорода, и имеет строение
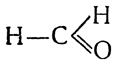 или
сокращенно
,
Н—СНО.
В
остальных альдегидах предельного
ряда
место
одного атома водорода занимает алкил:
СnС2n+1—СНО.
или
сокращенно
,
Н—СНО.
В
остальных альдегидах предельного
ряда
место
одного атома водорода занимает алкил:
СnС2n+1—СНО.
Альдегиды можно также рассматривать как вещества, происшедшие от замещения в парафиновых углеводородах атома водорода на альдегидную группу, т. е. как однозамещенные производные углеводородов гомологического ряда метана. Следовательно, здесь гомология и изомерия те же, что и для других однозамещенных производных предельных углеводородов.
Названия альдегидов производятся от тривиальных названий кислот с тем же числом атомов углерода в молекуле. Так, альдегид СН3—СНО называется уксусным альдегидом или ацетальдегидом, СН3СН2—СНО — пропионовым альдегидом, СН3СН2СН2—СНО — нормальным масляным альдегидом или бутиральдегидом, (СН3)2СН—СНО — изомасляным альдегидом, альдегиды С4Н9—СНО — валериановыми альдегидами и т. д.
По женевской номенклатуре, названия альдегидов производятся от названий углеводородов, имеющих то же число углеродных атомов, с присоединением к окончанию ан слога аль, например метаналь Н—СНО, этаналь СН3—СНО, 2-метилпропаналь СН3СН(СН3)—СНО
Н—СНО. В остальных альдегидах предельного ряда место одного атома водорода занимает алкил: СnС2n+1—СНО.
Билет№9.
№1.Оксиды. Классификация, химические свойства.
Оксиды — сложные вещества, состоящие из двух элементов, один из которых кислород.
Оксиды делят на кислотные, осно́вные, амфотерные и несолеобразующие (безразличные).
Кислотным оксидам соответствуют кислоты. Кислотными свойствами обладают большинство оксидов неметаллов и оксиды металлов в высшей степени окисления, например CrO3.
Многие кислотные оксиды реагируют с водой с образованием кислот. Например, оксид серы (IV), или серни́стый газ, реагирует с водой с образованием серни́стой кислоты:
SO2 + H2O = H2SO3
Кислотные оксиды реагируют со щелочами с образованием соли и воды. Например, оксид углерода (IV), или углекислый газ, реагирует с гидроксидом натрия с образованием карбоната натрия (соды):
CO2 + 2NaOH = Na2CO3 + H2O
Осно́вным оксидам соответствуют основания. К осно́вным относятся оксиды щелочных металлов (главная подгруппа I группы),
магния и щелочноземельных (главная подгруппа II группы, начиная с кальция), оксиды металлов побочных подгрупп в низшей степени окисления (+1+2).
Оксиды щелочных и щелочноземельных металлов реагируют с водой с образованием оснований. Так, оксид кальция реагирует с водой, получается гидроксид кальция:
CaO + H2O = Ca(OH)2
Основные оксиды реагируют с кислотами с образованием соли и воды. Оксид кальция реагирует с соляной кислотой, получается хлорид кальция:
CaO + 2HCl = CaCl2 + H2O
Амфотерные оксиды реагируют и с кислотами, и со щелочами. Так, оксид цинка реагирует с соляной кислотой, получается хлорид цинка:
ZnO + 2HCl = ZnCl2 + H2O
Оксид цинка взаимодействует и с гидроксидом натрия с образованием цинката натрия:
ZnO + 2NaOH = Na2ZnO2 + H2O
С водой амфотерные оксиды не взаимодействуют. Поэтому оксидная пленка цинка и алюминия защищает эти металлы от коррозии.
Несолеобразующим (безразличным) оксидам не соответствуют гидроксиды, они не реагируют с водой. Несолеобразующие оксиды не реагируют ни с кислотами, ни со щелочами. К ним относится оксид азота (II) NO.
Иногда к несолеобразующим относят угарный газ, но это неудачный пример, т.к. этот оксид реагирует с гидроксидом натрия с образованием соли:
CO + NaOH = HCOONa (эта реакция не для запоминания! Изучается в 10–11 классах)
№2.Предельные одноосновные карбоновые кислоты. Гомологический ряд, номенклатура, химические свойства.
Одноосновные предельные карбоновые кислоты (одноосновные насыщенные карбоновые кислоты) — карбоновые кислоты, в которых насыщенный углеводородный радикал соединен с одной карбоксильной группой -COOH. Все они имеют общую формулу СnH2n+1COOH
