
- •Введение
- •Лабораторная работа № 1. Выбор состава и приготовление буферного раствора с заданным значением рН
- •Приборы и реактивы.
- •Выполнение работы
- •I. Выбрать реактивы для приготовления буферного раствора.
- •II. Рассчитать объемы реактивов для приготовления буферного раствора.
- •III. Приготовить буферный раствор и определить его рН
- •IV. Определить буферную емкость
- •Протокол лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Определение концентрации ионов меди методом прямой потенциометрии
- •Оборудование и реактивы
- •Выполнение работы
- •I. Приготовить серию контрольных растворов с содержанием определяемого иона 101, 102, 103, 104 моль/кг методом последовательного разведения.
- •II. Получить градуировочную зависимость и измерить эдс пробы при помощи ионоселективного электрода.
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3. Определение концентрации ионов I– и Cl– методом потенциометрического титрования
- •Оборудование и реактивы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 4. Определение содержания кислоты методом потенциометрического титрования
- •Оборудование и реактивы:
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 6. Определение концентрации кислоты методом кондуктометрического титрования.
- •Оборудование и реактивы
- •Выполнение работы
- •Протокол лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 7. Анализ смеси кислот и солей слабых оснований методом кондуктометрического титрования.
- •Оборудование и реактивы
- •Выполнение работы
- •Протокол лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 8. Разделение меди и цинка на катионите
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 9. Экстракция цветных металлов карбоновыми кислотами
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 10. Определение концентрации железа (III) фотометрическим методом с роданидом калия
- •Оборудование и реактивы
- •Выполнение работы
- •I. Приготовление рабочего раствора соли железа.
- •II. Получение градуировочной зависимости
- •III. Проведение анализа пробы
- •Протокол лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 11. Определение концентрации никеля фотометрическим методом с диметилглиоксимом
- •I. Приготовление рабочего раствора соли никеля
- •II. Получение градуировочной зависимости
- •III. Проведение анализа пробы
- •Протокол лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 12. Определение сульфат-иона турбидиметрическим методом
- •Оборудование и реактивы.
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 13. Фотометрическое определение цветности воды
- •Оборудование и реактивы
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная Работа № 14. Получение спектра поглощения и определение аналитической длины волны
- •Оборудование и реактивы.
- •Выполнение работы
- •1. Приготовить рабочий раствор соли железа:
- •2. Приготовить раствор роданидного комплекса железа для получения спектра:
- •3. Приготовить раствор сравнения для получения спектра:
- •4. Получение спектра поглощения роданидного комплекса железа
- •5. Получение спектра поглощения раствора сульфата никеля
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Содержание
Содержание протокола лабораторной работы
Название экстрагента:
Концентрация экстрагента:
Растворитель:
Название соли металла:
Химическая формула соли металла:
Концентрация раствора щелочи (NaOH) СNaOH = _________
Концентрация раствора трилона Б СТ = ___________
Объем аликвоты, взятый для анализа Vа = _______мл.
Таблица экспериментальных данных
№ п/п |
VNaOH, мл |
рН |
V трилона Б, мл |
|
V1 |
V2 |
|||
исходный |
нет |
нет |
|
|
1 |
1,0 |
|
|
|
2 |
1,5 |
|
|
|
3 |
2,0 |
|
|
|
4 |
2,5 |
|
|
|
Обработка результатов эксперимента
1. Рассчитать исходную и равновесные концентрации металла (2+) по уравнению:
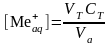 ,
,
где VT и СТ – объем, мл и концентрация, моль/л трилона Б, Va – объем аликвоты, мл.
2. Вычислить концентрацию металла (2+) в органической фазе по уравнению:
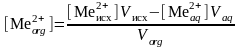 ,
,
где
 и Vисх
концентрация, моль/л, и объем, мл,
исходной соли металла, взятой для
экстракции; Vaq – объем
водной фазы, мл, Vaq = Vисх
+ VNaOH; Vorg – объем
органической фазы, мл.
и Vисх
концентрация, моль/л, и объем, мл,
исходной соли металла, взятой для
экстракции; Vaq – объем
водной фазы, мл, Vaq = Vисх
+ VNaOH; Vorg – объем
органической фазы, мл.
3. Рассчитать коэффициент распределения
 .
.
4. Заполнить таблицу:
№ п/п |
VNaOH, мл |
рН |
VТрБ, мл (средний по двум измерениям) |
|
|
DMe |
lgDMe |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
5. Построить график зависимости lgDMe = f(pH).
6. По графику определить коэффициенты K (константу равновесия) и z уравнения зависимости логарифма коэффициента распределения от рН: lgD = lgK + zpH
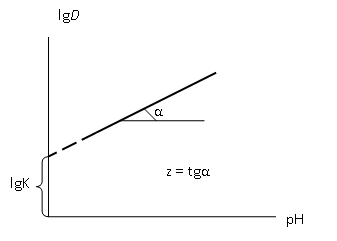
7. Сравнить полученную величину z с зарядом иона и сделать вывод о справедливости принятой модели.
8. Сравнить значения lgK для других металлов и сделать вывод о сравнительной экстрагируемости катионов металлов нафтеновыми кислотами.
Содержание отчета по лабораторной работе
1. Название работы.
2. Цель работы.
3. Ход эксперимента.
4. Экспериментальные данные (см. протокол к лабораторной работе).
5. Обработка экспериментальных данных.
6. Вывод.
Лабораторная работа № 10. Определение концентрации железа (III) фотометрическим методом с роданидом калия
Цель работы. Фотометрическое определение концентрации вещества в растворе по измеренному значению оптической плотности при помощи калибровочного графика, построенного по серии стандартных растворов.
Сущность работы. Ион железа (III) с ионами тиоцианата, образует комплексное соединение кроваво-красного цвета. Раствор бледнеет вследствие восстановления ионов железа ионами роданида. Поэтому фотометрировать раствор необходимо сразу же после приготовления. Раствор окрашенного комплекса имеет максимум поглощения при длине волны 480 нм.

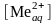 ,
моль/л
,
моль/л ,
моль/л
,
моль/л