
- •8 Класс
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •9 Класс
- •Решение
- •Уравнения реакций (по 0,5 балла) - 5 баллов Итого 10 баллов
- •Решение
- •Итого – 10 баллов
- •Решение
- •Решение
- •Итого – 10 баллов
- •Итого – 10 баллов
- •Решение
- •Решение
- •Уравнение горения аммиака – 2 балла
- •Нахождение доли аммиака с пояснением и расчетом – 6 баллов
- •Итого – 10 баллов
- •10 Класс
- •Решение
- •Решение
- •Решение
- •Решение
- •11 Класс
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение:
Решение
Легкая дегидратация II под действием кислоты указывает на то, что это – третичный спирт. Образовавшийся алкен при озонировании образует ацетон – важный растворитель.
(CH3)2C(OH)CH2CH3
![]() (CH3)2C=CHCH3
(CH3)2C=CHCH3
II III
(CH3)2C=CH2CH3
![]() (CH3)2C=О
+ СH3CHO
+ H2O2
(CH3)2C=О
+ СH3CHO
+ H2O2
III IV V
Реакции гидролиза в кислой и щелочной средах:
(CH3)3CCH2OSO3K + Н2О = (CH3)3CCH2OН + КНSO4 (кислота – катализатор)
(CH3)3CCH2OSO3K + КОН + = (CH3)2C(ОН)CH3 + К2SO4
Зависимость lgkнабл от рН выражается графиком:
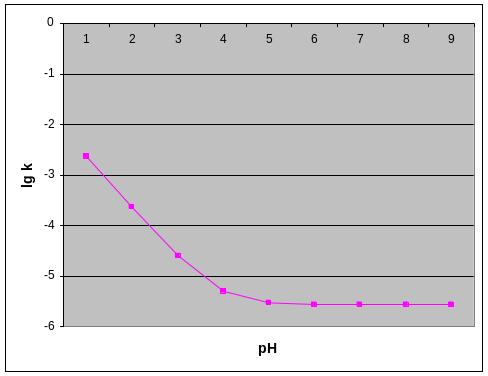
Видно, что график состоит из двух прямолинейных отрезков с некоторым переходным участком. Причем в кислой области график является рН-зависимым, то есть скорость реакции линейно зависит от сН+. Таким образом, в щелочной среде скорость реакции описывается выражением v = kcI, а в кислой – выражением v = kcIсН+. Иными словами, при переходе из кислой в щелочную среду меняется общий порядок реакции и происходит смена механизма гидролиза.
При рН = 5 реализуются оба механизма гидролиза. Если значение рН поддерживается постоянным, то в кислой среде реакция имеет псевдопервый порядок и значение k = 2,3·10–1·сН+ = 2,3·10–6 с–1.
В этом случае
![]() ,
то есть при рН 5 продукт содержит 46%
неопентанола и 54% трет-пентанола.
,
то есть при рН 5 продукт содержит 46%
неопентанола и 54% трет-пентанола.
Ускорение гидролиза алкилсульфатов в присутствии бактерий, несомненно, связано с ферментативными процессами. Действительно, многие бактерии содержат фермент сульфатазу, которая увеличивает скорость гидролиза более чем на 20 порядков.
Разбалловка:
За определение вещества II 2 балла
За реакции по: 4×0,5 балла: всего 2 балла
За построение графика 2 балла
За объяснение зависимости lgk – pH 2 балла
За расчет отношения спиртов 1 балл
За объяснение роли бактерий 1 балл
Итого: 10 баллов
№6
В рамках программы поиска интересных для парфюмерной промышленности соединений был синтезирован о-эвгенол (F) – изомер природного эвгенола. Синтез был осуществлен по схеме:

Вещества A, B, D, F дают характерное окрашивание при взаимодействии с раствором FeCl3, вещества С и Е – нет. Соединения Е и F являются изомерами с молекулярной формулой С10Н12О2. Для установления точной структурной формулы о-эвгенола его обработали сначала безводным хлористым водородом, а образовавшееся производное (G) – спиртовым раствором КОН. Образовавшийся продукт (H) имеет молекулярную формулу С10Н12О2 и не взаимодействует с раствором FeCl3.
1. Установите строение о-эвгенола и соединений В–Е и G–Н.
2. Рассчитайте общий выход о-эвгенола.
3. Почему при добавлении раствора FeCl3 к некоторым веществам образуются окрашенные растворы?
Решение
Все реакции, входящие в схему синтеза о-эвгенола, протекают по фенольным группам:

Строение о-эвгенола однозначно устанавливается за счет синтеза циклического эфира по схеме

Общий выход о-эвгенола в это синтезе составляет 0,87·0,77·0,80·0,85·0,85·100% = 38,7%.
Растворы хлорного железа реагируют с фенольными гидроксильными группами, образуя комплексы различного состава, причем для появления окраски достаточно одного фенолятного лиганда:
ArOH + [Fe(H2O)6]3+ = [(ArO)Fe(H2O)5]2+ + H+
Разбалловка:
За строение о-эвгенола 2 балла
За строение В–Е и G–Н 6×1 баллу: всего 6 баллов
За расчет выхода 1 балл
За окраску с FeCl3 1 балл
Итого: 10 баллов
№7
Поиск и синтез пористых органических молекул является актуальной задачей для получения металл-органических пористых полимеров. Вещество Х – возможная основа для таких материалов. Синтез Х описывается следующей схемой:

![]()
Соединение A (углеводород, содержащий 90 % углерода) имеет два, а вещество Х – три типа атомов водорода (по данным спектров ЯМР 1Н). Вещество В содержит 80.8 % брома.
Вопросы.
Расшифруйте схему синтеза Х и напишите структурные формулы соединений А, В, С и X.
Возможно ли использование на стадии B – C раствора щёлочи?
Какова роль СF3COOH на стадии получения Х?
