
- •Дополнительная
- •Определение аналитической химии.
- •3). Классификация методов ах по природе анализируемых составных частей объекта:
- •4). По ходу анализа методы аналитической химии делятся на:
- •Классификация методов определения
- •5). Классификация методов ах по способу выполнения реакции.
- •6). Классификация ах по количеству анализируемого вещества.
- •Требования к методам аналитической химии.
- •Значение аналитической химии.
- •Лекция 2.
- •Равновесие в гомогенной системе.
- •Термодинамическая, концентрационная и условная константы равновесия. Связь между ними.
- •Связь между термодинамической и реальной константами
- •Применение органических реагентов в анализе.
- •Применение органических реагентов.
- •Хелаты.
- •Строение органических реагентов, способных образовывать внутрикомплексные соединения.
- •Комплексообразующие группы.
- •Солеобразующие группы
- •Устойчивость внутрикомплексных соединений.
- •Лекция 4 Окислительно-восстановительные потенциалы и их использование в анализе.
- •Факторы, влияющие на величину окислительно-восстановительного потенциала.
- •Влияние конкурирующей реакции осадкообразования на потенциал
- •Влияние конкурирующей реакции комплексообразования на величину окислительно-восстановительного потенциала.
- •Лекция 5 Буферные растворы
- •Механизм действия буферной системы
- •РН некоторых биологических жидкостей.
- •Расчёт рН буферного раствора
- •Способы выражения концентрации растворов.
- •Инструментальные методы анализа
- •Принципы аналитической оптической спектроскопии.
- •Молекулярный абсорбционный анализ
- •Пределы измерения оптической плотности
- •Методы установления подчинимости основному закону светопоглощения.
- •Методы определения концентрации вещества в растворе
- •Атомно – эмиссионная спектроскопия
- •Лекция 8 Атомно-абсорбционная спектроскопия
- •Способ атомизации.
- •Способы определения концентрации
- •Достоинства метода.
- •Недостатки метода.
- •Лекция 9 Потенциометрия
Лекция 8 Атомно-абсорбционная спектроскопия

Метод атомно-абсорбционной спектроскопии (ААС) основан на поглощении (абсорбции) электромагнитного излучения атомами вещества в свободном состоянии. Общую схему атомной абсорбции можно представить следующим образом:
А+hν (от внешнего источника излучения) → А•
Атомы поглощают кванты света, соответствующие переходу из основного состояния в возбуждённое. В результате излучение, проходящее через атомный пар, ослабляется. Зависимость степени поглощения излучения от концентрации атомов описывается законом Бугера-Ламберта-Бера:
Ig(Io/I) = k•c•l
где Io – интенсивность падающего излучения; I - интенсивность прошедшего через пар излучения; l – толщина слоя атомного пара; k - атомный коэффициент поглощения. k = 108.
Способ атомизации.
В ААС аналитический сигнал получают от невозбуждённых атомов, поэтому для атомизации подходят лишь такие источники, энергии которых хватает для распада вещества на атомы, но не для возбуждения атомов. Такими атомизаторами являются пламя и электротермический атомизатор-графитовая кювета, которую нагревают с помощью электрического тока. Анализируемый раствор с помощью распылителя переводится в аэрозоль и подаётся в пламя горелки. Под действием высокой температуры растворитель испаряется, а находящиеся в растворе соли распадаются на атомы, способные поглощать излучение.
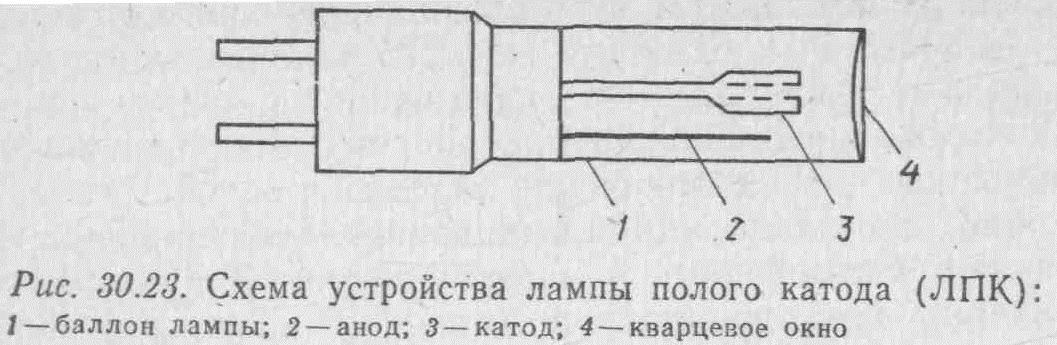
Источником излучения является лампа с полым катодом. Лампа с полым катодом представляет собой стеклянный или кварцевый баллон, заполненный инертным газом, внутри которого находятся два электрода-катода и анод. Катод изготавливается из того же металла, который нужно определять. При подаче напряжения на электроды возникает тлеющий разряд с образованием положительных ионов газа- наполнителя, например аргона. Положительные ионы бомбардируют катод, выбивая атомы металла в газовую фазу. Там эти атомы возбуждаются и испускают излучение.
Излучение направляют на пламя (или графитовую кювету), где находятся атомы определяемого элемента. Таким образом, для определения каждого элемента нужна своя лампа.
Приёмником света, прошедшего через пробу, является фотоэлемент или фотоумножитель.
Способы определения концентрации
Поглощение излучения атомами подчиняется тем же законам, что и поглощение молекулами. Сигнал прямо пропорционален концентрации определяемого компонента. Для определения концентрации используют метод градуировочного графика и метод добавок.
Достоинства метода.
- Высокая чувствительность, до 10-3 мкг/мл.
- Высокая избирательность.
- Экспрессность, т.е. быстрота анализа.
Методом ААС можно определять около 70 элементов в периодической системе Менделеева. Этот метод успешно применяется для определения цинка, железа, марганца и некоторых других элементов в почвах, удобрениях, растениях, водах и т.д. Используется также в клинических и биологических анализах.
Недостатки метода.
- Для определения каждого элемента нужна своя лампа.
- Определение только одного элемента в пробе.
