
- •Дополнительная
- •Определение аналитической химии.
- •3). Классификация методов ах по природе анализируемых составных частей объекта:
- •4). По ходу анализа методы аналитической химии делятся на:
- •Классификация методов определения
- •5). Классификация методов ах по способу выполнения реакции.
- •6). Классификация ах по количеству анализируемого вещества.
- •Требования к методам аналитической химии.
- •Значение аналитической химии.
- •Лекция 2.
- •Равновесие в гомогенной системе.
- •Термодинамическая, концентрационная и условная константы равновесия. Связь между ними.
- •Связь между термодинамической и реальной константами
- •Применение органических реагентов в анализе.
- •Применение органических реагентов.
- •Хелаты.
- •Строение органических реагентов, способных образовывать внутрикомплексные соединения.
- •Комплексообразующие группы.
- •Солеобразующие группы
- •Устойчивость внутрикомплексных соединений.
- •Лекция 4 Окислительно-восстановительные потенциалы и их использование в анализе.
- •Факторы, влияющие на величину окислительно-восстановительного потенциала.
- •Влияние конкурирующей реакции осадкообразования на потенциал
- •Влияние конкурирующей реакции комплексообразования на величину окислительно-восстановительного потенциала.
- •Лекция 5 Буферные растворы
- •Механизм действия буферной системы
- •РН некоторых биологических жидкостей.
- •Расчёт рН буферного раствора
- •Способы выражения концентрации растворов.
- •Инструментальные методы анализа
- •Принципы аналитической оптической спектроскопии.
- •Молекулярный абсорбционный анализ
- •Пределы измерения оптической плотности
- •Методы установления подчинимости основному закону светопоглощения.
- •Методы определения концентрации вещества в растворе
- •Атомно – эмиссионная спектроскопия
- •Лекция 8 Атомно-абсорбционная спектроскопия
- •Способ атомизации.
- •Способы определения концентрации
- •Достоинства метода.
- •Недостатки метода.
- •Лекция 9 Потенциометрия
Пределы измерения оптической плотности

Если вещество не поглощает свет, то Io=I, следовательно Io/I = 1, Ig 1 = 0, А = 0.
Если вещество полностью поглощает свет (I = 0), Io/I = ∞, Ig Io/I = ∞, А = ∞,
т.е. теоретически оптическая плотность меняется от нуля до бесконечности.
Но экспериментально доказано, что наиболее правильные и точные результаты получаются когда оптическая плотность находится в пределах от 0,1 до 1.
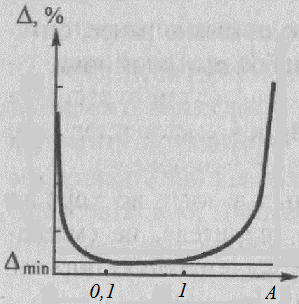
Здесь по оси ординат отложена погрешность, по оси абсцисс – оптическая плотность.
Если А < 0,1 и А > 1, то погрешность резко возрастает.
т.е. надо проводить измерения оптической плотности в интервале от 0,1 до 1,0,
где погрешность измерения минимальная. Чтобы попасть в этот интервал надо варьировать концентрацию и толщину поглощающего слоя (толщину кюветы).
А – величина безразмерная.

Т – пропускание – это отношение интенсивности прошедшего через раствор света к интенсивности падающего света. Тогда А=-lgТ
Пропускание измеряется в процентах.

Т изменяется от 0 до 100%.
СПЕКТРЫ ПОГЛОЩЕНИЯ. СВЕТОФИЛЬТРЫ.
Окрашенный раствор поглощает не все лучи спектра в одинаковой степени. Часть лучей видимого света поглощается раствором сильно, а другая часть не поглощается. Иначе говоря, окрашенные соединения избирательно поглощают видимые лучи и в видимом спектре этих соединений наблюдаются полосы поглощения – спектры поглощения.
СПЕКТР ПОГЛОЩЕНИЯ ─ ЗАВИСИМОСТЬ ОПТИЧЕСКОЙ ПЛОТНОСТИ ОТ ДЛИНЫ ВОЛНЫ ПАДАЮЩЕГО СВЕТА.
Для подбора длины волны падающего света используются светофильтры. Светофильтры подбирают опытным путём. Измеряют оптическую плотность окрашенного раствора с наибольшей концентрацией при всех светофильтрах и стоят зависимость оптической плотности от длины волны.
Тот светофильтр, который даёт наибольшую плотность раствора считается наиболее подходящим для дальнейшей работы. При максимальной длине волны малярный коэффициент поглощения тоже максимальный, а он характеризует чувствительность, т.е. надо работать при максимальной длине волны.
Методы установления подчинимости основному закону светопоглощения.
1). Снимают зависимость оптической плотности от концентрации стандартных растворов по отношению к раствору сравнения. Если раствор подчиняется основному закону, наблюдается прямая пропорциональность между оптической плотностью и концентрацией. Прямая линия проходит через начало координат.
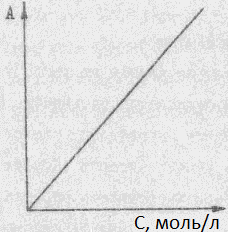
Зависимость оптической плотности от концентрации называется градуировочным графиком, им пользуются при проведении количественного анализа.
2). Строят зависимость молярного коэффициента светопоглощения от концентрации при постоянной длине волны.
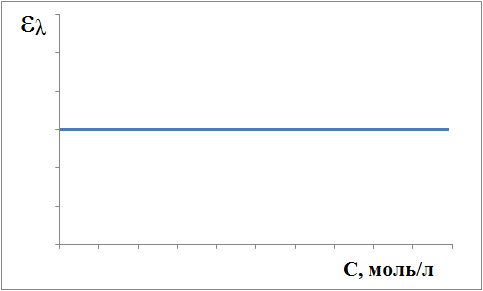
3). Снимают зависимость оптической плотности от длины волны для ряда стандартных растворов. Если максимум поглощения наблюдается при одной и той же длине волны, то раствор подчиняется основному закону светопоглощения.
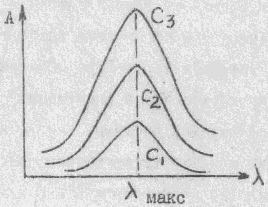
4). Строят зависимость молярного коэффициента поглощения от длины волны для стандартных растворов с концентрациями С1, С2, С3.
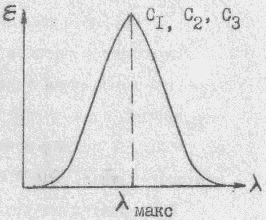
5). Если окрашенный раствор подчиняется закону Бугера-Ламберта-Бера, то при разбавлении раствора в «n» раз и увеличении толщины кюветы в «n» раз оптическая плотность должна остаться постоянной.
