
- •Введение
- •Лабораторная работа № 1. Экстракционное концентрирование цветных металлов карбоновыми кислотами
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 2. Разделение катионов меди и цинка методом ионообменной хроматографии
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 3. Разделение смеси углеводородов методом хроматографии
- •Лабораторная работа № 4. Изучение электропроводности растворов электролитов
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 5. Кондуктометрическое определение константы диссоциации слабой кислоты
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка экспериментальных данных
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 6. Кондуктометрическое кислотно-основное титрование
- •Лабораторная работа № 7. Определение содержания сильной кислоты и одноименной соли слабого основания кондуктометрическим методом
- •Лабораторная работа № 8. «определение концентрации хлорид-иона методом прямой кондуктометрии»
- •Лабораторная работа № 9. Определение среднеионного коэффициента активности потенциометрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 10. Определение значения стандартного электродного потенциала
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 11. Измерение и расчет рн в растворах сильных и слабых электролитов
- •Лабораторная работа № 12. Выбор состава и приготовление буферного раствора с заданными рн и ёмкостью
- •Выполнение работы
- •Лабораторная работа № 13. Потенциометрическое кислотно-основное титрование
- •Лабораторная работа № 14. Потенциометрическое титрование с ионоселективным электродом
- •Лабораторная работа № 15. Потенциометрическое титрование в неводных средах
- •Лабораторная работа № 16. Получение спектра поглощения и определение аналитической длины волны для окрашенного комплекса соли металла в видимой области спектра поглощения
- •I. Приготовление рабочего раствора соли железа.
- •II. Получение спектра поглощения
- •Лабораторная работа № 17. Получение спектра поглощения и определение аналитической длины волны для органического вещества в ультрафиолетовой области спектра поглощения
- •Лабораторная работа № 18. Получение градуировочных графиков
- •Лабораторная работа № 19. Фотометрическое определение константы нестойкости тиоцианатного комплекса железа
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Лабораторная работа № 20. Фотометрическое определение содержания железа
- •Лабораторная работа № 21. Фотометрическое определение концентрации железа (III) в присутствии никеля
- •Лабораторная работа № 22. Фотометрическое определение цветности воды
- •Лабораторная работа № 23. Определение сульфат-иона турбидиметрическим методом
- •Лабораторная работа № 24. Фотометрическое определение содержания никеля в сточных водах
- •Лабораторная работа № 25. Определение мутности природных вод турбидиметрическим методом
- •Выполнение работы
- •Содержание протокола лабораторной работы
- •Обработка результатов эксперимента
- •Содержание отчета по лабораторной работе
- •Лабораторная работа № 26. Определение тяжелых металлов методом рентгено-спектральным флуоресцентным методом
- •Лабораторная работа № 27. Получение и анализ инфракрасных спектров поглощения
- •I. Градуировка анализатора
- •Содержание
Лабораторная работа № 17. Получение спектра поглощения и определение аналитической длины волны для органического вещества в ультрафиолетовой области спектра поглощения
Цель работы. Определение примеси спирта в формалине по поглощению в ультрафиолетовой области спектра.
Сущность работы. Определение количества заданного вещества может быть проведено химическим, физическим или физико-химическим методами. Инструментальные физико-химические методы анализа, такие как ИК-, УФ-, ЯМР- спектроскопия, хроматография, находят широкое применение в научных лабораториях, однако из-за необходимости применения сложной аппаратуры они избирательно применяются в студенческих практикумах.
Провести количественный анализ примеси спирта в формалине возможно методом УФ- спектроскопии. Данный метод анализа является несложным в аппаратурном оформлении, что позволяет провести анализ самостоятельно, и определить примесное содержание спирта в незначительном количестве: минимальной концентрацией фотометрического метода является с=10-5 моль/л. В качестве метода определения заданного компонента выбран фотометрический метод, основанный на поглощении света окрашенным соединением спирта с ди-(8-гидроксихинолин)-орто-ванадатом в ближней ультрафиолетовой области спектра.
Определение спиртов (метилового, этилового, бутилового, амилового) основано на реакции с ди-(8-гидроксихинолин)-орто-ванадатом, полученным при взаимодействии метаванадата натрия или аммония с 8-гидроксихинолином:
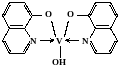
Реактив имеет сине-фиолетовую окраску и растворяется в бензоле, хлороформе, ацетоне и других органических растворителях. При добавлении спиртов к реактиву синяя окраска переходит в красную. Окрашенное соединение поглощает свет в ближней ультрафиолетовой области спектра.
Приборы и реактивы.
Реактивы
Формалин, 37% -й раствор формальдегида СН2О. Метаванадат аммония (натрия) NH4VО3, 0,1%-й раствор. 8-Гидроксихинолин C9H7NO, 2,5%-й раствор в 6%-й уксусной кислоте. Ацетатный буферный раствор (рН 4,5). Бензол С6Н6. Гидроксид натрия NaOH, 1M раствор. Стандартные 0,05-0,5% -е растворы анализируемого спирта в формалине. Формалин предварительно разбавляют в 4 раза водой.
Посуда
Делительные воронки (100 мл). Пипетки градуированные (1 мл). Бюретки (25 мл).
Аппаратура
Спектрофотометр или фотоэлектроколориметр КФК-3.
Выполнение работы
1. Снятие спектра поглощения и выбор длины волны. В делительную воронку помещают 1 мл стандартного 0,5%-ного раствора спирта в формалине, добавляют по 1 мл растворов метаванадата аммония и 8-гидроксихинолина и 4 мл ацетатного буферного раствора. Перемешивают, добавляют 15 мл бензола и продолжают перемешивание в течение 20 мин, используя магнитную мешалку.
Бензольный слой сливают в другую делительную воронку, взбалтывают 2 мин с 10 мл раствора NaOH, сливают органическую фазу в кювету прибора (l = 1 см) и измеряют оптическую плотность относительно раствора сравнения. Раствор сравнения готовят следующим образом, 15 мл бензола помещают в делительную воронку и добавляют 10 мл NaOH. Раствор сравнения взбалтывают и бензольный слой сливают в кювету, измеряют оптическую плотность в области длин волн 300-400 нм через каждые 5-10 нм. Строят график в координатах «оптическая плотность - длина волны» и выбирают длину волны (светофильтр), соответствующую максимуму поглощения.
2. Построение градуировочного графика. Для построения графика берут 3 - 4 стандартных раствора спирта в формалине в указанном интервале концентраций. Данные для раствора с заданной концентрацией получены при снятии спектра поглощения. В делительные воронки помещают по 1 мл каждого из стандартных растворов, добавляют те же реактивы и выполняют те же операции, что и при снятии спектра поглощения. Измеряют оптическую плотность каждого раствора при выбранной длине волны и строят градуировочный график в координатах «оптическая плотность - массовая доля спирта, % ».
3. Анализ исследуемого раствора. Пипеткой отбирают 25 мл исследуемого раствора формалина, помещают в мерную колбу вместимостью 100 мл и доводят до метки водой. Аликвоту этого раствора объемом 1 мл пипеткой помещают в делительную воронку, добавляют по 1 мл растворов метаванадата аммония и 8-гидроксихинолина, 4 мл ацетатного буферного раствора и перемешивают. Затем добавляют 15 мл бензола и выполняют те же операции, что и при снятии спектра поглощения. Измеряют оптическую плотность исследуемого раствора при выбранной длине волны и с помощью градуировочного графика находят массовую долю спирта (%) в формалине.
