
- •Основы пмп рафинирование металлов методами ликвации и фракционной перекристаллизации
- •Ликвационное рафинирование свинца от меди
- •Понятие о шлаке и его функциях в металлургии
- •При вычислении степени кислотности силикатного шлака Al2o3 и другие амфотерные оксиды в расчет не принимаются.
- •Основные автогенные процессы "взвешенные" плавки Процесс взвешенной плавки (пвп) фирмы "Оутокумпу" (Финляндия)
- •Кислородно-факельная плавка (кфп) фирмы инко (Канада)
- •Плавки в расплаве
- •Процесс Норанда (Канада)
- •Процесс Мицубиси (Япония)
- •Процесс Ванюкова а.В. (пв , Россия)
- •Процесс Айзасмелт (Осмелт, Австралия)
- •Конвертирование медных штейнов
- •Рафинирование черновой меди
- •Принципиальные технологические схемы производства никеля из рудного сырья
- •Производство и потребление свинца
- •Переработка вторичного свинцового сырья
- •Гидрометаллургия цинка
При вычислении степени кислотности силикатного шлака Al2o3 и другие амфотерные оксиды в расчет не принимаются.
Степенью основности или основностью шлака называют отношение числа молей основных окисидов к числу молей кремнезема. Например для составов 2СаО-SiO2 ; FеО-СаО-SiO2 степень основности равна 2.
ПЛАВКА СУЛЬФИДНЫХ МЕДНЫХ РУД НА ШТЕЙН
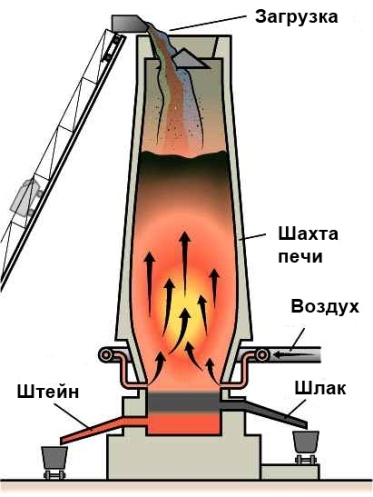
Медные руды и концентраты содержат медь, главным образом, в виде сульфидов: СuS, Cu2S, CuFeS2 и др. и пустую породу ;в виде SiO2 и силикатов. При содержании от 1,5—2,5% меди в руде и до 15—30% в концентрате основная задача плавки — получить медный штейн с содержанием меди 20—50%. Для этой цели применяют окислительную концентрационную плавку кусковых руд в шахтных печах, печах Ванюкова и других печах, где реализуется автогенный процесс.
4CuS = 2 Cu2S + S2,
S + O2 = SO2,
2CuFeS2 = Cu2S + 2FeS + 0,5 S2,
FeS + 1,5O2 = FeO + SO2,
2FeS2 = 2FeS + S2,
Cu2S + 1,5O2 = Cu2O + SO2 .
Между сульфидами и образовавшимися окcидами, особенно после расплавления сульфидов, образующих штейновую фазу (примерно при 900° С), происходит взаимодействие, в том числе и реакции взаимного обмена:
Cu2O + FeS = Cu2S + FeO.
При повышении температуры образуются силикаты и расплавленные шлаки из оксидов CuO, FеО, SiO2 и др. Далее идёт взаимодействие между двумя расплавленными фазами - штейном и шлаком, по реакции:
Cu2Oшлак + FeSштейн = Cu2Sштейн + FeOшлак
Если в штейне остаётся сульфид железа, медь всегда в виде Cu2S !

Схема шахтной печи
Вследствие большой величины стандартного термодинамического потенциала этой реакции Cu2O из шлака в значительной мере переходит в штейн, а железо распределяется между штейном и шлаком:
2FеО + SiO2 = 2FеО.SiO2.
В рудных плавках сульфидных руд на штейн получаются медные штейны, содержащие 30—50% Сu. Отвальные шлаки не содержат CuO, но содержат 0,2—0,3% Сu в виде тонкодисперсных, не отстоявшихся корольков штейна и растворенного в шлаке Cu2S.
ПРОДУВКА МЕДНОГО ШТЕЙНА В КОНВЕРТЕРЕ
Дальнейшая концентрация сульфида меди в штейне осуществляется продувкой его воздухом. Применяемый в этом случае конвертер представляет собой цилиндрический барабан, футерованный внутри огнеупорным кирпичом. В конвертер заливают расплавленный штейн и добавляют кварц в качестве флюса для связывания закиси железа в шлак. При продувке воздуха штейн частично окисляется:
FeS + 1,5O2 = FeO + SO2
Cu2S + 1,5O2 = Cu2O + SO2,
а затем образовавшаяся закись меди взаимодействует с еще неокислившимся сульфидом железа:
Cu2O + FeS = Cu2S+ FeO.
По этой причине в конвертерных шлаках остается до 2% Сu в составе закиси и в виде капелек сульфида меди.
Далее получаемый штейн конвертируют продувкой кислорода (воздуха). Кислород, имея большое сродство к сере, восстанавливает медь до черновой, подвергаемой далее электролитическому рафинированию.
Cu2S+ O2=2Сu +SO2 .
Медь хороший коллектор благородных металлов. Последние при электролизе меди накапливаются в шламе - основном сырье для производства металлов платиновой группы и золота.
ПЛАВКА ОКИСЛЕННЫХ НИКЕЛЕВЫХ РУД НА ШТЕЙН
Никелевые руды, содержащие 1—1,2% Ni в виде силикатов и алюмосиликатов закиси никеля, перерабатывают на никелевый штейн, содержащий до 20% Ni. В качестве источника серы служат либо пирит FeS2 либо гипс CaSO4.2H2O.
Плавку ведут в таких же печах, как и для медного сырья, в восстановительной среде. В печи гипс восстанавливается до сульфида кальция по реакции:
СаSO4 + 4СО = СаS + 4СО2.
При плавке с пиритом (его вводят в виде массивного колчедана или в виде отходов углеобогатительных фабрик) идут реакции:
2FeS2= 2FeS + S2; 0,5S2 + O2 = SO2 .
Далее протекает практически необратимая реакция:
3FeSштейн + 3NiOшлак =Ni3S2 штейн + 3FeOшлак + 0,5S2 .
Так как процесс идет в восстановительной среде, закись никеля, даже если она остаётся в шлаке, восстанавливается углеродом до металла.
Обычно содержание никеля в шлаках 0,1—0,2%, главным образом из-за растворенного в шлаке сульфидного никеля и взвешенных тонкодисперсных корольков штейна.
FeOшлак + CaS = FeSштейн + CaOшлак ,
3NiOшлак + 3CaS = Ni3S2 штейн + 2CaOшлак+ 0,5S2 .
Константа равновесия первой реакции при 1400° С k= 104,5, из чего следует, что вся закись железа FеО может быть переведена в сульфид железа с помощью СаS, или при избытке FеО остаток СаS будет практически отсутствовать. Для второй реакции k еще больше.
Однако закись никеля сульфидируется, главным образом сернистым железом, получаемым по первой реакции. Никелевый штейн содержит обычно 15—20% Ni. Его можно продуть воздухом в конвертере и получить чистый никелевый сульфид — файнштейн.
Конвертирование никелевого штейна, так же как и медного, осуществляется с добавкой в конвертер кварцевого флюса для ошлаковывания железа. При продувке воздуха штейн (сульфиды и содержащиеся в нем железо и никель) частично окисляется, но закись никеля тут же вступает в реакцию с сульфидом железа, переводящим никель в сульфидную фазу (файнштейн). Продувку ведут до тех пор, пока не получится сульфид никеля с примесью металлического никеля. Конвертерный шлак, содержащий повышенное количество никеля (до 4%), направляют на специальный обеднительный передел в конвертеры или электропечи.
Файншейн напрявляют на восстановительную плавку с нефтекоксом, не содержащим серу, и получают черновой никель, пригодгый для выплавки ферроникеля и электролитического рафинирования, а шлак, содержащий кобальт, направляют в кобальтовое отделение.
(В конверторах с продувкой кислорода черновой никель в принципе можно получить, но при температурах более 1500оС. Термодинамика такая!)
Производство важнейших тяжёлых цветных металлов пирометаллургическими способами
К пирометаллургическим относят процессы, идущие при повышенных температурах: сушка, различные виды обжига (хлорирующий, сульфатизирующий, окислительный, восстановительный и др.), спекание и сплавление компонентов шихты, различные виды плавок (рафинировочная, плавки на штейн и шлак и др.), металлотермия. К ним относят также "хлорную металлургию" (производство циркония, титана, тантала и ниобия) и электролиз в расплавах (производство алюминия и магния).
МЕДЬ
В 1997 г. суммарное мировое производство рафинированной меди составило 13,6 млн. т, в том числе ~2 млн. т (14,6%) из вторичного сырья. Четыре крупнейшие страны-продуцента: США, Чили, Япония и Китай – обеспечили 51,8% мирового производства рафинированной меди из первичного и вторичного сырья, а страны, вошедшие в первую десятку продуцентов, – 74,4%.
Основные страны производители меди по данным за 1997 г. (тыс. т)
|
Рафинированной меди |
Черновой меди |
Меди в концентратах |
США |
2452,4 |
1720,9 |
1940 |
Чили |
2116,6 |
1389,6 |
3392 |
Япония |
1278,7 |
1350,4 |
0,9 |
Китай |
1179,4 |
969 |
495,5 |
Германия |
673,6 |
349,1 |
- |
Россия |
610 |
570 |
530 |
Канада |
560,3 |
626,5 |
658 |
Польша |
440,6 |
442 |
414,7 |
Бельгия и Люксенбург |
386 |
142,5 |
- |
Перу |
384,1 |
326,4 |
603 |
Замбия |
338,4 |
315,8 |
352,9 |
Казахстан |
302,5 |
327,4 |
316,2 |
Мексика |
297 |
339 |
393,1 |
В России в 2002 г. произведено более 800 тыс. т рафинированной меди, из которой 450 тыс. т приходится на «Норильский никель» и 320 на УГМК.
Бóльшую часть меди получают из сульфидных медных (медно-никелевых, медно-цинковых) руд.
В России около 70% всей меди производится из медно-никелевых сульфидных руд (Норильск, Кольский полуостров), 22,6% из медно-колчедановых (медных и медно-цинковых руд), остальная – из других типов руд.
Переработка сульфидных медных концентратов с получением катодной меди в самом общем виде состоит из следующих стадий:
автогенная плавка (концентрата или огарка) на штейн (сплав сульфидов меди и железа)
во взвешенном состоянии или в расплаве;
конвертирование штейна (продувка кислородом) с получением черновой меди;
окислительное (анодное) рафинирование черновой меди;
электролитическое рафинирование анодной меди.


Основное оборудование для пирометаллургического производства меди
Плавка во взвешенном состоянии отличается от плавки в расплаве тем, что нагрев, окисление и расплавление шихтовых компонентов протекает в газошихтовом факеле.



C + O2 → CO2 + Q;
CuFeS2 + O2 → Cu2S + FeS + SO2;
Cu2S + FeS + O2 → Cu2S + FeO + SO2;
Cu2S + FeS + O2 + SiO2 → Cu2S + (FeO)2SiO2 + SO2;
Cu2S + O2 → Cu + SO2
Достоинства автогенных технологий по сравнению с традиционными процессами плавки (отражательной и электроплавкой) :
сокращение расходов топлива;
стабилизация потоков и сокращение объёмов отходящих газов и повышение концентрации в них SO2, что дает возможность утилизировать эти газы с минимальными затратами. За счет этого объём выбросов SO2 резко сокращается;
высокая удельная производительность;
возможность регулировать состав штейна и получать в процессе плавки концентратов богатые штейны.
