
- •Часть I
- •Содержание
- •Введение
- •Вводный блок основы математической обработки экспериментальных данных
- •1. Элементы теории вероятности и математической статистики
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •2. Ошибки измерений
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •3. Округление чисел
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •4. Построение графиков
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •5. Расчет коэффициентов прямой
- •Задачи и упражнения для самостоятельного решения
- •6. Линеаризация
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •7. Нахождение производных и интегрирование
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •1. Физическая химия модуль 1 термодинамика. Термохимия
- •1.1. Основные понятия и законы термодинамики. Термохимия
- •1.1.1. Первое начало термодинамики Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.1.2. Термохимия Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.1.3. Второе начало термодинамики. Энтропия Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.1.4. Термодинамические потенциалы. Функции Гиббса, Гельмгольца Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.2. Термодинамика химического равновесия
- •1.2.1. Изотерма химической реакции. Расчет констант равновесия химических реакций по термодинамическим таблицам Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.2.2. Зависимость констант равновесия реакций от температуры. Расчет равновесного выхода продуктов реакции Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •Модуль 2 химическое равновесие. Фазовые равновесия
- •1.3. Термодинамика фазовых равновесий
- •1.3.1. Фазовые равновесия в однокомпонентных системах. Правило фаз Гиббса. Уравнения Клапейрона, Клапейрона – Клаузиуса Основные уравнения
- •Примеры решения типовых задач
- •Задачи для самостоятельного решения
- •1.3.2. Фазовые равновесия в двухкомпонентных системах, перегонка Основные уравнения
- •Равновесие «твердое вещество – жидкость». Фазовая диаграмма системы с простой эвтектикой
- •Системы с ограниченной растворимостью в жидкой фазе (расслаивающиеся жидкости)
- •Перегонка с водяным паром
- •1.3.3. Фазовые равновесия в трехкомпонентных системах. Экстракция
- •П римеры решения типовых задач
- •Задачи для самостоятельного решения
- •Модуль 3 коллигативные свойства растворов. Электрохимия
- •1.4. Термодинамика разбавленных растворов, взаимосвязь между коллигативными свойствами
- •1.4.1. Давление пара растворителя над разбавленными растворами. Закон Рауля Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.4.2. Осмотическое давление растворов Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.4.3. Криоскопия. Эбуллиоскопия Основные уравнения Криоскопия
- •Эбулиоскопия
- •Экспериментальные методы определения молярных масс и изотонического коэффициента методом эбуллиоскопии и криоскопии
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.5. Термодинамика растворов электролитов
- •1.5.1. Теория растворов сильных электролитов Дебая – Хюккеля Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.5.2. Буферные системы и растворы Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.6. Электрохимия
- •1.6.1. Электропроводность растворов электролитов Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.6.2. Электродные потенциалы и электродвижущие силы гальванических элементов
- •1.6.2.1. Электроды и электродные потенциалы Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.6.2.2. Гальванические элементы и эдс Основные уравнения
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •Модуль 4 кинетика химических реакций и катализ
- •1.7. Кинетика химических реакций
- •1.7.1. Скорость реакции Основные уравнения Скорость реакции
- •Расчет скорости реакции по экспериментальным данным, заданным в виде таблицы
- •Расчет скорости реакции по экспериментальным данным, заданным в виде графика
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.7.2. Формальная кинетика необратимых реакций нулевого, первого, второго порядков Основные уравнения Основной постулат химической кинетики – закон действия масс для кинетики
- •Молекулярность химической реакции
- •Реакция нулевого порядка
- •Реакция первого порядка
- •Реакция второго порядка
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •Графический метод
- •Определение порядка реакции по периоду полупревращения
- •Дифференциальные методы Метод Вант-Гоффа
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.7.4. Зависимость скорости реакции от температуры Основные уравнения Правило Вант-Гоффа
- •Уравнение Аррениуса
- •Метод ускоренного определения срока годности лекарственных препаратов
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.7.5. Сложные реакции
- •Обратимые реакции
- •Параллельные реакции
- •Последовательные реакции
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •1.7.6. Ферментативный катализ
- •Примеры решения задач
- •Задачи и упражнения для самостоятельного решения
- •Модуль 5 поверхностные явления и адсорбция
- •1.8. Поверхностные явления и адсорбция
- •1.8.1. Термодинамика поверхностного слоя Основные уравнения Поверхностная энергия Гиббса и поверхностное натяжение
- •Методы определения поверхностного натяжения на легкоподвижных границах фаз
- •Краевой угол смачивания
- •Зависимость поверхностного натяжения от температуры. Связь поверхностной энергии Гиббса и поверхностной энтальпии
- •Энтальпия смачивания и коэффициент гидрофильности
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.8.2. Адсорбция на границе «жидкость – газ» Основные уравнения Уравнение изотермы адсорбции Гиббса
- •Изотерма поверхностного натяжения
- •Поверхностно-активные, поверхностно-инактивные вещества, их молекулярное строение
- •Ориентация молекул в поверхностном слое
- •Адсорбция на границе «жидкость – газ». Уравнение Ленгмюра
- •Определение площади, занимаемой молекулой поверхностно-активного вещества в насыщенном адсорбционном слое, и максимальной длины молекулы пав
- •Уравнение Шишковского
- •Правило Дюкло – Траубе
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •1.8.3. Адсорбция на границе «твердое тело – газ» и «твердое тело – жидкость» Основные уравнения Мономолекулярная адсорбция, уравнение изотермы адсорбции Лэнгмюра, Фрейндлиха
- •Полимолекулярная адсорбция
- •Капиллярная конденсация
- •Адсорбция электролитов. Неспецифическая (эквивалентная) адсорбция ионов. Избирательная адсорбция ионов. Правило Панета – Фаянса
- •Ионный обмен. Иониты и их классификация. Обменная емкость. Применение ионитов в фармации
- •Примеры решения задач
- •Задачи для самостоятельного решения
- •Предметный указатель
- •Приложение
- •1. Основные единицы измерения физических величин
- •2. Основные физические постоянные
- •3. Основные математические формулы дифференциального и интегрального исчисления
- •Основные правила дифференцирования
- •Основные правила интегрирования Неопределенный интеграл:
- •Определенный интеграл:
- •4. Критические значения коэффициента Стьюдента t
- •6. Стандартные энтальпии плавления и испарения при температуре фазового перехода
- •7. Константы Генри (Па) при 25с
- •8. Криоскопические и эбуллиоскопические константы
- •9. Термодинамические свойства простых веществ, ионов и соединений
- •Простые вещества и ионы
- •Неорганические соединения
- •Органические соединения Углеводороды
- •Кислородсодержащие соединения
- •Галогенсодержащие соединения
- •Азотсодержащие соединения
- •10. Теплота сгорания питательных веществ в живом организме и в калориметре
- •11. Криоскопические и эбуллиоскопические константы
- •12. Удельная электрическая проводимость растворов kCl
- •13. Предельные молярные подвижности ионов в водном растворе при 25°с
- •14. Молярная электропроводность разбавленных водных растворов электролитов при 25°с
- •15. Константы диссоциации слабых кислот при 25°с
- •16. Константы диссоциации слабых оснований при 25°с
- •17. Стандартные электродные потенциалы при 25°с
- •18. Основные физические постоянные
- •19. Плотность пав в жидком состоянии
- •20. Зависимость поверхностного натяжения воды от температуры
- •Литература
Определение площади, занимаемой молекулой поверхностно-активного вещества в насыщенном адсорбционном слое, и максимальной длины молекулы пав
Если известна величина Г, то можно рассчитать площадь, занимаемую одной молекулой ПАВ в насыщенном монослое S0
|
(318) |
где NA = 6,021023 моль–1 – число Авогадро.
Толщина адсорбционного слоя, равная длине молекулы, рассчитывается по уравнению:
|
(319) |
где М – относительная молекулярная масса ПАВ; – плотность ПАВ в жидком состоянии (Приложение 19).
Уравнение Шишковского
Зависимость поверхностного натяжения раствора ПАВ от его концентрации в растворе описывается уравнением Шишковского
|
(320) |
где В – эмпирическая константа, постоянная для данного гомологического ряда, которая равна
В= RTГ∞ |
(321) |
Поэтому уравнение Шишковского можно записать следующим образом:
|
(322) |
где – величина предельной адсорбции ПАВ в мономолекулярном слое на границе «ж – г», моль/м2; K – константа адсорбционного равновесия, л/моль; с – концентрация ПАВ в растворе, моль/л.
В области концентрированных растворов, для которых Kc >> 1 уравнение Шишковского принимает вид:
|
(323) |
Это уравнение линейно в координатах « – lnс». По графику, построенному в этих координатах (рис. 73), можно рассчитать константы и K, входящие в уравнение Шишковского и Ленгмюра.

Рис. 73. Схема расчёта констант в уравнении Шишковского в области концентраций Kс>>1 с помощью линеаризации уравнения
Правило Дюкло – Траубе
Влияние природы ПАВ на их поверхностную активность описывается правилом Дюкло-Траубе:
В пределах одного гомологического ряда поверхностная активность ПАВ увеличивается в 3 – 3,5 раза при удлинении гидрофобной части на одну метиленовую группу (-СН2-).
Правилу Дюкло – Траубе соответствует уравнение:
|
(324) |
где gn – поверхностная активность ПАВ, содержащего n -CH2- групп, gn+1 – поверхностная активность ПАВ, содержащего n+1 ‑CH2- групп.
Правило Дюкло – Траубе выполняется вследствие того, что в пределах одного гомологического ряда ПАВ объем, занимаемый одной ‑CH2- группой постоянен.
Из рисунка (74) видно, что чем длиннее углеводородная цепь, тем быстрее снижается σ водного раствора с ростом концентрации ПАВ.
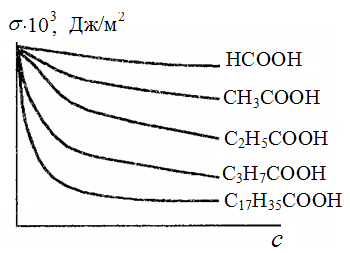
Рис. 74. Изотермы поверхностного натяжения для водных растворов карбоновых кислот при 298 К
Примеры решения задач
1. Определить адсорбцию (мкмоль/м2) при 10С для раствора, содержащего 50 мг пеларгоновой кислоты С8Н17СООН. Поверхностное натяжение исследуемого раствора 57,010–3 Дж/м2. Считать, что поверхностное натяжение изменяется в указанном диапазоне концентраций линейно.
Решение:
Находим
![]() (Приложение 20) при 10С,
которое составляет 74,2210–3
Дж/м2.
(Приложение 20) при 10С,
которое составляет 74,2210–3
Дж/м2.
Молярная концентрация кислоты в растворе равна:
![]() моль/л;
с1 = 0.
моль/л;
с1 = 0.
По уравнению Гиббса (310) рассчитаем адсорбцию раствора пеларгоновой кислоты:
![]()
![]()
2. По уравнению Шишковского рассчитать поверхностное натяжение водного раствора масляной кислоты с концентрацией 0,104 моль/л при 273 К. Поверхностное натяжение воды при той же температуре 75,6210–3 Дж/м2. Константы уравнения Шишковского B = 12,6103 Дж/м2, K = 21,5 л/моль.
Решение:
По уравнению Шишковского (322), рассчитываем поверхностное натяжение водного раствора масляной кислоты, учитывая, что константа В определяется по уравнению (321):
![]()
![]() .
.
3. Найдите значение адсорбции и площади, занимаемой одним ммолем уксусной кислоты при различных концентрациях, если при определении поверхностного натяжения растворов уксусной кислоты при 20°С были получены следующие результаты:
с, моль/л |
0 |
0,01 |
0,1 |
0,5 |
1,0 |
σ, мДж/м2 |
72,26 |
70,02 |
66,88 |
61,66 |
57,28 |
Решение:
Рассчитываем величину адсорбции уксусной кислоты по уравнению (310):




Рассчитаем площадь, занимаемую одним ммолем уксусной кислоты при заданных концентрациях, по уравнению, которое следует из уравнения (318):
![]()
![]()
![]()
![]()
![]()
