
- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Глава 1. Геном 25
- •Глава 2. Реализация генетической информации при экспрессии генов 61
- •Глава 3. Основные пути регуляции экспрессии генов 224
- •Глава 4. Воспроизведение генетической информации 390
- •Глава 5. Защита генетической информации 432
- •Глава 6. Современная концепция гена 522
- •Часть II. Искусственные генетические системы 531
- •Глава 7. Принципы генной инженерии 532
- •Глава 8. Направленный мутагенез и белковая инженерия 629
- •Глава 9. Антисмысловые рнк, рибозимы и дезоксирибозимы 679
- •Глава 10. Трансгенные животные и растения 722
- •Глава 11. Днк-диагностика и днк-типирование 755
- •Глава 12. Картирование и определение первичной структуры генома человека 797
- •Предисловие редактора
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Глава 1.Геном
- •1.1.Гены и хромосомы
- •1.2.Геном прокариот
- •1.2.1.Геном вирусов
- •1.2.2.Нуклеоид бактериальной клетки
- •1.2.3.Геном архебактерий
- •1.2.4.Минимальный размер генома одноклеточных организмов
- •1.3.Геном эукариот
- •1.3.1.Последовательности нуклеотидов эукариотического генома
- •1.3.2.Хроматин
- •1.3.3.Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Глава 2.Реализация генетической информации при экспрессии генов
- •2.1.Транскрипция
- •Характеристики белковых компонентов холофермента
- •2.1.2.Единицы транскрипции (транскриптоны)
- •2.1.3.Этапы транскрипции
- •2.1.4.Хроматин во время транскрипции
- •2.2.Котранскрипционные и посттранскрипционные модификации рнк
- •2.2.1.Процессинг рнк у бактерий
- •2.2.2.Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •2.2.3.Другие модификации эукариотических мРнк
- •Механизм прямой и обратной реакций аутосплайсинга
- •2.3.Функциональная компартментализация ядра
- •2.3.1.Интерфазные хромосомы в ядре
- •2.3.2.Ядрышко
- •2.3.3.Пространственная организация синтеза мРнк
- •2.3.4.Ядерные тельца и домены
- •2.3.5.Компартментализованное ядро
- •2.4.Биосинтез белка рибосомами бактерий
- •2.4.1.Рибосомы
- •2.4.2.Этапы биосинтеза белка
- •2.4.3.Антибиотики, действующие на уровне трансляции
- •2.5.Трансляция у эукариот
- •2.5.1.Особенности первичной структуры эукариотических мРнк
- •2.5.2.Инициация биосинтеза белка эукариотическими рибосомами
- •2.5.3.Элонгация полипептидных цепей
- •2.5.4.Терминация трансляции
- •2.5.5.Трансляция в митохондриях
- •2.5.6.Трансляция в хлоропластах.
- •Глава 3.Основные пути регуляции экспрессии генов
- •3.1.Регуляция экспрессии генов на уровне транскрипции у прокариот
- •3.1.1.Регуляция на уровне инициации транскрипции
- •3.1.2.Регуляция синтеза рнк на уровне элонгации и терминации
- •3.2.Регуляция экспрессии генов на уровне транскрипции у эукариот
- •3.2.1.Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •3.2.2.Механизмы позитивной регуляции транскрипции
- •Функциональные домены факторов транскрипции
- •3.2.3.Механизмы негативной регуляции транскрипции
- •3.2.4.Структура хроматина как специфический регулятор экспрессии генов
- •3.2.5.Импринтинг
- •3.2.6.Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •3.3.Посттранскрипционная регуляция экспрессии генов
- •3.3.1.Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •3.3.2.Сплайсинг рнк в регуляции экспрессии генов
- •3.3.3.Избирательная деградация мРнк
- •3.4.Регуляция экспрессии генов на уровне трансляции
- •3.4.1.Регуляция инициации трансляции
- •3.4.2.Регуляция элонгации синтеза полипептидных цепей
- •3.4.3.Регуляция терминации трансляции
- •3.5.Синтез белков, содержащих остатки селеноцистеина
- •3.6.Посттрансляционная регуляция экспрессии генов
- •3.6.1.Последствия фолдинга вновь синтезированных полипептидных цепей
- •3.6.2.Специфические протеиназы в посттрансляционном процессинге белков
- •3.6.3.Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •3.6.4.Сплайсинг белков
- •3.6.5.Другие посттрансляционные модификации белков
- •Глава 4.Воспроизведение генетической информации
- •4.1.Репликация днк
- •4.1.1.Белки, участвующие в репликации днк
- •4.1.2.Репликативная вилка e. Coli и бактериофага t4
- •4.1.3.Особенности функционирования репликативной вилки эукариот
- •4.2.Регуляция репликации днк
- •4.2.1.Инициация репликации днк у e. Coli и ее регуляция
- •4.2.2.Регуляция репликации плазмиды ColE1
- •4.3.Особенности репликации линейных геномов
- •4.3.1.Линейные хромосомы бактерий
- •4.3.2.Репликаторы эукариот
- •4.3.3.Репликация теломерных участков эукариотических хромосом
- •4.3.4.Пространственная организация синтеза днк у эукариот
- •Глава 5.Защита генетической информации
- •5.1.Мутации
- •5.1.1.Основные источники мутаций и методы определения мутагенной активности
- •5.1.3.Мутаторный фенотип
- •5.1.4.Экспансия днк
- •5.1.5.Адаптивные мутации
- •5.1.6.Механизмы защиты генома от мутаций
- •5.2.Репарация днк
- •5.2.1.Основные механизмы репарации поврежденной днк
- •5.2.2.Эксцизионная репарация в клетках животных
- •Белки животных, участвующие в ner
- •5.2.3.Гомологичная рекомбинация в репарации днк
- •5.2.4.Репарация ошибочно спаренных нуклеотидов
- •5.2.5.Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •5.3.Альтруистичная днк
- •5.3.1.Парадокс возможности существования многоклеточных организмов
- •5.3.2.Повышение информационной стабильности генома избыточными последовательностями
- •5.3.3.Селективная защита генов от мутаций
- •5.3.4.Высокоупорядоченное расположение летальных генов на хромосомах
- •5.3.5.Возможный смысл парадокса с
- •Глава 6.Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы Глава 7.Принципы генной инженерии
- •7.1.Основные ферменты, используемые в генной инженерии
- •7.1.1.Рестриктазы и днк-метилазы
- •7.1.3.Ферменты матричного синтеза днк и рнк
- •7.1.4.Другие ферменты
- •7.2.Векторы
- •7.2.1.Плазмидные векторы
- •7.2.2.Векторы на основе фага
- •7.2.3.Космиды и фазмиды
- •7.2.4.Сверхъемкие векторы yac, bac и pac
- •7.2.5.Интегрирующие и челночные (бинарные) векторы
- •7.2.6.Конструирование экспрессирующих векторов и их функционирование
- •7.2.7.Векторы для переноса днк в клетки животных и растений
- •7.3.Клонотеки генов
- •7.3.1.Получение клонотек генов
- •7.3.2.Введение рекомбинантных днк в клетки
- •7.3.3.Методы скрининга клонотек генов
- •7.4.Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •7.4.1.Клетки яичников китайских хомячков (линия cho)
- •7.4.2.Клетки мышиной миеломы (линия Sp2/0)
- •7.4.3.Клетки селезенки мышей (линия mel)
- •7.4.4.Клетки африканской зеленой мартышки (линия cos)
- •7.4.5.Клетки насекомых, зараженные бакуловирусами
- •7.4.6.Сравнение эффективности рассмотренных систем экспрессии
- •7.5.Бесклеточные белоксинтезирующие системы
- •7.5.1.Прокариотические системы
- •7.5.2.Эукариотические системы
- •7.5.3.Проточные системы
- •7.6.Другие современные методы исследования генов
- •7.6.1.Рестрикционное картирование генов
- •7.6.2."Прогулки и прыжки по хромосомам"
- •7.6.4.Футпринтинг
- •7.7.Стратегия выделения нового гена
- •Глава 8.Направленный мутагенез и белковая инженерия
- •8.1.Методы направленного получения мутаций
- •8.1.1.Получение делеций и вставок
- •8.1.2.Химический мутагенез
- •8.1.3.Сайт-специфический мутагенез с использованием олигонуклеотидов
- •8.1.4.Полимеразная цепная реакция в направленном мутагенезе
- •8.2.Белковая инженерия
- •8.2.1.Библиотеки пептидов и эпитопов
- •8.2.2.Белки-репортеры в гибридных белках
- •8.2.3.Гибридные токсины
- •8.2.4.Подходы к созданию новых ферментов
- •8.2.5. Субтилигаза в лигировании пептидов
- •8.3.Концепция ксенобиоза
- •Глава 9.Антисмысловые рнк, рибозимы и дезоксирибозимы
- •9.1.Антисмысловые рнк и олигонуклеотиды
- •9.1.1.Механизм действия антисмысловых рнк
- •9.1.2.Использование антисмысловых рнк
- •9.1.3.Природные антисмысловые рнк
- •9.1.4.Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •9.2.Рибозимы и дезоксирибозимы
- •9.2.1.Типы рибозимов
- •9.2.2.Свойства рибозимов
- •9.2.3.Рибозимы как лекарственные средства
- •9.2.4.Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •9.2.5.Дезоксирибозимы
- •9.3.Аптамеры
- •9.4.Молекулы рнк у истоков жизни
- •9.4.1.Молекулы рнк в качестве рнк-репликаз
- •9.4.2.Возможность синтеза полипептидных цепей молекулами рнк
- •Глава 10.Трансгенные животные и растения
- •10.1.Способы получения трансгенных многоклеточных организмов
- •10.2.Экспрессия трансгенов
- •10.3.Использование трансгенов у животных
- •10.3.1.Исследование механизмов экспрессии генов
- •10.3.2.Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •10.3.3.Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •10.3.4.Моделирование наследственных и приобретенных заболеваний человека
- •10.4.Трансгенные растения
- •10.5.Генотерапия наследственных и приобретенных заболеваний
- •10.5.1.Способы доставки новых генов в геном человека
- •10.5.2.Управление экспрессией трансгенов в клетках-мишенях
- •10.5.3.Современные достижения генотерапии онкологических заболеваний
- •10.5.4.Ближайшие перспективы использования генотерапии
- •10.5.5.Успехи генотерапии в модельных экспериментах
- •10.5.6.Проблемы, возникающие в связи с практическим применением генотерапии
- •Глава 11.Днк-диагностика и днк-типирование
- •11.1.1.Получение клинического генетического материала
- •11.1.2.Диагностика заболеваний
- •11.2.2.Идентификация личности на основе минисателлитной днк: определение отцовства
- •11.3.Микроматрицы и микрочипы днк
- •11.3.1.Методы создания микроматриц днк
- •11.3.2.Ограничения в использовании микроматриц днк
- •11.3.3.Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Глава 12.Картирование и определение первичной структуры генома человека
- •12.1.Основные подходы к картированию генома человека
- •12.1.1.Генетические карты сцепления
- •12.1.2.Пцр в исследованиях генома человека
- •12.1.3.Физические карты низкого разрешения
- •12.1.4.Физические карты высокого разрешения
- •12.2.Определение полной первичной структуры днк генома человека
- •12.3.Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
5.3.1.Парадокс возможности существования многоклеточных организмов
Огромный размер генома многоклеточных организмов с генетической точки зрения должен создавать для их существования многочисленные и, на первый взгляд, трудноразрешимые препятствия. Проблемы начинаются уже при редупликации гигантских молекул геномной ДНК с помощью ферментных систем, точность функционирования которых не является абсолютной. Кроме того, репликация происходит в присутствии мутагенов экзогенного и эндогенного происхождения. Принято считать, что частота спонтанных мутаций в геноме соматических клеток млекопитающих, растущих в культуре, варьирует от локуса к локусу одного и того же генома и, по разным оценкам, достигает значений от 10-8 до 10-12 на нуклеотид за клеточную генерацию. Точное определение частоты спонтанных мутаций в геномной ДНК высших эукариот in vivo является сложной задачей. По ряду экспериментальных и косвенных данных, в частности, исходя из частоты встречаемости некоторых наследственных заболеваний в популяциях человека (например серповидно-клеточной анемии, вызываемой заменой единственного нуклеотида в геномной ДНК), полагают, что эти показатели, по крайней мере, не ниже значений, полученных in vitro.
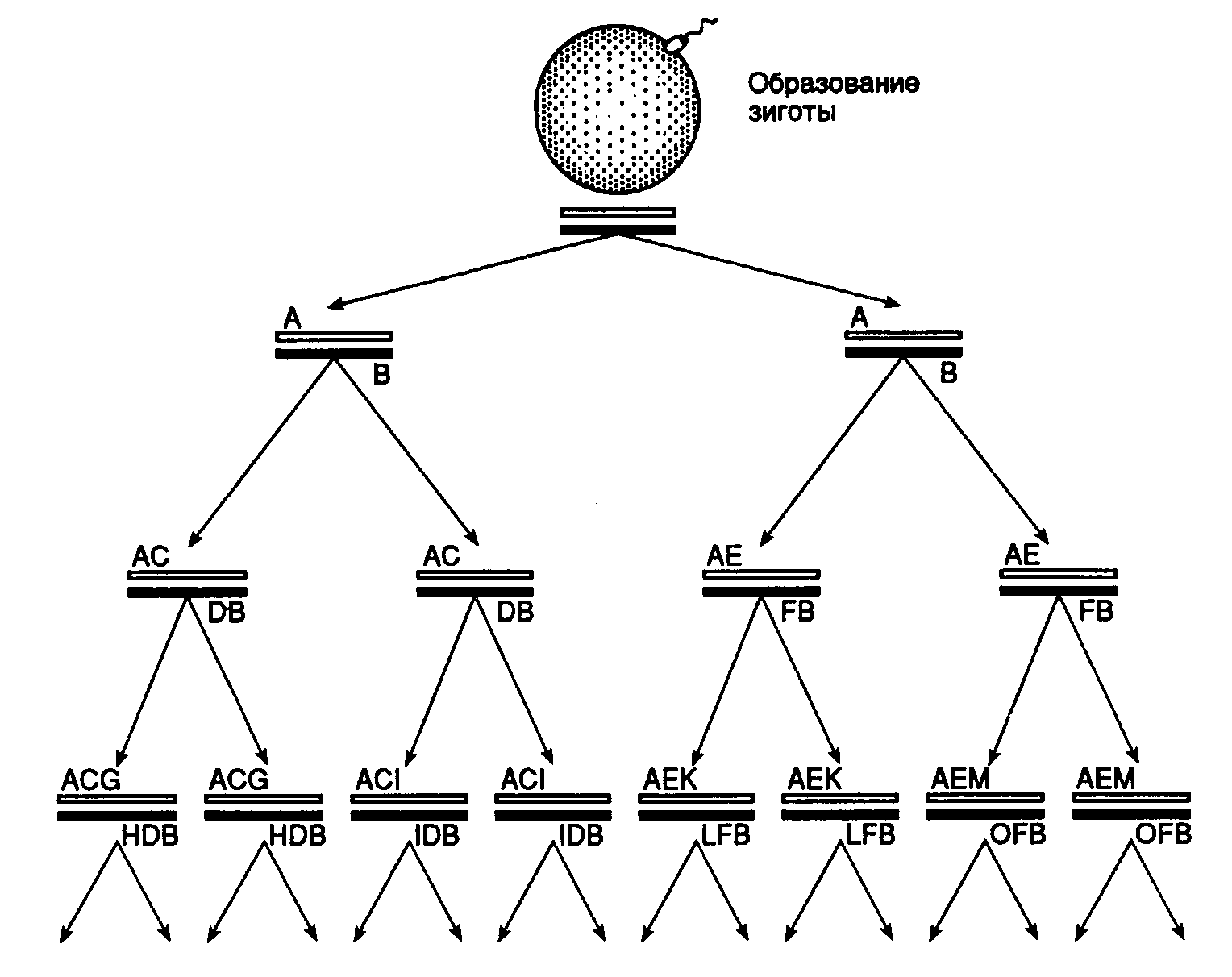
Рис. I.62. Происхождение генетического груза в геноме соматических клеток многоклеточных организмов
Развитие многоклеточного организма начинается с дробления зиготы, образующейся в процессе оплодотворения яйцеклетки и содержащей диплоидный набор хромосом (две параллельные линии вверху рисунка). А–М – наборы мутаций
Принимая, что суммарная ДНК гаплоидного генома человека насчитывает 3·109 п.о., а частота спонтанных мутаций в среднем составляет 10-8 на нуклеотид за генерацию, можно предположить, что, начиная с первого деления оплодотворенной яйцеклетки в процессе онтогенетического развития организма человека, каждое следующее деление должно сопровождаться появлением в их геномной ДНК, по крайней мере, 30 независимых мутаций (рис. I.62). Организм человека состоит из 1015 клеток. Для образования стольких клеток из оплодотворенной яйцеклетки требуется 50 клеточных генераций. Следовательно, гаплоидный геном каждой из соматических клеток человека 50-й генерации должен содержать в разных частях, по крайней мере, 1500 мутаций. Если предположить далее, что набор из 30 мутаций возникает и закрепляется в каждом последующем клеточном делении независимо от мутаций, полученных во время предыдущих делений клеток, то получается, что любая дочерняя соматическая клетка наследует от клетки-предшественницы все имеющиеся в ее геноме мутации и приобретает блок новых 30 мутаций. При этом набор соматических мутаций в потомстве каждой из делящихся клеток одного поколения будет отличаться один от другого, в том числе и в парах аллельных локусов ДНК отдельных клеток, поскольку они редуплицируются независимо. При таком развитии событий мутации, возникающие в геноме соматических клеток каждой последующей генерации, случайным образом сканируют шаг за шагом всю реплицирующуюся геномную ДНК, а результаты сканирования не повторяются в каждом новом поколении клеток. Так, блок из 30 спонтанных мутаций, возникающих после гипотетической 50-й генерации соматических клеток в онтогенезе многоклеточного организма, должен присутствовать в 1015 (250) вариантах.
Проблема становится еще более очевидной, если иметь в виду, что многие клетки организма, например эпителиальные или стволовые клетки крови, пролиферируют на протяжении всей жизни многоклеточного организма, совершая громадное число клеточных делений. По некоторым оценкам, общее число клеточных циклов, в которых участвуют клетки человека на протяжении его жизни, приближается к 1016. Кроме того, соматические мутации возникают в многоклеточном организме не только в активно пролиферирующих, но и покоящихся клетках. Частоты возникновения спонтанных мутаций в пролиферирующих и в покоящихся клетках млекопитающих в ряде случаев различаются лишь незначительно.
Парадоксальность эволюционно сложившейся генетической ситуации заключается в том, что если бы большая часть последовательностей нуклеотидов геномной ДНК заключала в себе жизненно важную генетическую информацию, существование многоклеточных организмов было бы невозможно. Их гибель происходила бы из-за неизбежного накопления в делящихся соматических клетках вредных или летальных мутаций, приводящих к обрыву линий дифференцирующихся в онтогенезе соматических клеток. Это особенно относится к мутациям в жизненно важных генах половых хромосом, которые в соматических клетках находятся в гемизиготном состоянии. Альтернативно основные генетические локусы многоклеточных организмов могут находиться под дополнительной защитой от мутационных изменений.2
На основании приведенных выше аргументов можно сделать вывод о том, что большая часть некодирующих избыточных последовательностей нуклеотидов геномной ДНК эукариот не заключает в себе жизненно важной генетической информации и/или у эукариотических клеток имеются механизмы, обеспечивающие дополнительную защиту геномной ДНК от мутаций. Не соглашаясь с основными положениями концепции "эгоистической" и "паразитической" ДНК, можно предположить, что именно такая организация генома эукариотических организмов, в корне отличающаяся от структуры генома прокариот, имеет отношение к разрешению проблемы генетической парадоксальности существования многоклеточных организмов, которую можно назвать парадоксом М (Metazoa, Metaphyta). Создается впечатление, что именно избыточная ДНК генома эукариот может иметь отношение к повышению его информационной стабильности до уровня, необходимого для реализации многоклеточности в природе.
