
- •Медицине нельзя научить, медицине можно только научиться. М.Я. Мудров Для нас нет и не может быть иного закона, кроме: от изучения человека – к пользе человеку. Р. Лериш
- •Введение в физиологию.
- •Общая функциональная характеристика организма
- •Самостоятельная работа студентов во внеаудиторное время
- •Общая характеристика нормальной физиологии
- •Основные исторические этапы развития физиологии.
- •Физиология как научная основа здорового образа жизни, оценки здоровья и работоспособности человека.
- •Методологические принципы в физиологии
- •Физиологическая функция
- •Норма и параметры функции.
- •Клетка и ее функции
- •Основные структурно-функциональные компоненты клетки.
- •Транспортная функция клеточной мембраны.
- •Функция размножения клеток.
- •Функция гибели клетки.
- •Физиологическая характеристика тканей
- •Общая характеристика органов
- •Общая характеристика организма
- •Профильные материалы
- •Для студентов всех факультетов
- •Средства для самоподготовки студентов
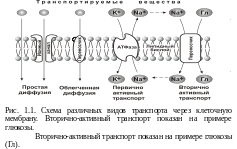
Транспортная функция клеточной мембраны.
Функциональная структура мембраны. Основными её компонентами являются липиды, белки и углеводы.
Липиды составляют 30 – 70% мембраны, они представлены преимущественно фосфолипидами (60% от всех липидов), холестеролом (≈ 20%) и гликолипидами (≈ 5%).
Фосфолипиды (фосфатидилхолин, фосфатидилэтаноламин, фосфатидилсерин, сфингомиелин) имеют гидрофильные полярные головки и неполярные гидрофобные хвосты, присоединенные к головкам с помощью глицерола. Липиды в мембране путем самосборки образуют бимолекулярный слой, полярные головки которого контактируют с внеклеточным и внутриклеточным водными отсеками, а гидрофобные хвосты контактируют друг с другом по принципу «хвост к хвосту» (рис. 1.1). Способность к самосборке создает и другую способность липидного бислоя – самовосстановления поврежденных участков мембраны. Фосфолипиды в бислое могут совершать вращательные и продольные движения. Липидный бислой имеет барьерную и транспортную функции, служит растворителем для белков, образуя «липидную рубашку», необходимую для их функций, создает ёмкостные свойства мембраны.
Холестерол увеличивает механическую прочность бислоя. Кроме того, холестерол ингибирует фазовые переходы мембраны (гелевую/жидкокристаллическую), которые могут возникать при изменении температуры, рН, ионной силы и приводить к резкому изменению вязкости бислоя с нарушением транспортных и ферментативных функций мембраны.
Гликолипиды (см. ниже углеводы мембраны).
Белки составляют 30 – 70% мембраны. Если липидный бислой обусловливает преимущественно структурные особенности мембраны, то белки определяют главным образом ее специфические функции. Они находятся в мембранах в разных формах: поверхностные слабо связанные с мембраной белки, частично погруженные в мембрану белки и интегральные белки, пронизывающие мембрану. Белки способны вращаться вокруг оси, а также перемещаться в плоскости самой мембраны. Важным следствием такой подвижности служит образование кластеров (пучков) белков (например, рецепторов). Однако клетка может и ограничивать подвижность мембранных белков (например, при участии белков в образовании межклеточных контактов и при их связи с цитоскелетом клетки). Белки выполняют в плазматической мембране ферментативную функцию, участвуют в процессах транспорта (переносчики, каналы, насосы), рецепции, распознавания клеток, образования межклеточных контактов, создают ионную проницаемость и электропроводимость мембраны.
Углеводы составляют 2 – 10% мембраны. Они представляют собой олигосахаридные цепи (в их составе обнаружено около девяти моносахаридов), которые ковалентной связью присоединены к белкам (гликопротеины) и липидам (гликолипиды) на наружной поверхности мембраны. Разветвленные цепи гликолипидов создают на наружной поверхности плазмолеммы обогащенную углеводами зону, называемую гликокаликсом. Преобладающим мембранным олигосахаридом является отрицательно заряженная сиаловая (ацетилнейраминовая) кислота, которая в основном и создает отрицательный заряд наружной поверхности плазмолеммы. Функции мембранных углеводов до сих пор точно неизвестны, наиболее доказанным является их участие в процессах распознавания клеток (например, групповой принадлежности эритроцитов).
Виды и механизмы транспортных процессов.
Пассивный транспорт происходит из зоны бòльшей концентрации в зону меньшей концентрации (по уменьшающемуся градиенту концентрации) с уменьшением энергии транспортируемого вещества. Различают простую и облегченную диффузию.
Простая диффузия осуществляется через липидный бислой и ионные каналы. Через липидный бислой переносятся малые молекулы: неполярные – О2, N2, этанол, эфир и др., полярные незаряженные молекулы – Н2О, мочевина, глицерол, СО2, аммиак и др. Через ионные каналы переносятся неорганические ионы – Na+, К+, Са2+, СI- и др. При этом, кроме градиента концентрации, играет роль электрический градиент между отрицательной внутриклеточной и положительной внеклеточной средами – мембранный потенциал, который усиливает транспорт катионов и препятствует транспорту анионов в клетку, и наоборот.
Облегченная диффузия используется для переноса более крупных полярных незаряженных молекул (например, глюкозы и аминокислот). Она осуществляется с использованием белков-переносчиков, которые избирательно связывают транспортируемые молекулы и за счет конформационных изменений переносят их через мембрану. Облегченная диффузия характеризуется специфичностью, бóльшей скоростью, явлением насыщения (когда заняты все переносчики), регулируется с помощью гормонов (например, инсулином при транспорте глюкозы).
А
 ктивный
транспорт
происходит из зоны меньшей концентрации
в зону бòльшей концентрации (по
возрастающему градиенту концентрации)
с увеличением энергии транспортируемого
вещества. Различают первично-активный
и вторично-активный транспорт.
ктивный
транспорт
происходит из зоны меньшей концентрации
в зону бòльшей концентрации (по
возрастающему градиенту концентрации)
с увеличением энергии транспортируемого
вещества. Различают первично-активный
и вторично-активный транспорт.
Первично-активный транспорт непосредственно использует энергию АТФ и осуществляется деятельностью ионных насосов: калий-натриевого, кальциевого, протонного, белок которых обладает свойствами как переносчика, так и фермента АТФазы.
Вторично-активный транспорт использует энергию градиента какого-либо иона (чаще Na+), предварительно созданную деятельностью ионного насоса, для транспорта других ионов, глюкозы, аминокислот. Транспорт происходит с участием белков-переносчиков.
Микровезикулярный транспорт (эндоцитоз и экзоцитоз) является вариантом активного транспорта, служит для переноса через мембрану крупномолекулярных веществ (например, белков).
Эндоцитоз выполняет питательную, защитную, регуляторную функции (последняя связана с изменением количества рецепторов мембраны и эндоцитозом гормонов, не проникающих через мембрану). При эндоцитозе локальный участок плазматической мембраны впячивается и отшнуровывается, формируя эндоцитозные пузырьки. Обычно эндоцитозные пузырьки сливаются с первичными лизосомами, образуя вторичные лизосомы, в которых переваривается макромолекулярное содержимое пузырьков. Выделяют три вида эндоцитоза – пиноцитоз, опосредованный рецепторами эндоцитоз и фагоцитоз.
При пиноцитозе происходит неспецифический захват внеклеточной жидкости и растворенных в ней веществ (в том числе и макромолекул), которые используются внутри клетки или переносятся сквозь клетку.
При опосредуемом рецепторами эндоцитозе вещества (например, липопротеины, незрелый тироглобулин, гормоны, иммуноглобулины, антигены) сначала связываются со специфическими белками-рецепторами плазматической мембраны, которые далее концентрируются в окаймленных ямках мембраны (окаймление совершается особым белком – кластрином, обладающим свойством АТФазы). После впячивания и отшнуровывания образуются окаймленные пузырьки (эндосомы), взаимодействующие с лизосомами.
При фагоцитозе (И.И. Мечников, 1883) крупные клеточные частицы (обломки своих клеток, инфекционные агенты и др.) захватываются «профессиональными» клетками (микро- и макрофагами) с дальнейшим внутриклеточным перевариванием.
Экзоцитоз используется для выделения из клеток медиаторов, гормонов, ферментов, которые используются в организме в регуляторных, питательных и других целях. Их выделение из клетки происходит в составе экзоцитозных пузырьков, образующихся в комплексе Гольджи. В этих пузырьках упаковываются белки, образовавшиеся в шероховатой ЭПС. Низкомолекулярные вещества (медиаторы, некоторые гормоны и др.) попадают в пузырьки преимущественно путем вторично-активного транспорта. Пузырьки транспортируются с помощью микрофиламентов и микротрубочек к плазмолемме, сливаются с ней, и содержимое пузырьков выделяется во внеклеточную среду. Важным регулятором экзоцитозной активности является уровень внутриклеточного Са2+, определяемый нервными и эндокринными влияниями на клетку.
Рецепторная функция клетки осуществляется специальными белками, которые находятся преимущественно на плазмолемме, а также в цитоплазме и ядре (для проникающих в клетку гормонов). Через эти рецепторы клетки воспринимают различные раздражители: химические (например, гормоны и медиаторы), физические (например, фотоны), биологические (например, микробы и вирусы).
Главные виды рецепторов плазмолеммы.
Ионотропные рецепторы («рецепторы-каналы») в своем составе имеют ионные каналы, расположены преимущественно в области синапсов, участвуют в передаче возбуждающих и тормозных влияний (Н-холинорецепторы, ГАМКА- рецепторы, глутаматные НМДА-рецепторы, глициновые рецепторы и др.).
Метаботропные рецепторы – через них действуют около 80 % гормонов и медиаторов, которые плохо проникают в клетку и формируют внутриклеточные эффекты преимущественно с помощью вторых посредников (подробно в 7.4, п. 2).
Рецепторы, регулирующие поступление молекул в клетку (например, липидов в составе липопротеинов низкой и высокой плотности).
Адгезивные рецепторы (семейства интегринов – СD61, кадгеринов, иммуноглобулинов, кластеров дифференцировки – СD54, СD242, селектинов СD62) – осуществляют связь «клетка - клетка» и «клетка – структуры межклеточной среды» (например, с базальной мембраной).
Регуляция рецепторной функции плазмолеммы. Эта функция на клеточном уровне может быть снижена (десенситизация рецепторов) или усилена (сенситизация рецепторов).
Десенситизация рецепторов возникает при усилении сигнала или увеличении времени его действия на рецептор. Она может быть связана с действием ферментов протеинкиназ, фосфорилирующих рецепторы, что может снижать их чувствительность к сигнальным молекулам. Другим механизмом является эндоцитоз комплексов «сигнальная молекула+рецептор», что уменьшает количество рецепторов на плазмолемме (интернализация рецепторов). Десенситизацию рецепторов может вызвать инактивирующая мутация генов, кодирующих данные рецепторы.
Сенситизация рецепторов может быть связана с увеличением синтеза рецепторов, активирующей мутации кодирующих их генов, с увеличением сопряженности рецептора с G-белком и вторыми посредниками, а также с протеолизом белков, блокирующих рецепторы.
Рецепторы цитоплазмы и ядра клетки стимулируются сигнальными молекулами, легко проникающими в клетку – стероидными и тироидными гормонами, витаминами D3 и А. Они представляют собой белки (факторы транскрипции), действующие в ядре клетки. Каждый рецептор содержит три главных специфических участка (домена): ДНК-связывающий, лигандсвязывающий и активирующий транскрипцию. Через эти рецепторы стимул становится фактором регуляции транскрипции (синтеза иРНК) в каких-либо генах. Физиологические эффекты таких лигандов (например, гормонов) осуществляются в результате экспрессии или репрессии десятков и сотен генов-мишеней, чувствительных к данному гормону.
Энергетическая функция клетки. Клетки для осуществления своих функций могут использовать две главные формы энергии: аккумулированную в высокоэргических связях АТФ и в виде энергии ионных трансмембранных градиентов. Энергия связей АТФ (7,3 ккал/моль) используется для различных видов работы клетки: биосинтетической, сократительной, электрической, осмотической, работы ионных насосов, создания ионных трансмембранных градиентов и др. Энергия трансмембранных ионных градиентов непосредственно используется для создания биопотенциалов и транспорта веществ через мембрану (вторично-активного транспорта).
Митохондрии играют главную роль в энергетическом обмене. Они окисляют пируват и жирные кислоты (через ацетил-КоА) в цикле трикарбоновых кислот, образуя активные формы водорода (в составе НАДН, частично ФАДН2). Их электроны поступают в цепь дыхательных ферментов внутренней мембраны митохондрий, а протоны – в матрикс. Энергия, освобождающаяся при транспорте электронов в дыхательной цепи, используется для создания протонного градиента по обе стороны внутренней мембраны. Энергия этого градиента во время обратного потока протонов через протонный канал АТФ-синтетазы используется для фосфорилирования АДФ, в результате чего образуется АТФ. (например, при окислении одной молекулы глюкозы с участием митохондрий образуется до 36 молекул АТФ.) Часть энергии АТФ резервируется в виде креатинфосфата и ионных градиентов клетки.
Энергетическая функция цитозоля связана с гликолизом: окисление одной молекулы глюкозы приводит в конечном балансе к образованию двух молекул АТФ и молекулы НАДН, водород которой может использоваться в митохондриях. Образование АТФ в цитозоле происходит как в аэробных, так и в анаэробных условиях. Таким образом, хотя гликолиз имеет малую эффективность образования АТФ по сравнению с митохондриями, важной его особенностью является малая зависимость от кислородного состояния клетки.
