
- •Аналитическая химия Методические указания к лабораторным работам
- •110900.62 «Технология производства и переработки сельскохозяйственной продукции»,
- •250100.62 «Лесное дело», 020400.62 «Биология»,
- •022000.62 «Экология и природопользование»
- •Титриметрические методы анализа
- •Кислотно-основное титрование
- •Лабораторная работа № 1 Тема: «Ацидиметрия»
- •1. Приготовление и стандартизация раствора hCl.
- •Стандартизация раствора hCl по тетраборату натрия
- •Согласно реакции:
- •Определение карбоната и гидрокарбоната в их смеси
- •Лабораторная работа № 2 Тема: «Алкалиметрия»
- •1. Приготовление и стандартизация раствора щелочи.
- •Стандартизация растворов щелочей
- •Определение хлороводородной и борной кислот при совместном присутствии
- •Окислительно – восстановительное титрование
- •Лабораторная работа № 3 Тема: «перманганатометрия»
- •Этот способ титрования также редко применяется (для определения некоторых органических веществ).
- •Приготовление и стандартизация раствора kMnO4
- •Определение массовой доли нитритов в растворе
- •1 С п о с о б (прямое титрование)
- •2 С п о с о б (обратное титрование)
- •Лабораторная работа № 4 Тема: «иодиметрия и иодометрия»
- •Приготовление и стандартизация раствора тиосульфата натрия
- •Приготовление раствора крахмала
- •Приготовление и стандартизация раствора иода
- •Комплексонометрическое титрование
- •Лабораторная работа № 5 Тема: «Комплексонометрическое титрование»
- •1 Приготовление и стандартизация раствора комплексона III
- •Голубой красно-
- •Задача 2 Определение общей жесткости воды
- •Задача 3 Комплексонометрическое определение кальция и магния в смеси
- •Осадительное титрование
- •Лабораторная работа № 6 Тема: «Осадительное титрование
- •Гравиметрический метод анализа принцип метода
- •Способ отгонки определяемого компонента
- •Лабораторная работа № 8 Тема: «определение массовой доли бария в дигидрате хлорида бария»
- •Аналитические весы и взвешивание
- •Классификация весов
- •Устройство и принцип действия рычажных призменных весов
- •2.1. Устройство двухчашечных весов.
- •2.2. Принцип действия рычажных весов.
- •Техника взвешивания
- •Бумажная хроматография
- •Лабораторная работа № 9 Тема: разделение и обнаружение катионов
Лабораторная работа № 8 Тема: «определение массовой доли бария в дигидрате хлорида бария»
Определение основано на осаждении ионов бария сульфат-ионами:
Ba 2+ + SO42- BaSO4
Сульфат бария – наименее растворимое из труднорастворимых соединений бария ( Кs = 1,1 10-10 ), он практически нерастворим в кислотах, имеет строго определенный состав, соответствующий формуле BaSO4. При прокаливании состав сульфата бария не меняется, следовательно, гравиметрическая форма совпадает с формой осаждения. Сульфат бария как в качестве осаждаемой, так и в качестве гравиметрической формы отвечает всем требованиям, которые к ним предъявляются. В качестве осадителя предпочитают серную кислоту, учитывая ее летучесть. Но поскольку BaSO4 по своей природе – мелкокристаллическое вещество, необходимо при осаждении обратить особое внимание на создание условий, обеспечивающих получение более крупных кристаллов.
Фильтруют осадок через плотный фильтр («синяя лента»). Вначале промывают осадок от ионов CI- горячей дистиллированной водой, в которую добавлена серная кислота, а затем от ионов SO42- горячей дистиллированной водой. Поскольку плохо отмытые остатки серной кислоты вызывают хрупкость фильтра при его высушивании, можно рекомендовать добавление в дистиллированную воду нитрата аммония. Осадок прокаливается вместе с фильтром при температуре 600–800 0С. При этом возможны следующие нежелательные процессы:
При озолении фильтра осадок BaSO4 частично восстанавливается углем до BaS: BaSO4 + 2C BaS + 2CO2
При прокаливании осадка кислород воздуха вновь окисляет BaS:
BaS + 2O2 BaSO4
Слишком высокая температура прокаливания приводит к разложению части осадка: BaSO4 BaO + SO3
Прокаливание тигля с осадком проводится до тех пор, пока не будет получена постоянная масса, что указывает на то, что эти побочные процессы закончились, и осадок не содержит примесей, удаляемых прокаливанием.
Х о д а н а л и з а
Расчет
навески. Сульфат бария – кристаллический
осадок, рекомендуемая масса которого
0,4–0,5 г.![]()
Согласно уравнению реакции
BaCl2 + H2SO4 BaSO4 + 2HCl
рассчитать массу навески BaCl2 2H2O.
Расчет объема осадителя. Согласно уравнению реакции рассчитывается необходимая масса безводной серной кислоты, которая бы полностью осадила рассчитанную массу навески хлорида бария.
Затем рассчитывается необходимый объем раствора серной кислоты
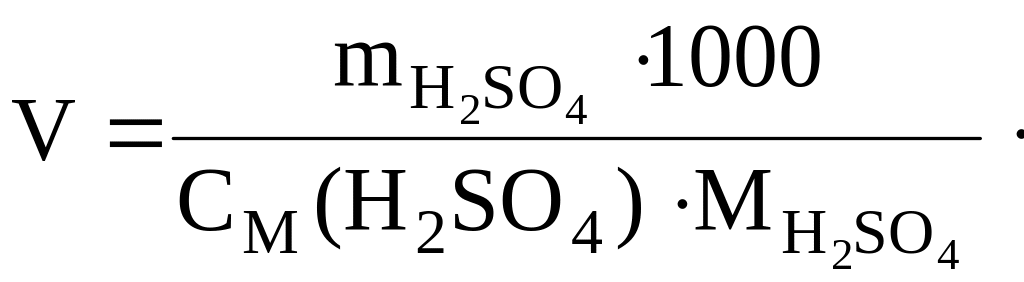
Хотя осадок BaSO4 имеет достаточно низкую растворимость, однако возможны его потери, обусловленные растворением осадка. Поэтому необходим избыток осадителя (полуторократный), который понижает растворимость осадка и при прокаливании может быть удален.
Взятие навески. Сначала берут навеску на технохимических весах и переносят ее в бюкс (при этом бюкс предварительно не взвешивают). Затем взвешивают бюкс с навеской на аналитических весах с точностью до 0,0001 г и переносят навеску в химический стакан для растворения. Не обмывая бюкс дистиллированной водой, его взвешивают с оставшимися крупинками вещества на аналитических весах и по разности масс находят массу вещества, взятого для анализа (массу навески).
Растворение навески. Поскольку осаждение должно проводиться из разбавленного раствора (массовая доля BaCl2 в растворе не должна превышать 0,5–1,0 %), в химический стакан с навеской добавляют 150 мл дистиллированной воды. В полученный раствор добавляют 2–3 мл 2 М HCl, для повышения растворимости сульфата бария на первых этапах осаждения, раствор перемешивают стеклянной палочкой. После этого палочку до конца осаждения из стакана не вынимают.
Осаждение. Параллельно с этим в другом химическом стакане готовят раствор серной кислоты (осадителя): отмеривают пипеткой рассчитанный объем серной кислоты и разбавляют его 30 мл дистиллированной воды. Содержимое обоих стаканов нагревают на водяной бане до 70 0С и затем горячий раствор кислоты медленно, по каплям, по палочке, приливают в анализируемый раствор BaCl2, постоянно перемешивая. Закончив осаждение, стакан (вместе с палочкой) вновь ставят на водяную баню до просветления раствора, после чего делают пробу на полноту осаждения ионов бария, прибавляя к прозрачному раствору над осадком 2–3 капли раствора серной кислоты. Отсутствие помутнения – признак полного осаждения бария. При наличии помутнения прибавляют дополнительный объем разбавленного раствора кислоты, перемешивают, дают отстояться и снова проверяют полноту осаждения. Когда полнота осаждения будет достигнута, стакан с палочкой закрывают бумагой и оставляют осадок для созревания до следующего занятия.
Если необходимо ускорить процесс созревания осадка, стакан с содержимым нужно оставить на водяной бане на 1–2 ч, периодически перемешивая осадок. Но перед фильтрованием раствор следует охладить.
Фильтрование и промывание осадка. Собрать установку для фильтрования. К чистой и сухой воронке подгоняют беззольный фильтр «синяя лента», помня, что края фильтра не должны доходить до края воронки на 0,5–1 см. Для собирания фильтрата под воронку подставляют стакан, в котором готовился раствор осадителя. В промывалке готовят промывную жидкость (на 200 мл воды прибавляют 1–2 мл 1 М H2SO4) и нагревают ее на водяной бане. Декантировав всю жидкость с осадка на фильтр, приступают к его промыванию в стакане, каждый раз прибавляя 15–20 мл промывной жидкости и декантируя жидкость на фильтр. Промывание проводят 2–3 раза, периодически выливая из стакана собранный фильтрат, убеждаясь, что он прозрачный. Затем делают пробу на полноту удаления ионов Cl-. С этой целью в пробирку собирают 1–2 мл фильтрата и добавляют 1–2 капли 1% раствора AgNO3 (в присутствии HNO3). Если фильтрат при этом помутнел, промывание продолжают до тех пор, пока не будет получена отрицательная реакция на ион Cl-. После этого осадок количественно переносят на фильтр, стараясь не потерять при этом ни одной капли раствора с осадком. На фильтре осадок промывают несколько раз горячей дистиллированной водой для удаления ионов SO42-. Заканчивают промывание при отрицательной пробе в фильтрате на ион SO42- (отсутствие помутнения при добавлении к фильтрату хлорида бария).
Высушивание и прокаливание осадка. Параллельно с фильтрованием и промыванием осадка доводят тигли до постоянной массы, прокаливая их в муфельной печи при той же температуре, при которой будет проводиться прокаливание осадка.
Осадок на воронке подсушивают в сушильном шкафу и переносят его вместе с фильтром в подготовленный тигель. Воронка при высушивании осадка должна быть закрыта листом фильтровальной бумаги. Поместив фильтр с осадком в тигель, фильтр озоляют при слабом нагревании, не давая ему воспламеняться. Озоление проводят под тягой на пламени горелки или на электроплите. Тигель с озоленным фильтром тигельными щипцами переносят в муфельную печь, нагретую до 600–800 0С. Прокалив тигель с осадком 40–45 мин, его охлаждают в эксикаторе и взвешивают на аналитических весах. Операцию повторяют, уменьшив продолжительность прокаливания до 10–15 мин, до тех пор, пока не будет получена постоянная масса тигля с осадком, т. е. пока разность массы тигля с осадком двух последних взвешиваний не превысит 0,2 мг.
Расчет результатов анализа. По разности полученных масс прокаленного тигля с осадком и пустого тигля находят массу осадка BaSO4. Зная массу анализируемой навески и массу осадка, можно вычислить массовые доли (%):
(Ba2+) = moc. F 100 / mн; F = M(Ba) / M(BaSO4)
(Ba2+)теор. = .F 100; F = M(Ba) / M(BaCl2 2H2O)
Отчет выполнить в виде таблицы:
mн |
m (H2SO4) |
V (H2SO4) |
m тигля |
m тигля с осадком |
mос. |
(Ba),% |
Теор. (Ba), % |
Абс. погреш. |
Отн. по- греш. |
|
|
|
1. |
1. |
|
|
|
|
|
|
|
|
2. |
2. |
|
|
|
|
|
Вывод (см. ЛР № 7).
ПРИЛОЖЕНИЕ
