
- •31. Патологічна фізіологія печінки
- •II. Недостатнє виведення тригліцеридів і ь
- •32. Патологічна фізіологія нирок
- •32.28. Які наслідки для організму може мати втрата білків із сечею при нефротичному синдромі?
- •33. Патологічна фізіологія ендокринної системи
- •Механізми регуляції
- •Зовнішні сигнали
- •Кровотеча
- •Стреоори
- •34. Патологічна фізіологія нервової системи
Фізичне
навантаження
Гіпоглікемія
//
Інфекція
ХолодКровотеча

Біль
ч\
4—
Токсини
Травма
—►
Вищі регуляторні центри і
Загальний адаптаційний синдром
Рис. 155. Фактори, що викликають стрес
33.40. Які стадії виділяють у розвитку стресу?
Стадія тривоги:
а) підстадія шоку. Характеризується короткочасним зменшенням резистентності до патогенного фактора;
б) підстадія контршоку. Опірність організму спочатку поновлюється, а потім підвищується.
Стадія резистеитиості. Характеризується стійким і тривалим збільшенням опірності організму як до фактора, що викликав стрес, так і до інших патогенних агентів.
Стадія виснаження. Настає при дуже інтенсивній або тривалій дії патогенного фактора, а також в умовах функціональної слабкості адаптаційних механізмів. Супроводжується зменшенням резистентності організму до патогенних впливів (рис. 156).
Нормальний
рівень опірності
Рис.
156. Стадії загального
адаптаційного синдрому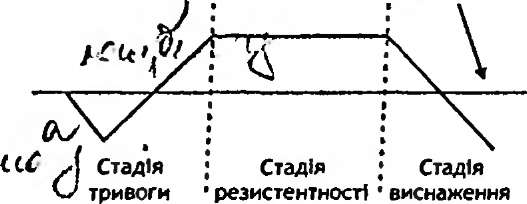
33.41. Які механізми беруть участь у реалізації стресу?
Численні ініціатори стресу (стресори) - травма, холод, біль, емоції, кровотеча, фізичне навантаження, гіпоглікемія, інфекції та ін.—через порушення гомеостазу або передвісників такого порушення викликають збудження вищих нервових регуля-
прних центрів і пов'язане з цнм вивільнення великої кількості гормонів. При цьому іелине значених мають такі процеси.
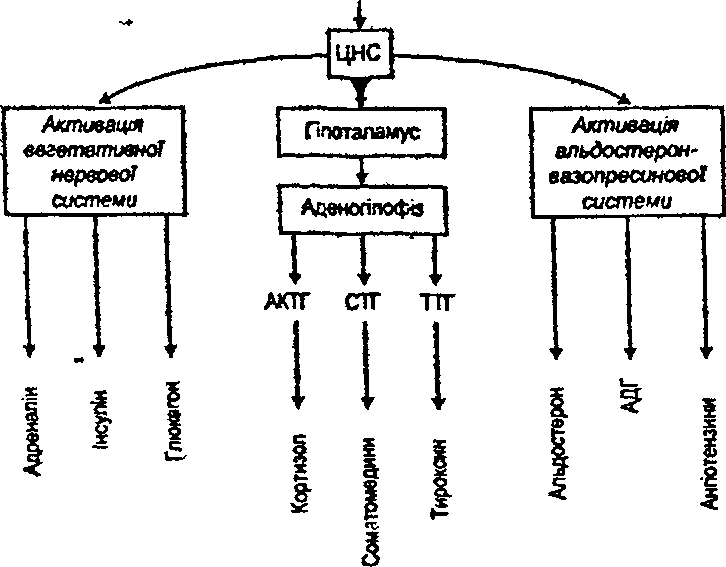
І Активація системи апотаяамус-аденогіпофіз. Як наслідок відбувається виділення АКТГ, СТГ, ТТГ, які відповідно стимулюють секрецію глюкокортикоїдів, сомзтомсдинів, тирсоїдних гормонів. 1. Активація вегетативної нервової системи (симпатичної і парасимпатичної*) супроводжується надходженням у кров катехол амінів, інсуліну, глюкагону. П. Активація альдостерон-вазопресинової системи веде до збільшення вмісту в крові ангіотензинів, альдостерону, вазопресину (АДГ) (рис. 157).
Рис
157. У реалізації стресу
беруть участь різні гормониСтреоори
33.42, Яка участь різних гормонів у розвитку стресу?
V Гормони, що виділяються під час стресу, визначають розвиток трьох послідовних фаз цій реакції.
І. Гостра фаза. Гормони, що вивільнюються в шо фазу, забезпечують захист від падіння артеріального тиску і об'єму циркулюючої крові. Це досягається збільшенням загального периферичного опору і збереженням води в організмі. Зазначені реакції пов'язані з посиленим надходженням кров катехаламінів, глюкокортикоїдів, ангіотсвднну П, альдостерону, вазопресину.
1Ь Під гостра фаза. Характеризується мобілізацією ресурсів для енергетичного і пластичного забезпечення систем, що здійснюють адаптацію. Цьому слугує перерозподіл зазначених ресурсів між активно функціонуючими органами (серце, головний мозок) і структурами, шо перебувають у відносному спокої (скелетні
м'язи, травний канал, лімфоїдна і жирова тканини). Метаболічні зміни е цю фазу обумовлені збільшенням секреції катехоламінів, ппококортякоїдш, глюкагону і зменшенням виділення інсуліну Наведені вище хонтрінсулярні гормони, посилюючи гпікогеноліз, шюконеогенез, ліполіз і протеоліз, викликають збільшбкия вмісту в крові глюкози, амінокислот, вільних жирових кислот. III. Фаза довгострокової адаптації Характеризується структурним» змінами (гіпертрофією, гіперплазією) органів і тканин, що забезпечують адаптацію і перебувають у стані гіперфункції. У її реалізації беруть участь інсулін, СТГ, соматомедини, тиреоїдні гормони, фактори росту - істинні та тканинні гормони, що активують анаболічні процеси і формують так званий структурний слід адаптації.
33.43. Що таке "хвороби адаптації"? Які захворювання до них відносять?
Хвороби адаптації — це захворювання, у розвитку яких провідна роль належить надмірному стресу і так званим стресорним механізмам ушкодження.
Прн великій інтенсивності і тривалості стрес із механізму адаптації може перетворитися у механізм патогенезу.
До хвороб адаптації відносять:
а) психосоматичні захворювання (ішемічну хворобу серця, гіпертонічну хворобу, виразкову хворобу шлунку і дванадцятипалої кишки);
б) хвороби обміну речовин (цукровий діабет);
в) алергічні І запальні захворювання (бронхі- ^ажень серЧебо*удинн<* системи альну астму, ревматизм).
33.44. Назвіть гормони щитоподібної залози. Як здійснюється регуляція їх утворення і секреції?
У щитоподібній залозі утворюються тиреоїдні гормони - тироксин (Т^) і три* йодтиронін (Т,). Крім того, С-клітинами (парафолікулярними) синтезується кольці*- тонім, який бере участь у регуляції фосфорно-кальцієвого обміну (див. розд. 24).
Вважають, що тироксин е прогормоном трийодтироиіну. На думку про це наводять такі факти:
а) Т, в 5 разів активніший, ніж Т4;
б) ефекти Т4 розвиваються після більш тривалого латентного періоду, якщо порівнювати зі змінами, що їх викликає Т,;
Рис.
158. Іммобілізащйний
стрес використовують для моделювання
Регуляція утворення і секреції тиреоїдних гормонів здійснюється системою гі- поталамус-аденогіпофіз за схемою: гіпоталамус —♦ тиреоліберин —♦ аденогіпофіз тиреотропний гормон (ТТГ) щитоподібна залоза. ТТГ, діючи на щитоподібну залозу викликає такі ефекти:
а) посилює захоплення і введення йоду в органічні сполуки;
б) посилює протеоліз депонованого тирео глобуліну;
в) посилює секрецію Т, і Т^
г) у разі тривалої дії викликає гіпертрофію й гіперплазію щитоподібної залози.
33.45. Які механізми діїй біологічні ефекти тиреоїдних гормонів?
Тиреоїдні гормони є гормонами з внутрішньоклітинним типом циторецепції. Установлено три внутрішньоклітинні мішені для їхньої дії: плазматична мембрана, мітохондрії, ядро.
На плазматичній мембрані чутливих до тиреоїдних гормонів клітин виявлено високоафінні ділянки зв'язування трийодгироніну (Т^. Результатом взаємодії Т3 з такими ділянками є стимуляція транспорту амінокислот. Відповідь виникає дуже швидко і не вимагає синтезу відповідних інформаційної РНК і білка.
У мітохондріях Т4 зв'язується з ферментом внутрішньої мембрани - транслока- зою аденінових нуклеотидів -і активує його. Наслідком цього є посилення транспорту АДФ із цитоплазми в мітохондрії. В результаті концентрація АДФ у мітохондріях зростає, що викликає збільшення інтенсивності біологічного окиснення (принцип акцепториого контролю).
Ядро є основною внутрішньоклітинною мішенню для Т,. Це визначає довгострокові ефекти тиреоїдних гормонів. При зв'язуванні Т, (у меншій мірі Т<) з ядеринми рецепторами відбувається індукція транскрипції і синтезу цілого ряду функціонально важливих білків. Серед них;
а) Ш-К-АТФ-аза плазматичних мембран;
б) ферменти літогенезу (зокрема, НАДФ-малатдегідрогеназа);
в) ферменти мітохондрій (а-гшцерофосфатдегідрогеназа);
г) білкові компоненти р-адренорецетгторів.
Усі біологічні ефекти, обумовлені дією тиреоїдних гормонів на клітини, можна поділити на три групи.
Аиаболічиа дія - вплив на ріст і диференціювання тканин. Є низькодозовим ефектом. Відсутність цього ефекту або його зменшення виявляється прн гіпотиреозі.
Метаболічні ефекти - збільшення інтенсивності катаболічних процесів (окисиення, ліполізу). Будучи високодозовими, вони виявляються в умовах гіпертиреозу.
Ш. Сенсибілізуючі ефекти-збільшення чутливості клітин ДО ДІЇ інших гормонів, зокрема естрогенів і катехоламінів. Щодо останніх сенсибілізуючий вплив тиреоїдних гормонів пов'язаний зі збільшенням кількості р-адренорецепторів на поверхні клітин.
Назвіть основні причини гіпотиреозу.
В основі розвитку гіпофункції щитоподібної залози - гіпотиреозу - можуть лежати такі причини.
Центральні порушення: зменшення утворення і секреції тиреоліберину і тире* етропного гормону (ТТГ) у зв'язку з розладами діяльності гіпоталамуса і адеиогіпофіза (вторинний гіпотиреоз).
Залозисті порушення, що призводять до розвитку первинного гіпотиреозу.
а) руйнування тканини залози, наприклад, радіоактивним йодом;
б) дефіцит йоду в питній воді та їжі - ендемічний зоб;
в) аутоімунне ушкодження клітин залози - аутоімунний тиреоїдит Хашимотог,
г) уроджені порушення - гіпо- і аплазія щитоподібної залози, ензимопатіГ.
Периферичні порушення:
а) нечутливість периферичних клітин до дії тиреоїдних гормонів;
б) підвищене зв'язування тиреоїдних гормонів білками плазми крові;
в) посилений їх метаболізм у печінці.
Який патогенез основних проявів гіпотиреозу?
У розвитку проявів гіпотиреозу мають значення такі механізми.
Порушення росту і диференціювання тканин. При цьому важливу роль віді
грають випадіння низькодозових (анаболічних) ефектів тиреоїдних гормонів і зменшення секреції СТГ.
Оскільки тиреоїдні гормони потрібні для нормального процесу енхондральної осифікації на межі діафіза й епіфіза, то в умовах гіпотиреозу порушується ріст кісток у довжину. При цьому неріостальиий ріст кісток зберігається, у зв'язку 5 чим вони стають товстими. Розвивається комплекс змін скелета - гіпотиреоїдна карликовість.
Поряд з цим затримується і розумовий розвиток - поступово виникає кретинізм.
Зменшення теплоутворювальної дії тиреоїдних гормонів, що виявляється:
а) зменшенням основного обміну (падіння на 20-40 %). Воно обумовлено зниженням інтенсивності біологічного окиснения в мітохондріях і функціональної активності збудливих ткаиии;
б) зменшенням теплопродукції, у зв'язку з чим падає температура тіла;
в) поганою адаптацією до холоду при збереженні адаптації до високої температури; і »
г) гіпофагією - малим споживанням енергетичних ресурсів.
Зменшення функціональної активності збудливих тканин. Пов'язане з падінням активності №-К-АТФ-аз і змінами процесів активного транспорту іонів. З другого боку, має значення зменшення чутливості тканин до катехоламінів, що обумовлено зменшенням кількості Р-адреиорецепторів иа клітинах. Функціональні зміни збудливих органів і тканин виявляються:
а) порушеннями діяльності центральної нервове» системи - уповільненням розумової діяльності, млявістю, загальмованістю, сонливістю і т. о.;
б) зменшенням функціональної активності скелетних м'язів — слабкістю, зменшенням тонусу, швидкою стомлюваністю;
в) порушеннями діяльності серцево-судинної системи - брадикардією, змен- * шеиням хвилинного об'єму серця, падінням артеріального тиску;
г) зменшенням скорочувальної функції гладких м'язів кишок - закрепами;
ґ) порушеннями процесів всмоктування і екскреції Зменшення всмоктування ппокози в кишках призводить до гіпоглікемії, а порушення екскреції холестеролу в складі жовчі— до гіперхолестеролемії і атеросклерозу. IV. Порушення з нез'ясоваиими механізмами розвитку. До них відносять слизовий набряк-мікседему. Характеризується збільшенням у тканинах кількості глі- козаміногліканів, що зв'язують воду, потовщенням шкіри, одутлим обличчям. Існує гіпотеза, згідно з якою мікседема є наслідком дії на сполучну тканину тире- отропного гормону (ТТГ), кількість якого при власне залозистій і периферичній формах гіпотиреозу істотно зростає.
33.48. Назвіть основні причини гіпертиреозу.
В основі розвитку гіпертиреозу можуть бути такі причини. Ь Центральні порушення - збільшення секреції тиреоліберину і тнреотропного гормону (ТТТ) при гіперфункції гіпоталамуса і аденогіпофіза (вторинний гіпертиреоз).
II. Власне залозисті порушення (первинний гіпертиреоз). Найпоширенішими клінічними формами первинного гіпертиреозу є дифузний токсичний зоб (хвороба Гревса, базедова хвороба) та аденоми щитоподібної залози. Вважають, що дифузний токсичний зоб є аутоімунним захворюванням, у виникненні якого мають значення ТТГ-міметичні антитіла, тобто антитіла, що імітують дію ТТГ при взаємодії з поверхневими антигенами клітин щитоподібної залози (V тип алергічних реакцій за Кумбсом і Джеллом). На роль таких антитіл претендують ІАТ8 (1оп§ ас(іп£ іЬугоіс! зіітиіаіог) і ТЗІ (іЬугоі<1 $1іти1а(іп£ ітт- ипо^ІоЬиІшеХ здатні взаємодіяти із 11 і -рецепторами. Оскільки ці антитіла ие мають міст, зв'язування комплементу, то клітини щитоподібної залози не ушкоджуються, а активно функціонують. III. Периферичні порушення:
а) збільшення чутливості клітин до дії Т, і Т^
б) зменшення зв'язування тиреоїдних гормонів транспортними білками;
в) уповільнення метаболізму тиреоїдних гормонів у печінці при ЇЇ недостатності.
33.49. Який патогенез основних проявів гіпертиреозу?
У патогенезі проявів гіпертиреозу мають значення такі механізми. І. Антианаболічні ефекти. Є високодозовими ефектами тиреоїдних гормонів. До них відносять:
а) затримку росту;
б) атрофію м'язів і слабкість;
в) схуднення;
г) негативний азотистий баланс.
Посилення теплоутворювальної дії тиреоїдних гормонів. Воно виявляється:
а) збільшенням основного обміну;
б) збільшенням теплоутворення й підвищенням температури тіла;
в) збереженою адаптацією до холоду і поганою - до високої температури;
г) гіперфагією - підвищеним споживанням енергетичних ресурсів.
Збільшення функціональної активності збудливих тканин. Пов'язане з підвищенням активності Ка-К-иасосів клітинних мембран і збільшенням чутливості клітин до катехоламінів. Цим, зокрема, обумовлені такі прояви гіпертиреозу:
а) порушення діяльності центральної нервової системи - прискорення психічних процесів, занепокоєння, збудження, безсоння;
б) постійна спонтанна скорочувальна активність волокон скелетних м'язів- фібрилярні посмикування, тремор. З цим пов'язана м'язова слабкість, стомлюваність; «
в) зміни діяльності серцево-судинної системи - тахікардія, збільшення хвилинного об'єму серця, артеріального тиску; -
г) підвищення скорочувальної активності гладких м'язів кишок - проноси;
ґ) збільшення інтенсивності процесів усмоктування і екскреції. З цим, зокрема, пов'язана гіперглікемія і гіпохолестеролемія.
Катехоламінові ефекти. Обумовлені підвищенням чутливості клітин до дії катехоламінів у зв'язку зі збільшенням иа клітинній поверхні кількості [)-адреноре- цепторів.
У клініці гіпертиреозу велике значення мають функціональні ефекти катехоламінів, зокрема, їхній вплив на серцево-судинну систему (див. запит. 33.36), і метаболічні зміни. З останніми пов'язані такі порушення:
а) посилення глікогенолізу в печінці —»гіперглікемія —»гіперфункція Р-клітин острівців підшлункової залози з наступним їх виснаженням —»тиреоїдний цукровий діабет;
б) посилення ліполізу в жировій тканині —» гіперліпацидемія —» збільшення кетогенезу в печінці —» метаболічний ацидоз;
в) активація не пов'язаного з фосфоруванням окиснеиня в бурій жировій тканині —»збільшення теплопродукції —»підвищення температури тіла і основного обміну.
Порушення з нез'ясованими механізмами розвитку - орбітопатія Г двосто
ронній екзофтальм (витрішкуватість). В основі їхнього розвитку - набряк і лім- фоїдна інфільтрація м'язів очного яблука і ретробульбарної тканини. Ці зміни не залежать від концентрації тиреоїдних гормонів у плазмі крові і від рівня ТТГ-мі- метичних антитіл (ЬАТЗ, ТЗІ). Вважали, що в умовах гіпертиреозу виділяється особливий екзофтальмічний фактор, однак його дотепер не виявлена
33.50. Що таке зоб? Які його види виділяють ? Який патогенез ендемічного зоба?
Зобом називають видиме збільшення щитоподібної залози. Виділяють три види зоба.
Дифузний токсичний зоб - гіпертиреоідний (хвороба Гревса, базедова хвороба). Характеризується ознаками гіперфункції щитоподібної залози.
Спорадичний зоб -еутиреоїдний. Збільшення маси щитоподібної залози не супроводжується вираженими змінами її функціональної активності.
Ендемічний зоб » гіпотиреоїдний. Виявляє себе клінікою гіпофункції щитоподібної задози.
Причиною ендемічного зоба є недостатній вміст йоду в питній воді і продуктах харчування, що пов'язано з особливостями ґрунту і підземних вод у певних регіонах і місцевостях земної кулі Дефіцит йоду призводить до порушення утворення тиреоїдних гормонів, вміст яких у крові зменшується. Це викликає посилення продукції тиреоліберину і тиреотропного гормону (ТТГ). Останній, впливаючи на тканину щитоподібної залози, стимулює процеси гіпертрофії і гіперплазії - розвивається зоб. Оскільки збільшення залози не усуває дефіцит тиреоїдних гормонів (причину - недостатність йоду - не ліквідовано), то підвищена продукція ТТГ зберігається і триває його дія на тканину залози: зоб прогресує,
33.51. Як здійснюється регуляція утворення і секреції паратирину прищитоподібними залозами? Назвіть основні біологічні ефекти паратгормону.
Утворення і секреція паратирину (паратгормону) регулюється вмістом іонів кальцію в плазмі крові. Секреція цього гормону зростає при зменшенні концентрації іонів Са1* у плазмі, і навпаки, зменшується при збільшенні вмісту цих іонів. Крім того, вивільнення паратирину в кров пригнічує 24Д5-(ОН)І вітамін О, що утворюється в нирках (див. розд. 24),
Біологічні ефекти паратирину (докладно див. розд. 24):
Дія на кісткову тканину - активація функції остеокластів.
Дія на нирки - пригнічення реабсорбції фосфату.
Активація перетворення в нирках вітаміну О у його гормональну форму — 1,25- (ОН)2 вітамін Б.
Наслідком усіх зазначених ефектів є збільшення концентрації іонів кальцію в плазмі крові.
33.52. Які причини і чим виявляє себе гіпопаратиреоз?
Причини гіпопаратиреозу - гіпофункції прищитоподібних залоз:
випадкове ушкодження або видалення прищитоподібних залоз при операціях на щитоподібній залозі;
ушкодження прищитоподібних залоз при лікуванні радіоактивним йодом хвороб щитоподібної залози;
аутоімунні ушкодження прищитоподібних залоз;
уроджене недорозвинення прищитоподібних залоз;
нечутливість клітин-мішеией до дії паратирину — псевдогіпопаратиреоз.
Основним проявом гіпопаратиреозу є гіпокальцісмія. Вона обумовлює розвиток паратиреопривної тетанії, що виявляється різким підвищенням нервово-м'язової збудливості, множинними фібрилярними скороченнями м'язів усього тіла. Потім виникають напади клонічних судом, що переходять у тонічні. Судомні скорочення можуть поширюватися і на внутрішні органи (пілороспазм, ларингоспазм). Під час одного з таких нападів настає смерть.
При хронічному гіпопаратиреозі у тварин розвивається клінічна картина порати* реопривної кахексії. Вона характеризується схудненням, анорексією, підвищеною иер- вово-м'язовою збудливістю, диспепсією й різноманітними трофічними порушеннями.
Які причини і чим виявляє себе гіперпаратиреоз? Причини гіперпаратиреозу - гіперфункції прищитоподібних залоз:
пухлина - аденома прищитоподібної залози;
гіперфункція прищитоподібних залоз, обумовлена зменшенням чутливості їхніх ендокринних клітин до іонів кальцію, - порушення регуляції за принципом негативного зворотного зв'язку.
Гіперпаратиреоз виявляється двома групами пов'язаних між собою змін.
Порушення кісткової тканини - генералізована фіброзна остеодистрофія. Обумовлена підвищенням активності остеокластів і пригніченням функції остеобластів. Виявляється болем у кістках і суглобах, розм'якшенням кісток, різкою деформацією скелета. Розвивається демінералізація кісткової тканини (остеомаляція), що обумовлює підвищення вмісту іонів кальцію в плазмі крові-гілер- кальціємію.
Гіперкальціємія. З нею пов'язані:
а) кальцнфікація м'яких тканин (нирок, судин, легень). У важких випадках розвивається ниркова недостатність;
б) утворення кальцієвих каменів у нирках;
в) порушення збудливості нервової системи і м'язів - м'язова слабкість, депресія, порушення нам'яті;
г) артеріальна гіпертензія;
ґ) посилення шлункової секреції.
Як здійснюється регуляція утворення і секреції чоловічих статевих гормонів? Назвіть їх основні біологічні ефекти.
Ендокринні клітини сім'яників (інтерстиціальні клітини, або клітини Лейдига) синтезують і секретують чоловічі статеві гормони - андрогени, серед яких основним є тестостерон,
Регуляція утворення андрогенів здійснюється за участю системи гіпоталамус- аденогіпофіз за схемою.' гіпоталамус —» гонадоліберии —» адеиогіпофіз —» лютеї- иізуючий гормон —» інтерстиціальні клітини сім'яників тестостерон —» клітини Серіалі сім'яників —» інгібін —» гальмування функціональної активності відповідних утворень гіпоталамуса і адеиогіпофіза —» зменшення утворення гоиадешіберину і лютеїнізуючого гормону —» зменшення синтезу і секреції андрогенів —» активація гіпоталамуса і т. д.
Основні біологічні ефйкти тестостерону: 1. Ембріональне диференціювання. Андрогени забезпечують диференціювання статевих залоз і статевих органів у період ембріонального розвитку. Утворюючись
від впливом хоріонічного гонадотропіну (у період між 6 і 1 б тижнями), тестостерон активує формування чоловічих статевих органів з вольфової протоки, урогеніталь- ного синуса і горбка, одночасно пригнічуючи розвиток жіночих статевих органів. Крім того, андрогени забезпечують диференціювання структур центральної нервової системи "за чоловічим типом", визначаючи надалі чоловічий тип статевої поведінки. т
Статеве дозрівання і розвиток вторинних статевих ознак в особин чоловічої статі. Оскільки андрогени стимулюють діяльність сальних залоз, то в пубертатному періоді шкіра стає жирною, часто відбувається інфікування сальних залоз - з'являються вугрі.
Регуляція сперматогенезу. Тестостерон активує діяльність міоепітеліальних клітин сім'яників (клітин Сертолі) та епітеліальних клітин проток, які у свою чергу здійснюють вплив на інтенсивність поділу статевих клітин та їхнє дозрівання. Така дія тестостерону не пов'язана з надходженням його в кров, а Є місцевою.
Регуляція статевої поведінки. Андрогени мають стосунок до формування статевого потягу (лібідо) і здатності до копуляції. Це пов'язано з тим, що тестостерон впливає на преоптичну зону гіпоталамуса (центр статевої поведінки) і полегшує спинномозкові рефлекси, важливі для копуляції. Тимчасова недостатність андрогенів у період статевого диференціювання і розвитку мозку призводить до формування в подальшому гомосексуальної орієнтації.
Анаболічна дія. Тестостерон активує процеси білкового синтезу. Саме з цим пов'язаний вплив андрогенів на ріст скелета і м'язів (посилення росту кісток у довжину, збільшення м'язової маси).
33.55. Які причини й основні прояви чоловічого гіпогонадизму?
Чоловічий гіпогонадизм - це гормональна недостатність чоловічих статевих залоз. Його причинами можуть бути:
І. Центральні (дисрегуляторні) порушення - зменшення утворення гонадолі- берину в гіпоталамусі, лкггеїнізуючого гормону в аденогіпофізі. Це може бути пов'язано з ураженням зазначені» структур, а також з гіперфункцією епіфіза, у разі якої збільшення утворення мелагоніну супроводжується пригніченням синтезу гонадотропних гормонів. Власне залозисті порушення:
а) кастрація - видалення сім'яників;
б) фіброз яєчок після деяких вірусних інфекційних захворювань, ускладнених орхітом (наприклад, після епідемічного паротиту);
в) порушення розвитку яєчок.
Після втрати яєчок розвивається комплекс порушень За назвою євнухізм. Гіпо» функцію яєчок при їх збереженні позначають терміном "євнухоїдизм". III. Периферичні порушення:
а) зменшення чутливості клітин-мішеней до дії андрогенів;
б) збільшене зв'язування тестостерону з білками плазми крові;
в) посилене руйнування андрогенів у печінці.
Прояви чоловічого гілогонадизму залежать від того, у який період онтогенезу вій розвивається.
Гіпогонадизм до періоду статевого дозрівання може виявлятися:
синдромам тестикулярної фемінізації (спадково обумовленим чоловічим пеевдо- гермафродитизмом). Цей синдром обумовлений порушеннями диференціювання статевої системи за чоловічим типом в період ембріогенезу;
слабко вираженими вторинними статевими ознаками;
пригніченням сперматогенезу;
відсутністю статевого потягу;
« порушенням окостеніння епіфізарних хрящів прн збереженому впливі СТГ—розвивається євнухоїдний, або гіпогонадний, гігантизм;
слабким розвитком скелетної мускулатури (відсутність аиаболічиих ефектів андрогенів).
Гіпогонадизм після завершення статевого дозрівання характерний, зокрема, для процесу старіння. Він виявляється: _
деяким зменшенням вираженості вторинних статевих ознак;
порушеннями сперматогенезу;
розвитком імпотенції;
анаболічними порушеннями - зменшенням маси скелетних м'язів і працездатності
Які причини і основні прояви чоловічого гіпергонадизму? Чоловічий гіпергонадизм може розвиватися в дитячому віці до періоду статевого дозрівання і у дорослих.
У дітей гіпергонадизм найчастіше пов'язаний з пухлинами і запальними процесами в гіпоталамусі, а також гіпофункцією епіфіза. Усі ці причини викликають збільшення продукції гонадотропних гормонів і, як наслідок, андрогенів. Клінічно такий гіпергонадизм виявляється передчасним статевим дозріванням.
Причиною гіперфункції статевих залоз у дорослих є добро- і злоякісні пухлини, що ростуть з інтерстиціальних клітин. При цьому виражених клінічних ознак, пов'язаних з гіперандрогенемією, немає. У випадку злоякісних новоутворень характерні відсутність кахексії, збереження м'язової маси і сили м'язів.
Які гормони відносять до жіночих статевих? Як здійснюється регуляція їх утворення і секреції?
Місцем синтезу зкіночи% статевих гормонів є яєчники. Тут утворюється три групи гормонів.
Естрогени: естрадіол, естрон, естріол. Продукуються епітеліальними клітинами фолікулів.
Прогестини, серед яких основним є прогестерон. Утворюються клітинами жовтого тіла.
Мінорні гормони: інгібін (пригнічує утворення ФСГ в аденогіпофізі) і релаксин (розм'якшує лобкове зрощення, тазові зв'язки, шийку маткн, розслаблює гладкі м'язи матки).
У )>егупяції утворення і секреції жіночих статевих гормонів вирішальне значення мають система гіпоталамус-аденогіпофіз-ясчники і механізми позитивного та негативного зворотного зв'язку.
У передовуляційний період під впливом ФСГ посилюється утворення і секреція естрогенів, які за принципом позитивного зворотного зв'язку стимулюють утворення гонадоліберину в гіпоталамусі і лютеїнізуючого гормону (ЛГ) в аденогіпофізі (забезпечують "пік ЛГ'). Останній викликає підвищення секреторної активності клітин, що продукують прогестинн.
У післяовуляційний період естрогени і прогестини за принципом негативного зворотного зв'язку пригнічують утворення гонадоліберину і гонадотропних гормонів аденогіпофіза, що веде в підсумку до зменшення секреції і самих жіночих статевих гормонів.
Назвіть основні біологічні ефекти жіночих статевих гормонів.
І. Статеве дозрівання і розвиток вторинних статевих ознак в особии жіночої статі. Ці ефекти обумовлені естрогенами, секреція яких починає зростати в період статевого дозрівання. П. Забезпечення циклічних змін в організмі жінки - підготовка статевих органів до запліднення та імплантації яйцеклітини. Це здійснюється завдяки участі жіночих статевих гормонів разом з ФСГ ї ЛГу гормональному контролі овуляції й менструального циклу.
Забезпечення вагітності, пологів і лактації Так, естрогени викликають швидкий ріст м'язів матки, стимулюють ріст системи проток молочних залоз. Прогестини блокують скорочувальну активність вагітної матки, стимулюють ріст залозистого епітелію молочних залоз. Зі зменшенням продукції прогестанів плацентою пов'язують настання пологів.
Екстрагенітальні ефекти. Естрогени впливають на:
а) кісткову тканину, забезпечуючи умови для своєчасного окостеніння епіфі- зарних хрящів;
б) печінку, активуючи синтез цілого ряду білків (транспортних білків, факторів зсідання, ангіотензиногену, ліпопротеїдів високої густини);
в) кровоносні судини, регулюючи процеси ангіогенезу, судинний тонус.
З дією прогестинів пов'язують збільшення базальної температури тіла в післяовуляційний період.
Які причини і основні прояви жіночого гіпогонадизму? Виділяють такі групи причин жіночого гіпогонадизму.
Центральні (диерегуляториі) порушення. Можуть бути обумовлені психогенними факторами, ураженнями гіпоталамуса (дефіцит гонадоліберину), гіпофункцією аденогіпофіза (дефіцит ФСГ і ЛГ), гіперфункцією епіфіза (зменшення утворення гонадотропних гормонів при збільшенні синтезу мелатоиіну).
Власне залозисті порушення:
а) спадково обумовлена аплазія яєчників;
б) дегенерація яєчників (запальна, кістозна);
в) аутоімунне ушкодження жіночих статевих залоз;
г) хірургічне видалення яєчників. III. Периферичні розлади:
а) зменшення чутливості клітин-мішеней до дії жіночих статевих гормонів;.
б) підвищене зв'язування їх білками плазми крові;
в) посилене руйнування жіночих статевих гормонів у печінці.
Клінічні прояви гіпофункції статевих залоз залежать від часу настання гіпо- гонадизму.
Якщо він розвивається до настання статевого дозрівання, то формується комплекс порушень під назвою "оваріальний євнухоїдизм": слабкий розвиток вторинних статевих ознак, первинна аменорея, високий зріст.
Розвиток гіпогонадизму в дітородному віці супроводжується порушеннями циклічних процесів в організмі жінки (розлади менструального никлу), безплідністю, передчасним клімаксом.
Після менопаузи розвиваються клімактеричні зміни - нестабільність судинного тонусу, остеопороз та ін.
Які причини і основні прояви жіночого гіпергонадизму?
В основі жіночого гіпергонадизму, при якому збільшується секреція жіночих статевих гормонів, можуть лежати центральні (дисрегуляторні) порушення і власне залозисті причини.
Центральні порушення, обумовлені збільшенням секреції гонадолібєрину і гонадотропних гормонів, можуть виявлятися розвитком синдрому передчасного ста- тевого дозрівання і синдрому уявної вагітності.
Для першого характерні рання поява вторинних статевих ознак, ранній початок менструацій і ймовірність завагітніти (у віці 7-8 років). Другий синдром виявляється аменореєю й усіма зовнішніми ознаками вагітності. При цьому має місце підвищена продукція пролакгину клітинами адеиогіпофіза.
До власне залозистих причин жіночого гіпергонадизму відносять кістозні процеси і пухлини яєчників, що продукують гормони. При цьому розвивається гіпертрофія ендометрію, порушується менструальний цикл, поновлюються маткові кровотечі в менопаузі.
У чому сутність ендокринної функції епіфіза? Чим можуть виявлятися її порушення?
Пінеалоцити (ендокринні клітини епіфіза) продукують гормон мелатонін - похідну сполуку амінокислоти триптофану. Рівень його секреції залежить від освітленості сітківки ока, інформація від якої через складні провідникові шляхи, у тому числі гіпоталамус і спинний мозок, надходить в епіфіз. У світлий час доби секреція мелатоніну гальмується, у темряві, навпаки, зростає. Так, у людини в нічний час (з 23 до 7 год.) вивільняється 70 % загальної добової кількості мелатоніну. З секрецією мелатоніну пов'язують функцію епіфіза, що її позначають як "біологічний годинник
Серед відомих нині біологічних ефектів мелатоніну - пригнічення утворення і секреції гонадотропних гормонів адеиогіпофіза, зменшення продукції ТТГ, АКГГ і СТГ.
Патологію епіфіза мало вивчено. Відомо, що при збільшенні продукції мелатоні- ну відбувається затримка статевого розвитку, а при зменшенні його секреції, навпаки - передчасне статеве дозрівання.
33.62. Якими змінами в організмі можуть виявлятися порушення ендокринної функції підшлункової залози ?
Ендокринну функцію виконують клітини острівців підшлункової залози, що продукують інсулін (бета-клітини) і глюкагон (альфа-клітини).
Зменшення синтезу й секреції інсуліну призводить до розвитку цукрового діабету (див. розд. 20).
Збільшення утворення інсуліну - гіперінсулінізм буває у разі виникнення пухлин, що розвиваються з р-клітин панкреатичних острівців і продукують інсулін; прн спонтанній ідіопатичній гіпоглікемії у дітей; на початкових стадіях цукрового діабету; прн ожирінні, демпінг-синдромі (стан після резекції шлунку), деяких ендокринних захворюваннях (акромегалія, тиреотоксикоз, хвороба Іценка-Кушинга).
Основні прояви гіперінсулінізму зумовлені гіпоглікемічною, анаболічною і міто- генною дією інсуліну (див. розд. 20). Під впливом надлишку інсуліну розвивається синдром гіпоглікемії (аж до гіпоглікемічної коми), ожиріння, склеротичні ураження кровоносних судин.
Другий гормон підшлункової залози—глюкагон має гіперптікемічну і ліполітич- ну дію, стимулює секрецію інсуліну.
Збільшення секреції глюкагону буває у разі розвитку пухлини з а-клітин острівців підшлункової залози (ппокашнома) і виявляє себе розвитком вторинного цукрового діабету (див. розд. 20).
Описано синдроми недостатності глюкагону. Для них характерна спонтанна гіпоглікемія, яку спостерігають у дітей.
