
- •Министерство образования и науки рф
- •Иркутский государственный технический университет
- •Издательство
- •Физические величины в химической кинетике
- •Математические методы обработки экспериментальных данных
- •Результаты опытов должны воспроизводиться Необходима объективная оценка результатов эксперимента Элементы теории вероятностей и математической статистики
- •Эмпирическое распределение случайной величины
- •Её определение
- •Формальная кинетика простых гомогенных реакций
- •Методы определения константы скорости и порядка реакии по экспериментальным данным
- •Общий вид зависимости концентраций реагента и продукта от времени
- •Реакции
- •Гомогенный катализ
- •АвтОкатализ
- •Гетерогенные реакции
- •Основные признаки протекания гетерогенного процесса
- •Лабораторные работы
- •Порядок выполнения работы
- •Необходимо быть внимательным и добавлять очередную порцию гипосульфита натрия сразу же после посинения раствора.
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Изменения относительного количества реагентов
- •Порядок выполнения работы
- •Соотношения объемов растворов в опытах и экспериментальные данные
- •Контрольные вопросы
- •От температуры
- •Порядок выполнения работы Температура опытов задается преподавателем
- •Экспериментальные и расчетные данные
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Пероксида водорода в присутствии катализатора
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •При кипячении реакционной смеси уравнительный сосуд поддерживать в наиболее высоком положении
- •Контрольные вопросы
- •Порядок выполнения работы
- •Не следует забывать, что делать это нужно перед каждым титрованием
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Гетерогенной реакции
- •Порядок выполнения работы
- •Экспериментальные и расчетные данные
- •Не забывать после каждого отбора пробы опускать брусок мрамора в раствор так, чтобы площадь контакта его с раствором оставалась постоянной
- •Контрольные вопросы
- •На скорость гетерогенной реакции
- •Порядок выполнения работы Температура опытов задается преподавателем
- •Экспериментальные и расчетные данные
- •Экспериментальные и расчетные данные
- •Контрольные вопросы
- •Библиографический список
- •Основные единицы измерения физических величин
- •Множители и приставки для образования десятичных кратных и дольных единиц и их наименования
- •Буквы греческого алфавита
- •Значения критерия Стьюдента при различных уровнях значимости
- •Значения критерия Кохрена при различных уровнях значимости
- •Значения критерия Фишера при различных уровнях значимости
- •664074. Иркутск, ул. Лермонтова, 83
От температуры
Цель работы: изучение влияния температуры на скорость химической реакции и ознакомление с методикой определения кинетических констант уравнения Аррениуса.
Исследуемая реакция протекает по уравнению
![]() .
.
За скоростью протекания процесса удобно следить по изменению концентрации йода, оттитровывая его раствором гипосульфита натрия с использованием крахмала в качестве индикатора.
Приборы
и материалы:
термостат, термометр, часы, реакционная
колба, бюретка на штативе с колбой для
титрования, пипетки на 10 см3
- 3 шт., на 5 см3
– 1 шт. Растворы: 0,02 М
;
0,0005М
![]() ;
0,25М
;
0,25М
![]() ;
0,05 М
;
0,05 М
![]() ;
крахмал.
;
крахмал.
Порядок выполнения работы Температура опытов задается преподавателем
Отмерить пипетками по 10 см3 растворов персульфата аммония и серной кислоты в реакционную колбу и поместить её в термостат.
Когда раствор примет температуру термостата, влить в него 5 см3 раствора йодида калия, и вернуть колбу в термостат. Заметить по часам время вливания и считать его за начало опыта.
Через 5 мин. от начала опыта отобрать из реакционной смеси пробу в 10 см3 и оттитровать её раствором гипосульфита натрия до полного обесцвечивания (индикатор – крахмал). Для замедления реакции во время определения концентрации йода в колбу для титрования следует налить холодной воды. Результаты титрования (объем гипосульфита натрия) записать в табл. 8.
Через 10 мин. от начала опыта ещё раз отобрать пробу в 10 см3 и также оттитровать её.
То же самое проделать, повышая температуру в соответствии с заданием преподавателя. Все результаты записывать в табл. 8.
Таблица 8
Экспериментальные и расчетные данные
-
Температура опыта,
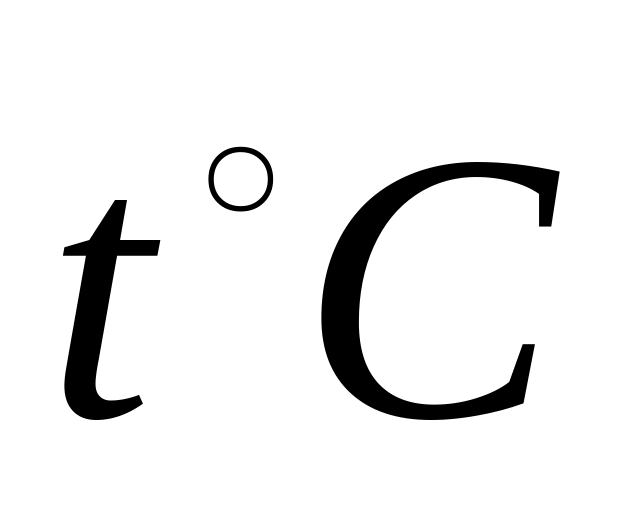
, мин.
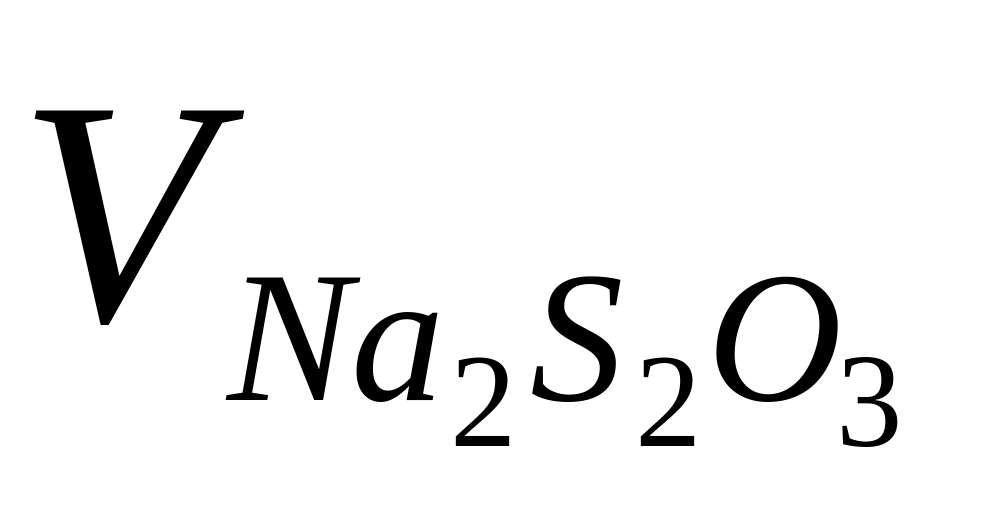 ,
см3
,
см3 ,
М
,
М
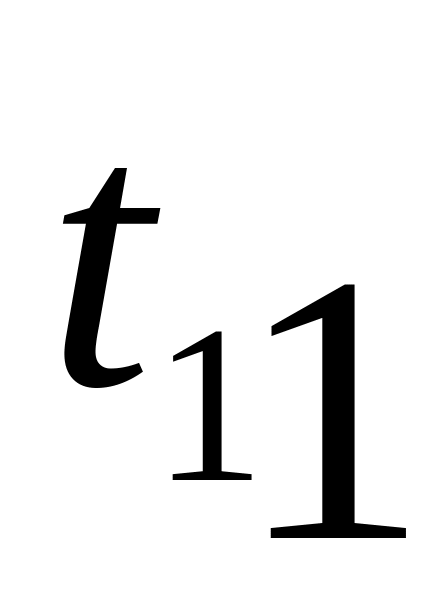
5
10
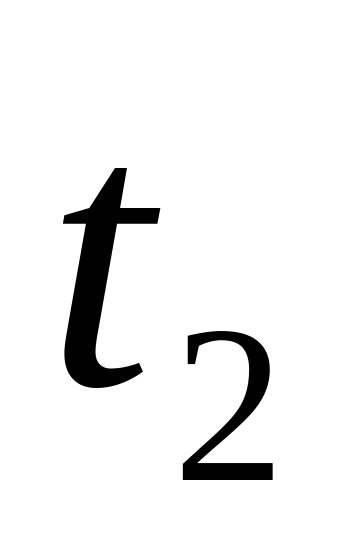
5
10
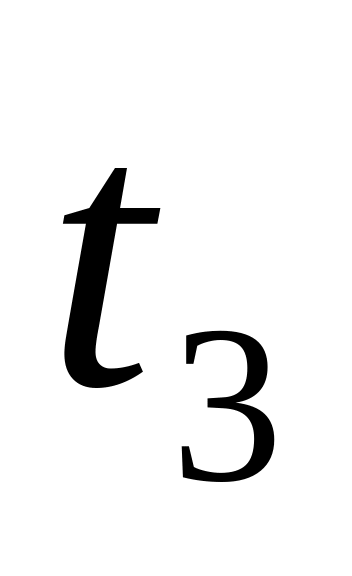
5
10
Рассчитать концентрацию йода по формуле (8).
Константу скорости реакции для всех шести случаев вычислить по формуле (21). При расчете учесть, что убыль концентрации равна концентрации йода, рассчитанной по данным титрования (табличные значения). Начальные концентрации персульфата аммония и йодида калия определить с учетом разведения:
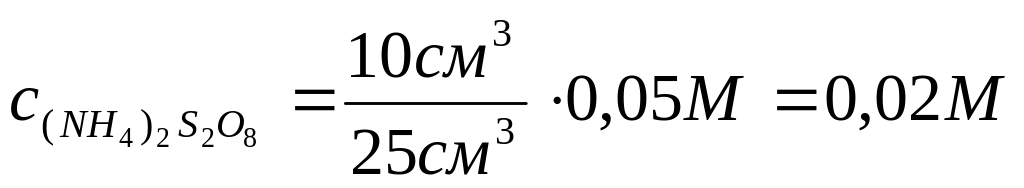 и
и
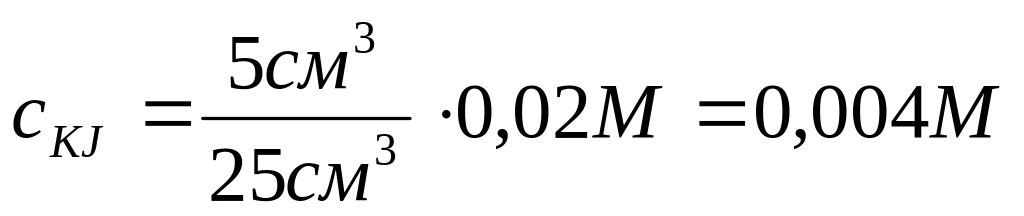 .
.Найти среднее из двух значений константы скорости реакции при каждой температуре и записать результаты в табл. 9.
Таблица 9
Экспериментальные и расчетные данные
-
Опыт
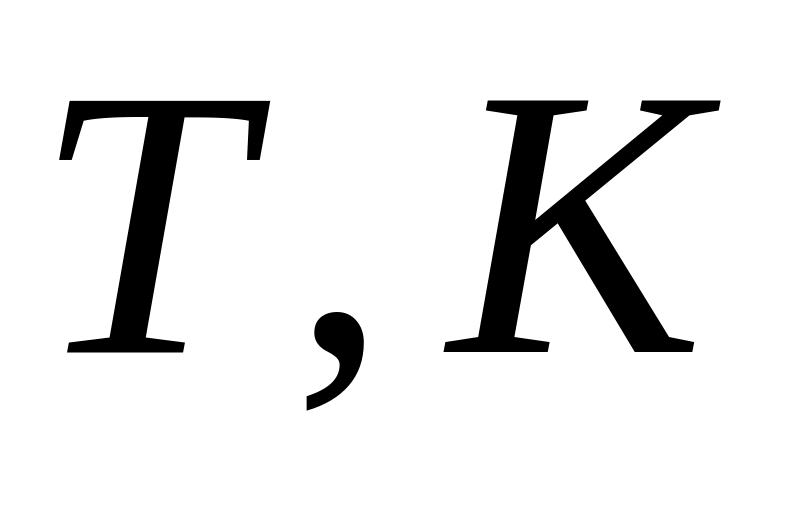
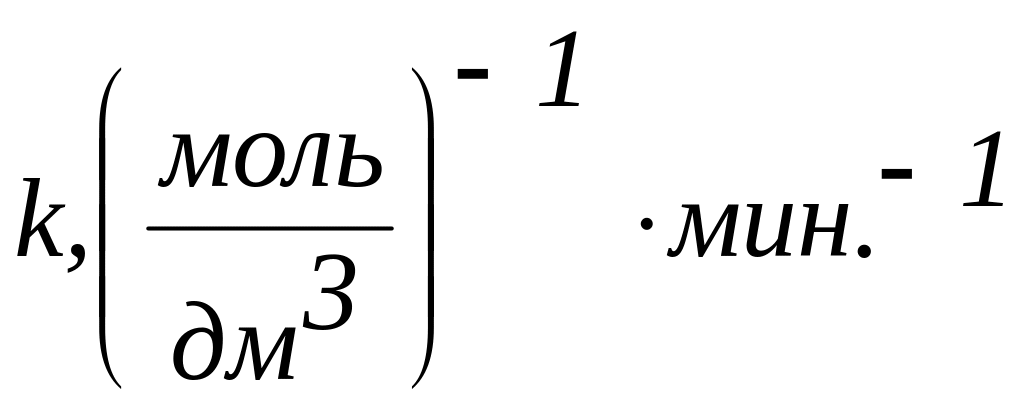
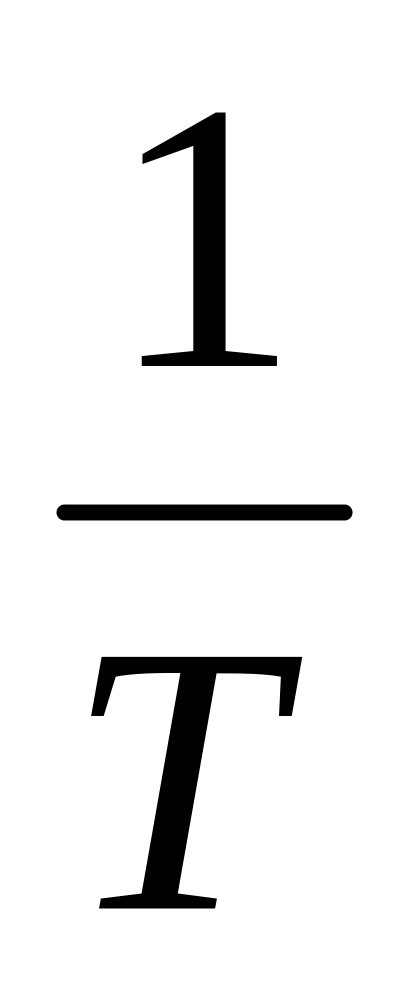
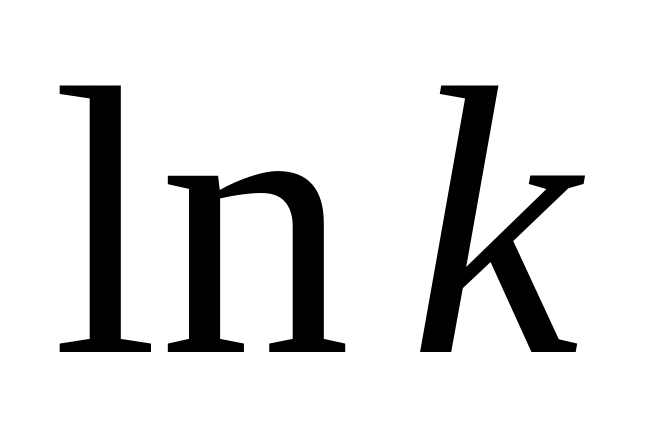
1
2
3
.
.
.
и т.д.
Построить график зависимости
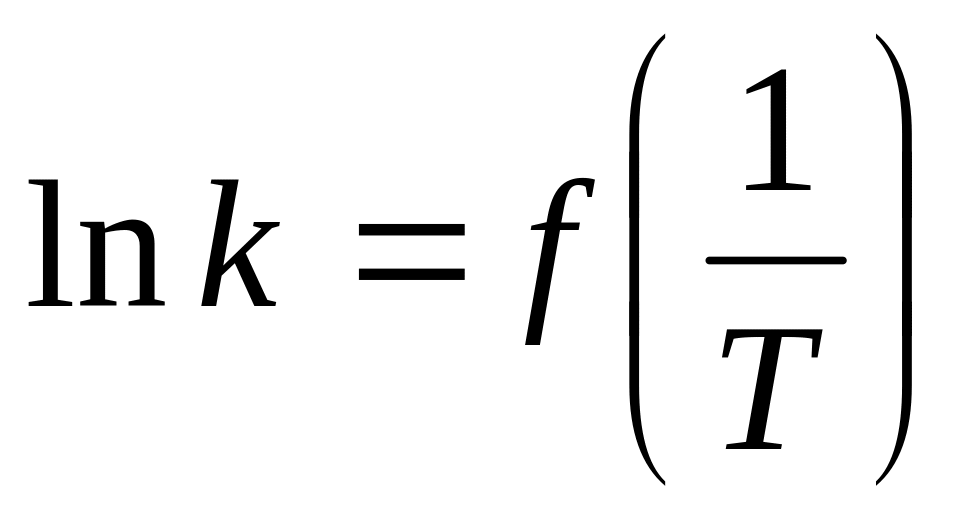 и графически определить энергию
активации и предэкспоненциальный
множитель.
и графически определить энергию
активации и предэкспоненциальный
множитель.Определить энергию активации и предэкспоненциальный множитель расчетным путем и сравнить полученные результаты с найденными графически.
Определить относительную ошибку в определении энергии активации по формуле
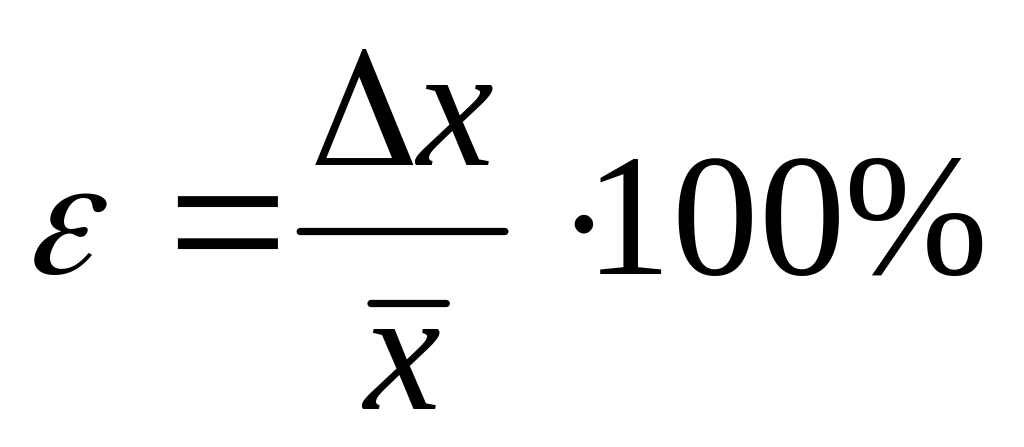 ,
считая за среднеарифметическое
значение, полученное графически.
,
считая за среднеарифметическое
значение, полученное графически.Вычислить энтропию активации изучаемой реакции и температурный коэффициент реакции
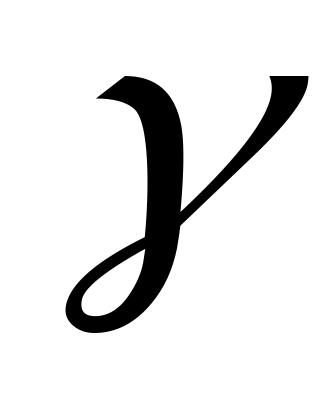 .
.
