- •Мета: Формування знання хімічних властивостей органічних сполук різних типів для розуміння їх реакційної здатності.
- •Дослід 2. Омилення жирів
- •Лабораторна робота №3
- •Тема: Реакційна здатність та хімічні властивості гетерофункціональних сполук
- •Дослід 1.
- •Якісні реакції на кетонові тіла
- •Лабораторна робота № 4 Тема: Гетероциклічні і ароматичні сполуки мета: Вивчити основні хімічні властивості гетероциклічних сполук, які приймають участь у метаболізмі людини.
- •Лабораторна робота № 5 Тема: Вуглеводи.
- •Реакція Тромера
- •1.2 Реакция Фелінга
- •Висновки
- •Дослід 5. Кислотний гідроліз крохмалю
- •Лабораторна робота № 6 Тема: -Амінокислоти, пептиди, білки.
- •Зразок завдань підсумкового контролю знань по биоорганической химии
- •План проведення лабораторно - практичних занять з курсу «Біоорганічна хімія» для студентів 1 курсу медичного факультету
- •Список літератури
- •Критерії оцінювання знань студентів
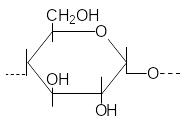
Дослід 5. Кислотний гідроліз крохмалю
В пробірку поміщують 2 мл 0,1 % розчину крохмалю і 15 крапель 2 н розчину сірчаної кислоти. Нагрівають на водяній бані протягом 10 хвилин. Відбирають піпеткою 3-4 краплі гідролізату і додають 1 краплю йоду. Відсутність забарвлення показує проходження гідролізу. У випадку забарвлення продовжують нагрівання ще 5 хвилин. Потім відбирають пробу на наявність крохмалю. При відсутності забарвлення пробірку охолоджують і відбирають 4-5 крапель гідролізату в іншу пробірку. Потім додають реактив Фелінга чи Тромера і спостерігають змінення забарвлення.
|
|
|
|
|
|
|
Крохмаль |
|
|
Декстрини |
|
|
|
|
|
|
|
|
Мальтоза |
|
|
-Д-глюкопираноза |
|
Висновок:
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Лабораторна робота № 6 Тема: -Амінокислоти, пептиди, білки.
Мета: Сформувати знання хімічних властивостей найважливіших амінокислот і хімічної основи структурної організації білкових молекул.
Дослід 1.
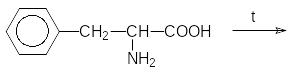
Декарбокилювання -амінокислот. Декарбокислювання тирозину.
В пробірку поміщають 3-4 краплі 0,03 % розчину тирозину, 1 мл насиченого розчину Са(ОН)2, перемішують і кипятять протягом декількох хвилин до появи каламуті.
![]()
ВИСНОВОК:
_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Дослід 2.
Хімічні властивості -амінокислот, пептидів, білків. Якісна реакція на окситоцин.
В пробірку поміщають 1-2 мл лікарського препарату окситоцину, 2-3 краплі 5 % ацетату свинцю, 5-7 крапель 30% їдкого натру. Перемішують, кипятять протягом 5 хвилин, спостерігають появу забарвленого осаду.
![]()
Н апішить
схематично реакцію, внаслідок якої
дисульфідний тип звязку
перейде в сульфгідрильний звязок,
на прикладі окситоцину.
апішить
схематично реакцію, внаслідок якої
дисульфідний тип звязку
перейде в сульфгідрильний звязок,
на прикладі окситоцину.
ВИСНОВОК:
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Дослід 3.
Виявлення білків в біологічному матеріалі. Нінгідринова реакція.
В пробірку поміщають 5-7 крапель лікарського препарату інсуліну, 4-5 крапель розчину нінгідрину, перемішують, нагрівають до появи забарвлення.
ВИСНОВОК:
___________________________________________________________________________________________________________________________________________________________________________________________________________________________________________
Дослід 4.
Виявлення -амінокислот, пептидів, білків в біологічному матеріалі. Біуретова реакція.
В пробірку помішують 1 мл лікарського препарату інсуліну, 1 мл 10% розчину їдкого натру, 2-3 краплі розчину сульфату міді (ІІ) до появи забарвлення.
ВИСНОВОК:
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________