
- •1. Понятие «биомембрана»
- •2. Эволюция представлений о биомембране
- •3. Жидкостно-мозаичная концептуальная модель биомембраны Сингера-Николсона (1972 г.)
- •Изображение элементов биомембраны
- •4. Предметные модели биомембраны
- •5. Современные подходы к исследованию биомембран
- •Выделение и характеристика мембранных фракций
- •Методы исследования мембранных структур
- •Электронная микроскопия
- •Методы замораживания-скалывания, замораживания-травления
- •Методы изучения динамического поведения мембранных систем и липид-белковых взаимодействий
- •Микровязкость мембран и применимость мембранных зондов
- •6. Мембранные липиды
- •Фосфолипиды
- •Глицерофосфолипиды
- •Сфингофосфолипиды
- •Гликолипиды
- •Стероиды. Холестерин.
- •Роль холестерина в биомембранах
- •Жирные кислоты и их пространственная конфигурация
- •Фосфолипиды как структурная основа бислоя
- •Трансмембранная асимметрия липидов
- •Подвижность компонентов липидного бислоя
- •Минорные липиды
- •7. Мембранные белки
- •Классификация мембранных белков
- •Топологическая классификация
- •Биохимическая классификация
- •Подвижность мембранных белков
- •Белок-липидные взаимодействия
- •Свойства мембранных белков
- •Основные функции мембранных белков
- •Белки-ферменты
- •Рецепторные белки
- •Структурные мембранные белки
- •8. Углеводы мембран
- •Рецепторная функция
- •Пресинаптическая мембрана
- •11. Типы биомембран
- •12. Подмембранные структуры
- •13. Надмембранные структуры
- •Гликокаликс
Стероиды. Холестерин.
Стероиды – спирты со стерановым скелетом, к которым относятся как немембранные липиды (из них наиболее важны гормоны), так и компоненты мембран. В перечень мембранных компонентов стероидного ряда входят холестерин, ситостерин, тетрахименин. В тканях животных распространен холестерин.
В растительных клетках холестерин не обнаружен, его заменяют фитостерины. У бактерий стероиды отсутствуют.
Холестерин и его эфиры – непременные составляющие плазматических мембран клеток животных.
При этом холестерин легче встраивается в мембрану, чем его эфиры (рис. 807231651).
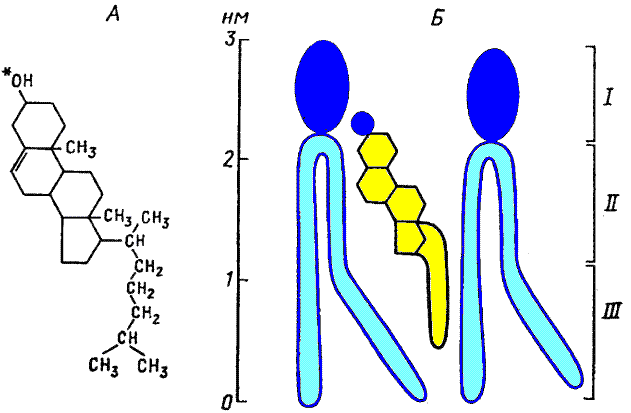

Рис. 807231651. Структурная формула холестерина (А), и его упаковка в бислое (Б). Звездочкой отмечен гидроксил, используемый для образования эфиров холестерина. I – область полярных голов; II – область, упорядочиваемая холестерином; III – область более подвижных цепей.
Молекула холестерина не содержит длинных прямых цепочек, а состоит из четырех колец (рис. 807231651).
Холестерин, как и другие липидные молекулы, имеют полярную голову и вытянутую в длину неполярную часть. Поэтому они хорошо встраиваются в бислойные липидные структуры, образующие клеточные мембраны (рис. 807231651).
Особенно много холестерина содержится в наружных мембранах. Например, в плазматической мембране клеток печени холестерин составляет около 30% всех мембранных липидов.
Роль холестерина в биомембранах
Было показано, что холестерин влияет на подвижность жирнокислотных хвостов мембранных липидов. Если мембрана слишком ригидна и существует опасность «застывания» жирнокислотных цепей, холестерин вызывает ее разжижение, поскольку цепи в его присутствии становятся более подвижными. Если же мембрана слишком «жидкая», то холестерин ее уплотняет.
Для мутантных клеток, которые не могут синтезировать холестерин, необходимо его присутствие в культуральной среде. В его отсутствии мембраны быстро разрушаются.
Таким образом, холестерол играет роль регулятора, обеспечивающего правильную упаковку липидной части мембраны, необходимую для ее нормальной работы.
Жирные кислоты и их пространственная конфигурация
|
9 |
И фосфо-, и гликолипиды включают в состав молекул различные жирнокислотные радикалы. Холестерин и его аналоги также способны образовывать эфиры с разнообразными жирными кислотами. Вследствие этого свойства образующихся при этом липидов сильно варьируют.
При всем разнообразии жирных кислот преобладающими для данной ткани являются обычно две или три из них. В организме животных кроме пальмитиновой и олеиновой кислот содержатся большие количества стеариновой кислоты, а также и более высокомолекулярные кислоты с числом атомов углерода 20 и более. Как правило, они имеют четное количество атомов углерода; жирные кислоты с нечетным числом атомов встречаются только в составе цереброзидов и ганглиозидов.
Число двойных связей в молекулах жирных кислот колеблется от 1 до 6 и зависит от среды обитания, состава пищи, сезона и т.д. Двойные связи в жирных кислотах животного происхождения разделены метиленовой группировкой –СН=СН-СН2-СН=СН-.
Углеродные связи в молекулах жирных кислот имеют различную конформацию (рис. 807231854).

Рис. 807231854. Пространственная конфигурация жирных кислот
1 – насыщенная углеводородная цепь в транс‑конформация, 2 – ненасыщенная цепь в цис‑конформации, 3 – насыщенная цепь в гош‑конформации.
По своей структурной конфигурации насыщенные жирные кислоты сильно отличаются от ненасыщенных.
Насыщенные жирные кислоты могут принимать множество конфигураций вследствие высокой свободы вращения вокруг одиночных С-С связей. Энергетически наиболее выгодной является транс-конфигурация.
Ненасыщенные жирные кислоты имеют жесткую структуру, поскольку вращение вокруг двойных связей невозможно. Ненасыщенные жирные кислоты содержат двойные связи почти всегда в цис-конформации (рис. 807231854), транс‑ненасыщенные жирные кислоты в природе почти не встречаются.
Цис-конфигурация двойной связи обусловливает изгиб цепи под углом приблизительно 30º. По этой причине цис-ненасыщенные жирные кислоты с одной двойной связью вызывают локальные возмущения бислоя.
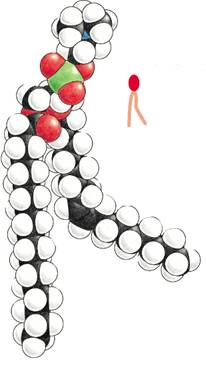
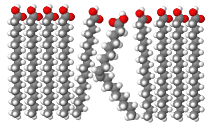
При этом длина такой цепи уменьшается, а занимаемый ею объем возрастает. В области локализации двойных цис-связей образуются изгибы (так называемая гош‑форма).
При повышении температуры тепловая подвижность жирнокислотных цепей приводит к спонтанному возникновению изгибов.
Если изгибы, соответствующие гош-конформации, появляются на близлежащих участках жирнокислотной цепи, эта область может принимать вид петли или полости (кинк). В результате взаимопревращения транс- и гош-конформаций (так называемого транс‑гош-перехода) кинки могут «скользить» вдоль цепи, обеспечивая перемещение их содержимого поперек мембраны.
Таким образом может осуществляться диффузия захваченной воды через гидрофобный бислой.
При повышении плотности упаковки бислоя конфигурационная подвижность С-С-связей ограничивается. В таком бислое подвижность цепей ограничена согласованными колебаниями или вращательной подвижностью около точки прикрепления жирнокислотных радикалов к полярной «головке» фосфолипида. В этой ситуации в бислое наиболее предпочтительны две конформации цепи: когда вся цепь находится в транс-конфигурации или когда имеется «двойной гош», то есть изгибы, возникающие на двух соседних участках цепи вследствие образования гош-конформации, компенсируют друг друга, и вся цепь в целом не имеет изгибов.
