
- •Итоговый тест по курсу «Химия» .
- •Итоговый тест по курсу «Химия»
- •2. Среди перечисленных веществ выбрать основную соль:
- •11. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •2. Среди перечисленных веществ выбрать основную соль:
- •12. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •IV вариант
- •12. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •V вариант
- •12. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •VI вариант
- •8. В гальваническом элементе самопроизвольно протекает реакция
- •13. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •VII вариант
- •13. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •VIII вариант
- •5. Химическая связь, образующаяся межу атомами элементов с порядковыми
- •13. Выберите кинетическое уравнение прямой реакции для данной химической реакции:
- •Итоговый тест по курсу «Химия»
- •IX вариант
- •Итоговый тест по курсу «Химия» х вариант
- •5. Химическая связь, образующаяся межу атомами элементов с порядковыми
- •Итоговый тест по курсу «Химия» Вариант XI
- •Не изменяется; б) уменьшается; в) увеличивается;
- •Итоговый тест по курсу «Химия»
- •XII вариант
- •Итоговый тест по курсу «Химия»
- •XIII вариант
- •Итоговый тест по курсу «Химия»
- •XIV вариант
- •2. Среди перечисленных веществ выбрать основную соль:
- •Итоговый тест по курсу «Химия»
- •XV вариант
- •4. Атом какого элемента проявляет наибольшую склонность к образованию ионной связи: а)h; б)с; в)Cl; г)р?
- •Итоговый тест по курсу «Химия»
- •XVI вариант
- •Итоговый тест по курсу «Химия»
- •XVII вариант
- •Итоговый тест по курсу «Химия»
- •XVIII вариант
- •11. Какой из факторов не оказывает влияния на скорость химической реакции в растворах: а) концентрация вещества; б) использование катализатора
- •Итоговый тест по курсу «Химия»
- •XIX вариант
- •Итоговый тест по курсу «Химия»
- •XX вариант
Итоговый тест по курсу «Химия»
XVII вариант
1. Укажите группу кислотных оксидов:
а) CO2 , CaO , N2O5; в) Al2O3 , CuO , Mn2O7;
б) Cl2O7 , SO2 , MgO; г) CO2 , SO3 , P2O5.
2. Укажите группу основных солей:
а) NaHSO4 , HOH; в) FeOHCl , NaOH;
б) Na2CO3 , ZnOHNO3; г) AlOHCl2 , MgOHBr
3. Какая кислота соответствует оксиду серы (VI): а) H2SO4 ; б) H2SO3 в) H2S; г) H2CO3.
4. Какая химическая связь наименее прочная:
а)металлическая; б)ионная;
в) ковалентная полярная; г)ковалентная неполярная?
5. Атом какого элемента проявляет наибольшую склонность к образованию ионных связей: а)С; б)Si; в)F; г)Р?
6. Используя значения относительной электроотрицательности элементов, определите тип химической связи в молекуле AlCl3. (электроотрицательность Al – 1,5; Cl – 3,0).
7. Металлы алюминий, магний, хром, плутоний – это соответственно:
а) s-, p-, d-, f- элемент; б) p-, d-, s-, f- элемент;
в) s-, d-, f-, p- элемент; г) p-, s-, d-, f- элемент.
8. Реакция Ме0 + 2Н+ = Меn+ + H2 возможна, если:
а) e0Men+/ Me > e02H+/ H2; б) e0Men+/ Me = e02H+/ H2; в) e0Men+/ Me < e02H+/ H2.
9. Электрод, на котором протекает процесс окисления, называется:
а) катодом; б) анодом.
10. К способам защиты металлов от коррозии не относится:
а) покраска изделий; б) покрытие полимерными пленками;
в) сварка изделий; г) присоединение более активного металла
11. Взаимодействие какой пары веществ будет протекать с большей скоростью, если известно, что концентрация растворов кислот во всех случаях одинакова:
а) Ni u HCl; б) Zn u HCl; в) Fe u HCl; г) Al u HCl.
12. В каком направлении сместится равновесие реакции при уменьшении концентрации первого из исходных веществ: Н2(г) +S(тв) ↔ Н2S(г) а) вправо (→); б) влево (←) ?
13. Выберите уравнение зависимости константы равновесия от концентрации исходных веществ и продуктов реакции для данного химического уравнения:
2NO(г) + Cl2(г) ↔ 2NОCl(г)
а)
 ;
б)
;
б)
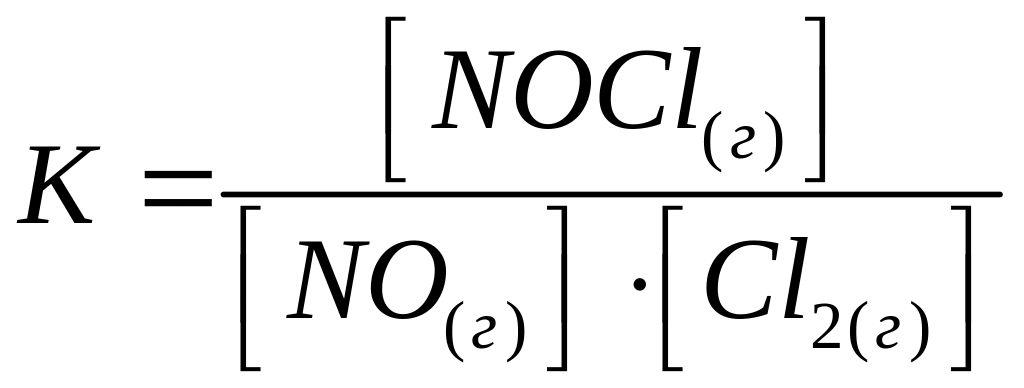 ;
;
в)
 ;
г)
;
г)
 .
.
14. Во сколько раз увеличится скорость обратной реакции: 2NO(г) + О2(г) ↔ 2NO2(г)
при увеличении концентрации оксида азота (IV) в 3 раза: а) 81; б) 27; в) 9; г) 3?
15. Во сколько раз увеличится скорость прямой реакции:
4HCl(г) + О2(г) ↔ 2Н2O(г) + 2Cl2(г)
при увеличении давления в 2 раза: а) 64;б) 32; в) 16; г) 4 ?
Составил Латышева Т.И.
Итоговый тест по курсу «Химия»
XVIII вариант
1. Укажите группу кислотных оксидов:
а) CO, ZnO, CO2; в) CO2, N2O5, MgO;
б) CO2, P2O5, Li2O; г) SO2, SO3, Mn2O7.
2 . Укажите группу основных солей:
а) MgOHCl и AlOHCl2; в) ZnOHCl и ZnCl2;
б) NH4Cl и CH3COONa; г) NaOH и Na2CO3.
3. Какая кислота соответствует оксиду азота (V):
а) HNO2; б) HNO3; в) NO2; г) N2O3.
4.В каком из указанных соединений сера проявляет степень окисления «6+»: а) Al2(SO4 )3; б) ZnS; в) CuSO3; г) SO2
5. Какая химическая связь наименее прочная:
а)металлическая; б)ионная;
в) ковалентная; г)водородная?
6. Атом какого элемента проявляет наибольшую склонность к образованию ионных связей: а)С; б)Si; в)F; г)Р?
7. Используя значения относительной электроотрицательности элементов, определите тип химической связи в молекуле AlCl3 (электроотрицательность Al – 1.5, Cl – 3,0).
8. В ряду Na – Mg – Al металлические свойства:
а) увеличиваются; б) ослабевают; в) остаются без изменений.
9. Реакция BiSO4 + Me0 = MeSO4 + Bi возможна, если:
а) e0Bi2+/ Bi > e0Men+/ Me; б) e0Bi2+/ Bi = e0Men+/ Me; в) e0Bi2+/ Bi < e0Men+/ Me.
10. Устройства, преобразующие энергию химической реакции в электрическую энергию, в которых протекают обратимые окислительно – восстановительные реакции, называются:
а) аккумуляторами; б) гальваническими элементами.
