
- •1Вопрос Основные положения теории химического строения а.М. Бутлерова
- •2 Вопрос. Предельные углеводороды
- •Химические свойства
- •Способы получения циклоалканов
- •Алгоритм составления названий предельных углеводородов
- •2.3.1.Прямое галогенирование углеводородов.
- •13 Аминокислоты: классификация, номенклатура, физические и химические св-ва,практическое применение.
- •Некоторые важнейшие a-аминокислоты общей формулы
- •Применение
- •Химические свойства
- •Применение
- •33. Органические соединения, содержащие серу: классификация, получение, свойства, применение
- •15 ВопросХимические свойства белков
- •21 Вопрос. Жиры и масла. Получение ,гидролиз и гидрогенизация жиров.
- •Вопрос 22.Карбоновые кислоты ароматического ряда: получение ,свойство ,применение.
- •25.Нитросоединения
- •20 Вопрос.Высокомолекулярные соединения.
- •27 Вопрос
- •Физические свойства спиртов.
- •30 Вопрос.Ароматические альдегиды и кетоны
- •3.Амины.
- •4.Арены
- •28. Органические соединения содержащие кремний.
13 Аминокислоты: классификация, номенклатура, физические и химические св-ва,практическое применение.
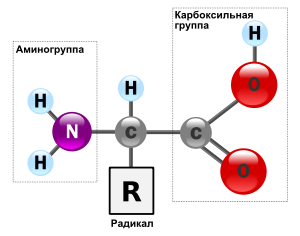
Аминокисло́ты (аминокарбо́новые кисло́ты) — органические соединения, в молекуле которых одновременно содержатсякарбоксильные и аминные группы.
Аминокислоты могут рассматриваться как производные карбоновых кислот, в которых один или несколько атомов водородазаменены на аминные группы.
Номенклатура
По систематической номенклатуре названия аминокислот образуются из названий соответствующих кислот прибавлением приставки амино и указанием места расположения аминогруппы по отношению к карбоксильной группе.
Часто используется также другой способ построения названий аминокислот, согласно которому к тривиальному названию карбоновой кислоты добавляется приставкаамино с указанием положения аминогруппы буквой греческого алфавита. Пример:
![]()
![]() Для a-аминокислот,
которые играют исключительно важную
роль в процессах жизнедеятельности
животных и растений, применяются
тривиальные названия.
Для a-аминокислот,
которые играют исключительно важную
роль в процессах жизнедеятельности
животных и растений, применяются
тривиальные названия.
Некоторые важнейшие a-аминокислоты общей формулы
Аминокислота |
-R |
Глицин |
-Н |
Аланин |
-CH3 |
Фенилаланин |
-CH2-C6H5 |
Валин |
-СH(CH3)2 |
Лейцин |
-CH2-CH(CH3)2 |
Серин |
-CH2OH |
Если в молекуле аминокислоты содержится две аминогруппы, то в ее названии используется приставка диамино, три группы NH2 – триамино и т.д.
Пример:
![]()
Наличие двух или трех карбоксильных групп отражается в названии суффиксом –диовая или -триовая кислота:
![]()
Физические свойства
Аминокислоты — бесцветные кристаллические вещества, хорошо растворимые в воде. Многие из них обладают сладким вкусом.
[править]Общие химические свойства
Все аминокислоты амфотерные соединения, они могут проявлять как кислотные свойства, обусловленные наличием в их молекулах карбоксильной группы —COOH, так и основныесвойства, обусловленные аминогруппой —NH2. Аминокислоты взаимодействуют с кислотами и щелочами:
NH2 —CH2 —COOH + HCl → HCl • NH2 —CH2 —COOH (хлороводородная соль глицина)
NH2 —CH2 —COOH + NaOH → H2O + NH2 —CH2 —COONa (натриевая соль глицина)
Растворы аминокислот в воде благодаря этому обладают свойствами буферных растворов, т.е. находятся в состоянии внутренних солей.
NH2 —CH2COOH
![]() N+H3 —CH2COO-
N+H3 —CH2COO-
Аминокислоты обычно могут вступать во все реакции, характерные для карбоновых кислот и аминов.
Этерификация:
NH2 —CH2 —COOH + CH3OH → H2O + NH2 —CH2 —COOCH3 (метиловый эфир глицина)
Важной особенностью аминокислот является их способность к поликонденсации, приводящей к образованию полиамидов, в том числе пептидов, белков, нейлона, капрона.
Реакция образования пептидов:
HOOC —CH2 —NH —H + HOOC —CH2 —NH2 → HOOC —CH2 —NH —CO —CH2 —NH2 + H2O
Изоэлектрической точкой аминокислоты называют значение pH, при котором максимальная доля молекул аминокислоты обладает нулевым зарядом. При таком pH аминокислота наименее подвижна в электрическом поле, и данное свойство можно использовать для разделения аминокислот, а также белков и пептидов.
Цвиттер-ионом называют молекулу аминокислоты, в которой аминогруппа представлена в виде -NH3+, а карбоксигруппа — в виде -COO−. Такая молекула обладает значительным дипольным моментом при нулевом суммарном заряде. Именно из таких молекул построены кристаллы большинства аминокислот.
Некоторые аминокислоты имеют несколько аминогрупп и карбоксильных групп. Для этих аминокислот трудно говорить о каком-то конкретном цвиттер-ионе.
