
2. Аппаратурное оформление очистки
Принципиальная схема каталитической очистки включает в себя камеру подготовки газа (камера сгорания), камеру смешения и реактор.
Конструктивно аппараты на установках каталитической очистки отходящих газов могут использоваться в вертикальном или горизонтальном исполнении.
Для примера рассмотрим реактор каталитической очистки (полочного типа).
Хвостовые нитрозные газы (рис. 4.1) входят сверху при температуре 400 – 520 °С. Чтобы исключить локальный прогрев корпуса, внутреннюю корзину футеруют слоем каолиновой ваты толщиной 70 – 100 мм.
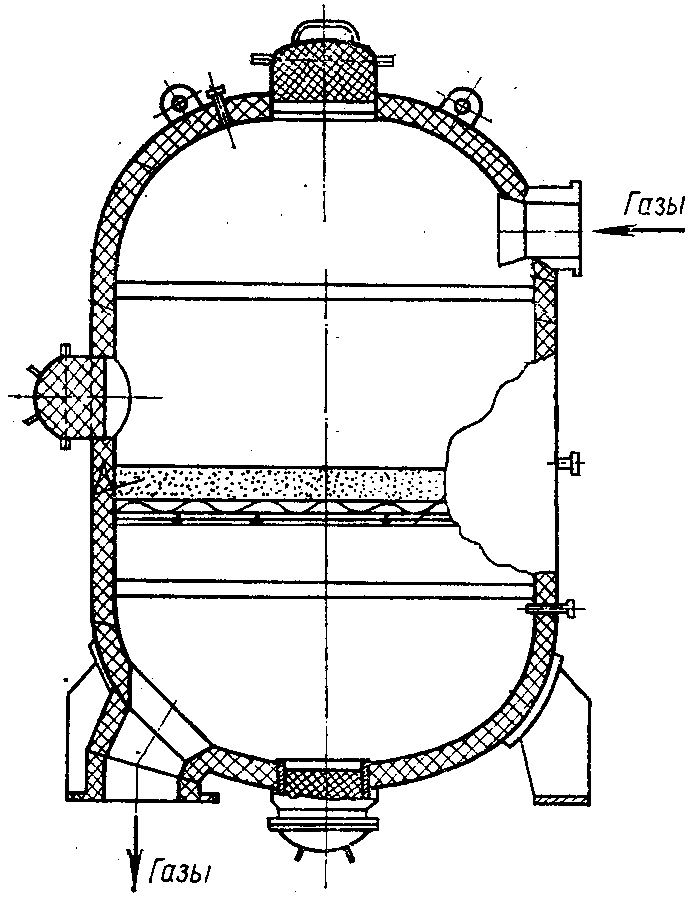
Рис. 4.1. Схема реактора каталитической очистки
3. Расчет реактора
3.1. Физико-химические основы процесса очистки.
Процесс каталитической очистки хвостовых нитрозных газов можно описать двумя основными суммарными реакциями:
СН4 + 2О2 CO2 + 2H2O + Q (1)
СН4 + 4NO СО2 + 2H2O + 2N2+ Q (2)
В адиабатических условиях в реакторе с неподвижным слоем катализатора процесс может быть описан системой уравнений [3]:
![]() (3)
(3)
![]() (4)
(4)
![]() (5)
(5)
![]() , (6)
, (6)
где V - объемный расход газа;С- концентрация соответствующего компонента;F- площадь проходного сечения реактора;W- скорость соответствующей химической реакции;Ср- теплоемкость газовой смеси;H- тепловой эффект химической реакции;l- высота слоя контактной массы.
Скорости реакций (1) и (2) выражают в виде зависимостей [3]:
![]() (7)
(7)
![]() (8)
(8)
Результаты исследований показали, что:
k01= 2,47105;k02= 1,63109;E1= 11,8 кДж/моль;E2= = 78,88 кДж/моль;H1= 800 кДж;H2= 956 кДж;Ср= 31,2 кДж/(мольК);i = 1,3;m= n=j= 1,0 [5].
Тогда уравнения математической модели процесса можно записать следующим образом:
![]() (9)
(9)
![]() (10)
(10)
![]()
![]() (11)
(11)
![]()
![]() (12)
(12)
3.2 Метод решения.
Для решения системы дифференциальных уравнений используем метод Рунге-Кутта 4-го порядка. Метод эффективен и реализуется программными средствами.
![]() (13)
(13)
i= 1, 2, 3,…,n
3.3. Исходные данные.
ЗАДАНИЕ:
- определить высоту слоя контактной массы в каталитическом реакторе для обеспечения концентрации оксида азота в отходящих из аппарата очищенных газах не болев ПДК;
- составить материальный баланс для каталитического реактора.
В соответствии со списком № 3086-84 [1] максимально разовая ПДК окислов азота в атмосферном воздухе населенных мест;
ПДКNO = 0,6 мг/м3= 0,44810-6м3/м3= 0,44810-4% об.
(ПДКNO2 = 0,085 мг/м3= 0,63410-7м3/м3= 0,63410-5% об.) (14)
Исходные данные:
диаметр аппарата - 3,6 м
объемный расход газа н.у. - 82000 м3/ч,
температура на входе в аппарат - 700K
начальная концентрация (% об.):
метана - 1,4
кислорода - 2,6
оксида азота - 0,13
начальная температура - 700 К
шаг по высоте слоя - 0,1 м
3.4. Расчет высоты слоя контактной массы.
Результаты расчета по программе для решения системы дифференциальных уравнений, реализующей метод Рунге-Кутта четвертого порядка, приведены далее. Счет по программе заканчивается, когда концентрация NOстановится меньше ПДК.
Результаты расчета:
Высота слоя катализатора h = 0.6 м
Концентрации: СО2= 0,222 % об.;СNO= 2,250 % об.;ССН4= 0,179 % об.
Температура Т = 1014,81 К
Таким образом, расчет показывает, что заданная концентрация NOдостигается при высоте контактной массы 0,6 м. В этом случае при диаметре контактного аппарата 3,6 м требуется объем контактной массы в 6,107 м3:
V=п *d^2 / 4 *h= 3.14 * 3.6^2 / 4 * 0.6 = 6.107 м3
3.5 Материальный баланс каталитического реактора.
Известно, что О2иNOпоступают в аппарат с нитрозными газами, имеющими в своем составе такжеN2, пары воды,NO2,N2O4и т.п. [3]. Примем для упрощения расчетов, что нитрозные газы состоят из азота и паров воды. Пусть последних после смешения нитрозных газов с метаном в смеси содержится 18 % об., а остальное – азот.
Реакции (1)и (2) протекают без изменения объема, суммарные объемы на входе и на выходе из аппарата будут одинаковыми.
Концентрация азота в газе на входе в аппарат:
У = 100 - (18 + 2,6 + 0,13 + 1,4) = 77,87 %
Количества реагентов на входе в аппарат:
Объемные расходы:
![]() м3/ч
м3/ч
![]() м3/ч
м3/ч
![]() м3/ч
м3/ч
![]() м3/ч
м3/ч
![]() м3/ч
м3/ч
Полученные значения вносим в таблицу 1. Затем по этим величинам с учетом соотношения (8) [1] рассчитаем массовые расходы каждого компонента и определяем суммарный расход смеси.
![]() кг/м3
кг/м3
mCH4=1148*0,7143=820,00кг/ч
![]() кг/м3
кг/м3
mO2=2132*1,4289=3045,7кг/ч
![]() кг/м3
кг/м3
mNO=1,3401*106,6=142,8 кг/ч
![]() кг/м3
кг/м3
mN2=63853,4*1,25=79816,75 кг/ч
![]() кг/м3
кг/м3
mH2O=0,804*14760=11860,7 кг/ч
![]() кг/м3
кг/м3
По вычисленным с помощью ЭВМ значениям концентраций находим объемные расходы газов на выходе из аппарата:
![]() м3/ч
м3/ч
![]() м3/ч
м3/ч
По количеству прореагировавшего O2по реакции (1) определяем количество образовавшихся водяных паров,СО2 и израсходованного метана:
VH2O=VO2=2132-182,04=1949,96 м3/ч
VCO2=VO2 /2=1949,96/2=974,98 м3/ч
VCH4=VO2 /2=974,98 м3/ч
