
- •Кафедра химии
- •7. Термодинамические процессы идеальных газов 39
- •8. Второй закон термодинамики 50
- •15. Циклы тепловых двигателей с газообразным рабочим телом 116
- •16. Циклы газотурбинных установок 134
- •17. Теплосиловые паровые циклы 151
- •18. Циклы холодильных установок 169
- •Введение
- •1. Основные понятия и определения
- •1.1. Основные термодинамические параметры состояния
- •1.2. Термодинамическая система
- •1.3. Термодинамический процесс
- •1.4. Теплота и работа
- •1.5. Термодинамическое равновесие
- •Контрольные вопросы
- •2. Состояние идеального газа
- •2.1. Основные законы идеальных газов
- •2.2. Уравнение состояния идеального газа
- •Контрольные вопросы
- •3. Смесь идеальных газов
- •3.1. Основные свойства газовых смесей
- •4. Реальные газы
- •4.1. Уравнение состояния Ван-дер-Ваальса
- •4.2. Уравнение м. П. Вукаловича и и. И. Новикова
- •Контрольные вопросы
- •5. Первый закон термодинамики
- •5.1. Внутренняя энергия
- •5.2. Работа расширения
- •5.3. Теплота
- •5.4. Аналитическое выражение первого закона термодинамики
- •5.5. Энтальпия
- •Контрольные вопросы
- •6. Теплоемкость газов. Энтропия
- •6.1. Основные определения
- •6.2. Удельная (массовая), объемная и мольная теплоемкости газов
- •6.3. Теплоемкость в изохорном и изобарном процессах
- •6.4. Молекулярно-кинетическая и квантовая теории теплоемкости
- •6.5. Истинная и средняя теплоемкости
- •6.6. Зависимость теплоемкости от температуры
- •6.7. Отношение удельных теплоемкостей ср и сυ. Показатель адиабаты
- •6.8. Определение qp и qυ для идеальных газов
- •6.9. Теплоемкость смеси идеальных газов
- •6.10. Энтропия
- •Контрольные вопросы
- •7. Термодинамические процессы идеальных газов
- •7.1. Основные определения
- •7.2. Изохорный процесс
- •7.3. Изобарный процесс
- •7.4. Изотермический процесс
- •7.5. Адиабатный процесс
- •7.6. Политропные процессы
- •Контрольные вопросы
- •8. Второй закон термодинамики
- •8.1. Основные положения
- •8.2. Круговые термодинамические процессы (циклы)
- •8.3. Термический кпд и холодильный коэффициент циклов
- •8.4. Прямой обратимый цикл Карно
- •8.5. Обратный обратимый цикл Карно
- •8.6. Математическое выражение второго закона термодинамики
- •8.7. Изменение энтропии в обратимых и необратимых процессах
- •Контрольные вопросы
- •9. Характеристические функции и термодинамические потенциалы. Равновесие систем
- •9.1. Характеристические функции состояния
- •9.2. Физический смысл изохорно-изотермического и изобарно-изотермического потенциалов
- •9.3. Термодинамическое учение о равновесии
- •9.4. Общие условия равновесия термодинамической системы
- •Контрольные вопросы
- •10. Водяной пар
- •10.1. Основные понятия и определения
- •10.2. Р, υ-диаграмма водяного пара
- •10.3. T, s-диаграмма водяного пара
- •10.4. I, s-диаграмма водяного пара
- •Контрольные вопросы
- •11. Истечение газов и паров
- •11.1. Первый закон термодинамики в применении к потоку движущегося газа
- •11.2. Работа проталкивания
- •11.3. Располагаемая работа
- •11.4. Адиабатный процесс истечения
- •11.5. Истечение из суживающегося сопла
- •11.6. Истечение идеального газа из комбинированного сопла Лаваля
- •Контрольные вопросы
- •12. Дросселирование газов и паров
- •12.1. Дросселирование газа
- •12.2. Изменение удельной энтропии и температуры при дросселировании
- •12.3. Дросселирование водяного пара
- •Контрольные вопросы
- •13. Влажный воздух
- •13.1. Параметры состояния влажного воздуха
- •13.2. Диаграмма состояния влажного атмосферного воздуха
- •Контрольные вопросы
- •14. Компрессоры
- •14.1. Классификация компрессорных машин
- •14.2. Поршневой компрессор. Индикаторная диаграмма идеального поршневого компрессора
- •14.3. Индикаторная диаграмма реального поршневого компрессора
- •14.4. Определение количества теплоты, отведенной от газа при различных процессах сжатия
- •14.5. Мощность привода и кпд компрессора
- •14.6. Многоступенчатое сжатие газа
- •Охлаждающей воды; 4, 15, 26 – вход рабочего тела – газа; 7, 18, 29 – выход сжатого газа;
- •Контрольные вопросы
- •15. Циклы тепловых двигателей с газообразным рабочим телом
- •15.1. Циклы поршневых двигателей внутреннего сгорания (двс)
- •15.2. Циклы двс с подводом теплоты при постоянном объеме
- •В изохорном процессе от степени сжатия и показателя адиабаты
- •15.3. Цикл двс с подводом теплоты при постоянном давлении (цикл Дизеля)
- •15.4. Цикл двс со смешанным подводом теплоты (цикл Тринклера)
- •15.5. Сравнение циклов поршневых двигателей внутреннего сгорания
- •15.6. Цикл двигателя Стирлинга
- •Двигателя Стирлинга при повороте коленчатого вала:
- •Объемов; 6, 7 – действительное изменение объемов
- •Контрольные вопросы
- •16. Циклы газотурбинных установок
- •16.1. Цикл гту с подводом теплоты при постоянном давлении
- •От степени повышения давления в турбокомпрессоре
- •16.2. Цикл гту с подводом теплоты при постоянном объеме
- •16.3. Методы повышения термического кпд гту
- •16.4. Цикл гту с регенерацией теплоты
- •С регенерацией и с изобарным подводом теплоты
- •С изохорным подводом теплоты и регенерацией
- •16.5. Цикл с многоступенчатым сжатием воздуха и промежуточным охлаждением
- •Сжатием в компрессоре и с регенерацией: 1 – топливный насос; 2 – камера сгорания;
- •Сжимаемого воздуха, промежуточным подогревом рабочего тела, с подводом теплоты при постоянном давлении
- •Контрольные вопросы
- •17. Теплосиловые паровые циклы
- •17.1. Цикл Карно
- •17.2. Цикл Ренкина
- •17.3. Влияние основных параметров на кпд цикла Ренкина
- •17.3.1. Влияние начального давления пара
- •17.3.2. Влияние начальной температуры пара
- •При различных значениях t1
- •17.3.3. Влияние конечного давления в конденсаторе
- •17.4. Цикл с вторичным перегревом пара
- •17.5. Регенеративный цикл паротурбинной установки
- •17.6. Теплофикационные циклы
- •Контрольные вопросы
- •18. Циклы холодильных установок
- •18.1. Основные понятия о работе холодильных установок
- •18.2. Цикл воздушной холодильной установки
- •18.3. Цикл парокомпрессионной холодильной установки
- •18.4. Цикл пароэжекторной холодильной установки
- •18.5. Цикл абсорбционной холодильной установки
- •18.6. Тепловой насос
- •Контрольные вопросы
- •Заключение
- •Библиографический список
- •Составители
7.5. Адиабатный процесс
Адиабатным называется процесс, протекающий без подвода и отвода теплоты, т. е. при отсутствии теплообмена рабочего тела с окружающей средой. Кривая процесса – адиабата (рис. 15).
Рис. 15. р, υ- и T, s-диаграммы адиабатного процесса |
Из уравнения первого закона термодинамики при q = 0 имеем
|
Интегрируя последнее
выражение при условии, что k = const
(поскольку ср = const
и сυ = const),
получим
 и
и
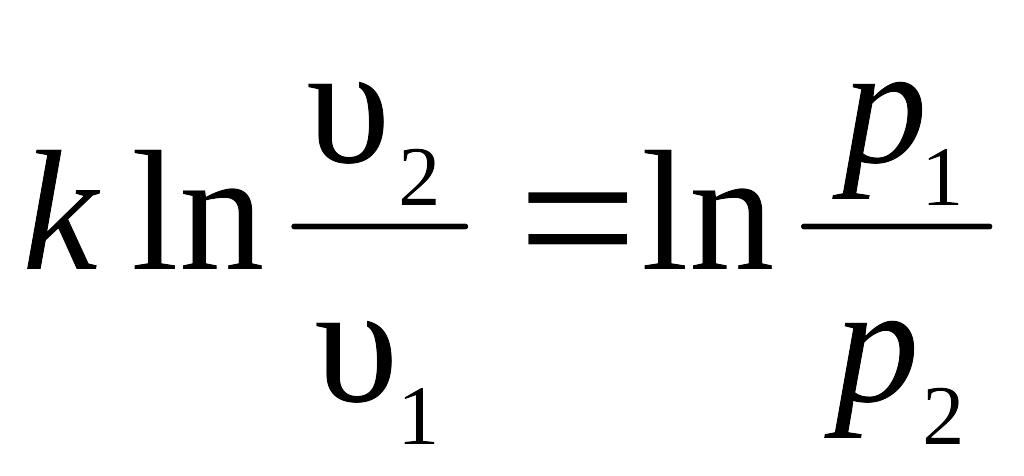 .
После потенцирования имеем
.
После потенцирования имеем
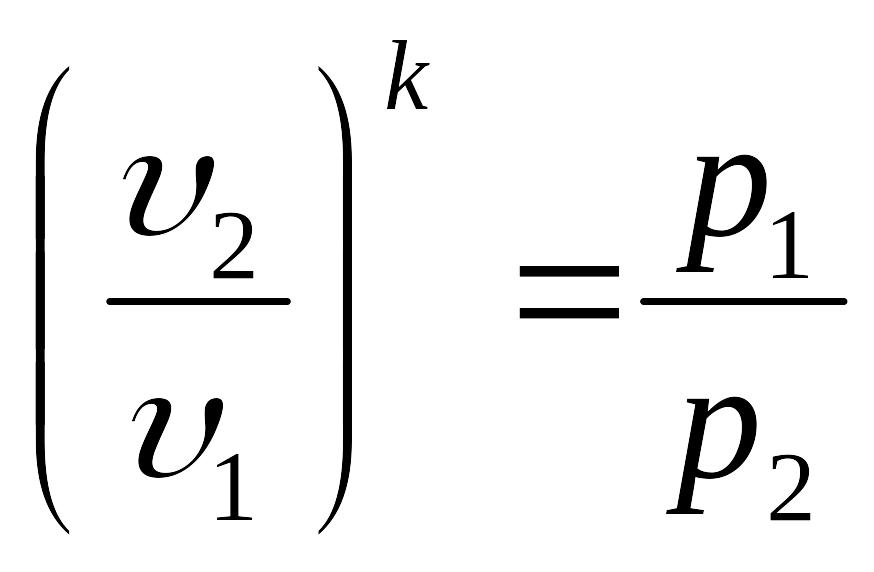 и
и
![]() .
.
Отсюда уравнение
адиабаты
![]()
Величина k называется показателем адиабаты.
Зависимость между основными параметрами в адиабатном процессе
Из уравнения
адиабаты следует, что
 и
и
 .
.
Если эти соотношения
параметров тела подставить в уравнение
состояния для крайних точек процесса
![]() ,
то после соответствующих преобразований
получим
,
то после соответствующих преобразований
получим
 .
.
Удельная работа
изменения объема
,
совершаемая телом над окружающей средой
при равновесном адиабатном процессе,
может быть вычислена по уравнению
адиабаты
 или
или
 .
.
Откуда
![]() .
.
Из данного выражения могут быть получены следующие формулы:
![]() и
и
![]() .
.
Отношение температур заменяем отношением объемов и давлений.
 .
.
Все зависимости между р, υ и Т и уравнения работы получены при условии k = const. При переменном k при расчетах берут среднее значение, соответствующее изменению температуры в процессе по уравнению:
 .
.
Уравнения первого закона термодинамики для адиабатного процесса:
![]() и
и
![]() .
.
Из этих выражений можно получить дифференциальное уравнение изоэнтропного (при постоянной удельной энтропии) процесса:
![]() .
.
В этом уравнении
![]() .
.
Согласно первому закону термодинамики, удельная работа изменения объема в адиабатном процессе получается за счет убыли удельной внутренней энергии тела.
При
cυ = const ![]()
При
сυ
≠
const ![]() .
.
Если газ расширяется, то его внутренняя энергия и температура убывают; если газ сжимается, то его внутренняя энергия и температура возрастают.
Удельная теплоемкость
в адиабатном процессе из выражения
![]() при q = 0
также равна нулю.
при q = 0
также равна нулю.
Располагаемая (полезная) внешняя работа в адиабатном процессе:

При
обратимом
адиабатном процессе идеального газа
располагаемая внешняя работа будет в
k
раз больше удельной работы изменения
объема и обратна ей по знаку:
![]() и
и
![]()
Графически располагаемая внешняя работа изображается на р, υ-диаграм-ме (пл. ABCD на рис. 16).
Рис. 16. Графическое изображение располагаемой внешней работы |
На рис. 16 видно,
что, поскольку k
> 1,
линия адиабаты (АВ)
идет круче линии изотермы: при адиабатном
расширении давление понижается
быстрее, чем при изотермическом, так
как в процессе расширения уменьшается
температура газа. Для обратимого
адиабатного процесса q = 0,
поэтому
|
Протекание необратимого адиабатного процесса не является изоэнтропным и независимо от его направления как при расширении, так и при сжатии сопровождается увеличением удельной энтропии. На рис. 12 обратимый адиабатный процесс изображается прямыми 0–b, d–c, необратимый адиабатный процесс расширения – кривая 0–с, процесс сжатия – с–e.


 или
или
 .
.