
- •1. Атомы, входящие в состав молекулы органического веще-
- •2. От строения молекул, т. Е. От того, в каком порядке
- •13) Циклоалканы(циклопарафины)
- •Гидратация
- •Гидрирование-
- •Реакция карбонилирования- Алкены в присутствии катализатора, высокой температуры и давления присоединяют co и h2 с образованием альдегидов]
- •Реакции электрофильного присоединения
- •2)Реакции гидрогалогенирования
- •3)Реакции карбонилирования , где х: он, or, ocor, nh2 и Пр. ,
- •22)Реакции циклобразования
- •24)Реакции образования гетероциклов
- •21) Получение
- •Реакции sn1
Гидратация
Реакция присоединения воды к алкенам протекает в присутствии серной кислоты
![]()
Реакция
протекает по правилу Марковникова.
Алкилирование
Присоединение алканов к
алкенам в присутствии
кислотного катализатора (HF или H2SO4)
при низких температурах приводит к
образованию углеводорода с большей
молекулярной массой и часто используется
в промышленности:![]() Данная
реакция также может протекать
по свободнорадикальному
механизму в
отсутствие катализатора при высокой
температуре и давлении. Для алкенов
также характерны следующие реакции
электрофильного присоединения]:
Присоединение спирта с
образованием простого
эфира:
Данная
реакция также может протекать
по свободнорадикальному
механизму в
отсутствие катализатора при высокой
температуре и давлении. Для алкенов
также характерны следующие реакции
электрофильного присоединения]:
Присоединение спирта с
образованием простого
эфира:

![]() Получение спиртов по
реакции оксимеркурирования-демеркурирования:
Получение спиртов по
реакции оксимеркурирования-демеркурирования:
![]() Присоединение хлорноватистой
кислоты с
образованием хлоргидринов:
Присоединение хлорноватистой
кислоты с
образованием хлоргидринов:
![]()
![]()
Реакции
радикального присоединения В
условиях, способствующих гомолитическому
разрыву связи, (высокая температура,
облучение, наличие свободных радикалов
и пр.) присоединение к алкенам происходит
порадикальному
механизму![]()
Механизм реакции:
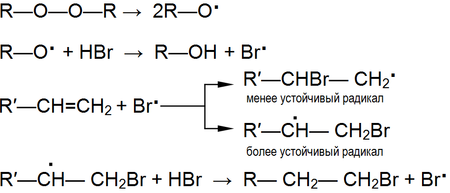
Гидрирование-
Гидрирование алкенов
непосредственно водородом происходит
только в присутствии катализатора.
Гетерогенными катализаторами гидрирования
служат платина, палладий, никель.
Реакции
радикального замещения-При
высоких температурах (более 400 °C)
реакции радикального присоединения,
носящие обратимый характер, подавляются.
В этом случае становится возможным
провести замещение атома водорода,
находящегося в аллильном положении
при сохранении двойной связи:![]() Окисление
происходит в зависимости от условий и
видов окислительных реагентов как с
разрывом двойной связи, так и с сохранением
углеродного скелета.Окисление
неорганическими окислителями-В
мягких условиях возможно окисление
посредством присоединения по двойной
связи двух гидроксильных групп:
Окисление
происходит в зависимости от условий и
видов окислительных реагентов как с
разрывом двойной связи, так и с сохранением
углеродного скелета.Окисление
неорганическими окислителями-В
мягких условиях возможно окисление
посредством присоединения по двойной
связи двух гидроксильных групп:![]() На
первом этапе происходит присоединение
оксида осмия к алкену, затем под действием
воосстановителя (Zn или
NaHSO3)
образовавшийся комплекс переходит
к диолу.
При
действии на алкены сильных окислителей
(KMnO4 или K2Cr2O7 в
среде Н2SO4)
при нагревании происходит разрыв
двойной связи:
На
первом этапе происходит присоединение
оксида осмия к алкену, затем под действием
воосстановителя (Zn или
NaHSO3)
образовавшийся комплекс переходит
к диолу.
При
действии на алкены сильных окислителей
(KMnO4 или K2Cr2O7 в
среде Н2SO4)
при нагревании происходит разрыв
двойной связи:![]()
![]() (кетон)
Окисление в присутствии солей
палладия окисляется
до ацетальдегида
(кетон)
Окисление в присутствии солей
палладия окисляется
до ацетальдегида![]() Реакция
идет в кислой среде и является промышленным
способом получения ацетальдегида.Озонолиз
алкенов
обычно проводят при низких температурах
(от −80 до −30 °C) в инертном растворителе
(гексан, тетрахлорметан, хлороформ, этилацетат и
пр.). Непосредственные продукты озонолиза
не выделяют, а подвергают дальнейшему
гидролизу, окислению или восстановлению.
Озонолиз в мягких
условиях:
алкен окисляется до альдегидов (в
случае монозамещенных вицинальных
углеродов), кетонов (в
случае дизамещенных вицинальных
углеродов) или смесиальдегида и кетона (в
случае три-замещенного у двойной связи
алкена).
Реакция
идет в кислой среде и является промышленным
способом получения ацетальдегида.Озонолиз
алкенов
обычно проводят при низких температурах
(от −80 до −30 °C) в инертном растворителе
(гексан, тетрахлорметан, хлороформ, этилацетат и
пр.). Непосредственные продукты озонолиза
не выделяют, а подвергают дальнейшему
гидролизу, окислению или восстановлению.
Озонолиз в мягких
условиях:
алкен окисляется до альдегидов (в
случае монозамещенных вицинальных
углеродов), кетонов (в
случае дизамещенных вицинальных
углеродов) или смесиальдегида и кетона (в
случае три-замещенного у двойной связи
алкена).
На первой стадии происходит присоединение озона с образованием озонида. Далее под действием восстановителя (например: Zn + CH3COOH) озонид разлагается:
![]() Если
взять более сильный восстановитель — алюмогидрид
лития,
продуктом реакции будут спирты.
Озонолиз в жёстких
условиях —
алкен окисляется до кислоты:
Если
взять более сильный восстановитель — алюмогидрид
лития,
продуктом реакции будут спирты.
Озонолиз в жёстких
условиях —
алкен окисляется до кислоты:![]()
