
- •Учебно-методические указания
- •240400 «Химическая технология органических веществ и топлива»,
- •Задача №1.2
- •Задача №1.3
- •Задача №1.4
- •Задача №1.5
- •Задача №1.6
- •Задача №1.7
- •Задача №2.2
- •Задача №2.3
- •Задача №2.4
- •Задача №2.5
- •Задача №2.6
- •Задача №2.7
- •Задача №2.8
- •Задача №2.9
- •Задача №2.10
- •Задача №2.11
- •Задача №2.12
- •Задача №2.13
- •Задача №2.14
- •Задача №2.15
- •Задача №2.16
- •Задача №2.17
- •Задача №2.18
- •Задача №2.19
- •Задача №2.20
- •Задача №2.21
- •Задача №3.6
- •Задача №3.7
- •Задача №3.8
- •Задача №3.9
- •Задача №3.10
- •Задача №3.11
Задача №2.2
Для газообразного 1,3-бутадиена теплоемкость СР в интервале температур 298 1500 К задана следующим уравнением:
СР = -0,707 + 81,282·10-3·Т - 53,463·10-6·Т2 кал/К·моль
Определить
среднюю теплоемкость
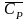 в интервале температур 400
500 К.
в интервале температур 400
500 К.
При решении использовать следующие формулы:
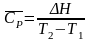 ,
,
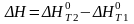 ,
,
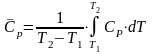
Задача №2.3
С использованием формулы Майера, вычислить теплоемкость метана Сv при 250С, если при той же температуре и давлении, равном 1атм, СР = 8,536 кал/К·моль. Считать, что метан:
идеальный газ;
реальный газ.
Задача №2.4
Графическим путем найти теплоту реакции дегидрирования этана до метана, ацетилена и водорода при температуре 1150 К, протекающей в газовой фазе, в стандартных условиях. Теплота этой реакции при стандартных условиях равна 246357 Дж, а зависимость теплоемкостей компонентов реакции от температуры выражается следующими данными:
Таблица 2.2 – Значения теплоемкостей компонентов при различных температурах, Дж/К·моль
T, К в-во |
298 |
400 |
500 |
600 |
700 |
800 |
900 |
1000 |
1100 |
1200 |
СН4 |
35,73 |
40,73 |
46,57 |
52,51 |
58,07 |
63,18 |
67,82 |
72,00 |
75,69 |
78,99 |
С2Н2 |
43,93 |
50,08 |
54,26 |
57,44 |
60,12 |
62,47 |
64,64 |
66,61 |
68,41 |
70,04 |
Н2 |
28,83 |
29,16 |
29,24 |
29,29 |
29,45 |
29,62 |
29,87 |
30,21 |
30,58 |
30,96 |
С2Н6 |
52,63 |
65,60 |
78,07 |
89,33 |
99,24 |
108,07 |
115,85 |
122,71 |
128,74 |
133,97 |
Задача №2.5
Возможна ли реакция дегидроциклизации н-октана в п-ксилол при температуре 800 К?
Таблица 2.3 – Значения термодинамических параметров компонентов при стандартных условиях
-
параметр вещество
н-октан
п-ксилол
Н2

-49,82
4,29
-
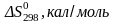
111,55
84,23
31,211
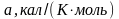
1,651
-6,196
6,95
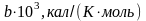
177,317
145,716
-0,2

-94,95
-83,786
0,48
Задачу решить двумя путями:
1) используя уравнения, основывающиеся на законах Кирхгофа;
2) применяя уравнения Темкина-Шварцмана- с использованием значений интегралов Mn:
Таблица 2.4 – Значения Mn для вычисления термодинамических функций по Темкину-Шварцману
Т, К |
М0 |
М1·10-3 |
М1·10-6 |
300 |
0,0000 |
0,0000 |
0,0000 |
400 |
0,0392 |
0,0130 |
0,0043 |
500 |
0,1133 |
0,0407 |
0,0149 |
600 |
0,1962 |
0,0759 |
0,0303 |
700 |
0,2794 |
0,1153 |
0,0498 |
800 |
0,3597 |
0,1574 |
0,0733 |
900 |
0,4361 |
0,2012 |
0,1004 |
1000 |
0,5088 |
0,2463 |
0,1134 |
1100 |
0,5765 |
0,2922 |
0,1652 |
1200 |
0,6410 |
0,3389 |
0,2029 |
1300 |
0,7019 |
0,3860 |
0,2440 |
1400 |
0,7595 |
0,4336 |
0,2886 |
Сравнить полученные величины и сделать вывод.
