
- •1.Структура и функции мембран.Виды трансмембранного переноса.Механизм работыNa-k-Атф-азы.
- •2.Функции и свойства белковых и липидных компонентов мембран. Белки-рецепторы.Транспортная передача сигналов в клетку.
- •3.Структура,классификация аминокислот по строению радикалов.
- •4.) Структура аминокислот. Заменимые и незаменимые аминокислоты, кетогенные и гликогенные.
- •5.) Физико-химические свойства аминокислот.
- •6.)Структура и функции белков.
- •8.Структура белков. Связи характерные для третичной и четвертичной структуры
- •9. Физико-химические свойства белков
- •11.Методы выделения и очистки белков.
- •12.Оценка степени очистки и Определение Mr.
- •Вопрос 22. Типы ферментативных реакций. Механизмы 2-хсубстратаых реакций. Механизм ферментативного действия пиридоксаль-зависимого фермента аланинаминотрансферазы.
- •Вопрос 23. Кинетика ферментативных реакций. Единицы активности. Измерения скорости реакции. Порядок реакции.
- •Вопрос 24. Зависимость скорости ферментативной реакции от рН, температуры, концентрации фермента, субстрата.
- •31. Применение ферментов в медицине. Способы определения активности ферментов в сыворотке крови.
- •32. Строение и функции нуклеотидов в живых организмах.
- •33. Биосинтез и катаболизм пиримидиновых нуклеотидав. Регуляция биосинтеза.
- •3 7. Строение и физико-химические свойства днк. Методы исследования структуры днк
- •38. Строение и функции рнк.
- •39.Репликация днк у прокариот. Свойства днк-полимераз прокариот. Лекарственные препараты, тормозящие репликацию.
- •40. Репликация днк у эукариот. Свойства днк-полимераз эукариот. Репликация днк и клеточный цикл.
- •41.Этапы процесса транскрипции. Днк-зависимые рнк-полимеразы эукариот и прокариот.
- •42.Инициация элонгации и терминация транскрипции у эу и про:
- •43. Процессинг у прокариот
- •44. Процессинг у эу:
- •45. Активирование аминокислот и необходимые компоненты этапов трансляции
- •46.Процесс трансляции и прокариот
- •47.Процесс трансляции у эукариот
- •Инициация трансляции
- •Механизм инициации трансляции у прокариот
- •Элонгация
- •51. Источники и пути расходования ак в организме. Азотистый баланс. Общая схема потока азота при катаболизме ак.
- •53. Цикл синтеза мочевины. Болезни, вызванные генетическими дефектами ферментов цнс. Методы определения концентрации мочевины в крови и моче.
- •Вопрос 60
- •Вопрос 61
- •Вопрос 62
- •64. Механизм сопряжения окисления и фосфорилирования.
- •65.Основной энергетический обмен и теплопродукция. Потоки важнейших метаболитов, поступающих в митохондрии и выходящих из них.
- •66.Токсичность активных форм кислорода (афк). Свободные радикалы. Перекисное окисление. Окислительный стресс. Механизмы антиоксидантной защиты.
- •70. Катаболизм глюкозы в условиях недостатка кислорода (анаэробный)
- •71. Катаболизм глюкозы в условиях недостатка кислорода (аэробный)
- •772.Глюконеогенез: локализация, функции, регуляция глюконеогенеза.
- •57. Биологически активные производные тирозина. Локализация синтеза и их роль в организме.
- •2.Меланины
- •58. Биосинтез креатина, креатинфосфата и креатинина в организме. Карнитин, карнозин, ансерин. Их роль в организме
- •59. Синтез и катаболизм гема. Значение конъюгирования продуктов метаболизма гема в печени.
- •75.Классификация и функции липидов.
- •76.Окисление жирных кислот.Реакции пути в-окисления.
- •77.Синтез и использование кетоновых тел.Изменения метаболизма при голодании.
- •78.Образование триацилглицеринов из углеводов.Метаболизм триацилглицеринов. Переваривание пищевых жиров. Депонирование и мобилизация жиров.
- •79.Стероиды.Роль и биосинтез холестерина в организме.
- •80.Механизмы формирования атеросклеротического повреждения сосудов.
- •82. Классификация, метаболизм, функции лп. Дислипопротеинемии.
- •83. Биологические активные вещества. Витамины.
- •67.Строение функции углеводов(ув)
- •69. Глюкоза как важнейший метаболит углеводного обмена. Источники и пути использования глюкозы в организме.
- •Вопрос 73. Соотношение превращений субстратов и процессов, происходящих в печени, мышцах и жировой ткани.
- •Регуляция гликолиза и глюконеогенеза.
- •Вопрос 74. Биосинтез и мобилизация гликогена. Схема регуляции активности гликогенфосфорилазы и гликогенсинтазы.
- •Гликгенолиз.
- •Ингибирование субстратом
- •90. Регуляторные полипептиды. Калликреин-кининовая и ренин-ангиотензиновая системы организма.
- •92.Интеграция и регуляция метаболизма. Направление потоков ключевых метаболитов между различными метаболическими путями.
- •84.Механизмы передачи гормонального сигнала.
- •Гидрофильные:
- •Липофильные
- •Вопрос 86.Синтез и секреция кортикостер.Г.Их роль
- •Вопрос87.Синтез и секреция гормонов щитов.Железы
- •Вопрос 88.Синтез и секреция половых гормонов.
- •Вопрос 89.Простагландины и их роль.
- •48.Лекарства и другие ингибиторы трансляции.
- •94.Интеграция метаболизма основных специализированных тканей организма человека.
- •50. Молекулярные механизмы канцерогенеза. Пути активации протоонкогенов.
- •49.Регуляция экспрессии генов.
- •13. Последовательность и методы изучения первичной и вторичной структуры белка
- •20.Классификация и номенклатура ферментов.
- •21. Механизмы ферментативного катализа. Энергия активации. Образование фермент-субстратного комплекса.
- •22.Типы ферментативных реакций.Механизмы 2-х субстратных реакций.Механизм ферментативного действия пиридоксаль-зависимого фермента аланинаминотрансферазы.
- •54 Катаболизм углеродного скелета ак. Кетогенные и гликогенные аминокислоты.
- •55 Биогенные амины:гистамины, серотонин, катехоламины. Происхождение и функции в организме.
- •56 Обмен фенилаланина и тирозина. Болезни, вызванные генетическими дефектами ферментов обмена этих аминокислот.
- •93 Интеграция и регуляция метаболизма. Стратегии регуляции потока метаболитов.
Ингибирование субстратом
Ингибирование субстратом — частный случай бесконкурентного ингибирования, когда две молекулы субстрата связываются с ферментом, что препятствует образованию продукта.
Схема и уравнение Михаэлиса-Ментен в случае ингибирования субстратом:
|
|
Необратимое ингибирование
Формирование стабильного комплекса ингибитора с ферментом, ведущее к его необратимой инактивации. Случай необратимого ингибирования можно обнаружить по тому признаку, что при разбавлении раствора не происходит повышения удельной активности фермента, как в случае обратимого ингибирования.
Вопрос№27Ингибиторы в медицине. Ингибиторы- яды ферментов.
Ингибиторы моноаминоксидазы (ИМАО, MAOI) — биологически активные вещества, способные ингибировать фермент моноаминоксидазу, т. е. замедлять или полностью блокировать его работу. К таковым относятся некоторые антидепрессанты, а также ряд природных веществ.
Ингиби́торы прото́нного насо́са (синонимы: Ингиби́торы прото́нной по́мпы, Ингиби́торы прото́нового насо́са, Ингиби́торы прото́новой по́мпы; часто употребляется аббревиатура ИПП, реже — ИПН) — лекарственные препараты, предназначенные для лечения кислотозависимых заболеваний желудочно-кишечного тракта за счёт снижения продукции соляной кислоты посредством блокирования в париетальных клетках слизистой оболочки желудка протонного насоса — Н+/К+-АТФазы. Относятся к антисекреторным препаратам.
Ингибиторы ангиотензин-превращающего фермента (АПФ) Фармакологическое действие ингибиторов АПФ обусловлено их влиянием на функциональное состояние ренин-ангиотензин-альдостероновой системы. При этом ингибиторы АПФ обладают необходимой структурой, позволяющей им взаимодействовать с атомом цинка в молекуле ангиотензин-превращающего фермента. Это сопровождается его инактивацией [14] и подавлением активности циркулирующей (плазменной) и тканевой (локальной) ангиотензиновых систем.
Препараты группы отличаются по выраженности и продолжительности ингибирующего влияния на ангиотензин I-превращающий фермент: в частности, рамиприл в организме превращается в активный метаболит - рамиприлат, сродство которого к ангиотензин I-превращающему ферменту в 42 раза выше, а комплекс рамиприл-фермент в 72 раза стабильнее, чем каптоприл-фермен
Ферментные яды,
вещества различной химической природы, специфически подавляющие активность определённого фермента или группы родственных ферментов. По существу Ф. я. представляют собой ингибиторы ферментов, которые даже в очень низких концентрациях угнетают жизненно важные физиологические функции организма. Многие ядовитые вещества, т. н. "нервные яды" (люизит), "дыхательные яды" (цианиды, H2S), пестициды (ядохимикаты) оказывают отравляющее действие в результате ингибирования отдельных ферментов (например, холинэстеразы у членистоногих). Изучение влияния Ф. я. на изолированные ферменты или ферментные системы позволяет целенаправленно искать эффективные противоядия к определённым отравляющим веществам или новые пестициды для борьбы с вредными насекомыми, клещами и т.д. и сорняками. Иногда термин "Ф. я." применяют для обозначения ферментов, входящих в состав ядов змей, пчёл, скорпионов и др. и разрушающих клетки крови или др. тканей человека и животных.
БИЛЕТ 63.
ОРГАНИЗАЦИЯ И ЛОКАЛИЗАЦИЯ е-ТРАНСПОРТНОЙ ЦЕПИ.
Принцип ядерной оболочки, имеют редокс-цепи. Участки редокс-цепи имеют выпячивания плазмолеммы.
По Грину имеется 4 комплекса е-транспортной цепи.
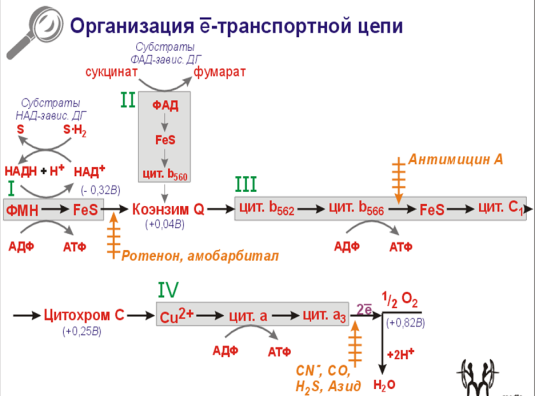
*Перечерченными оранжевыми стрелками указаны ингибиторы цепи.

КОМПЛЕКС 1:
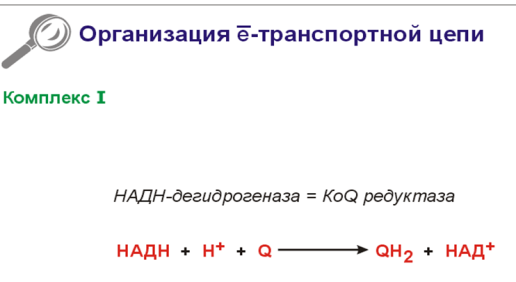
Комплекс 1-это точка входа протонов и электронов с HAДН+Н в е-транспортную цепь.
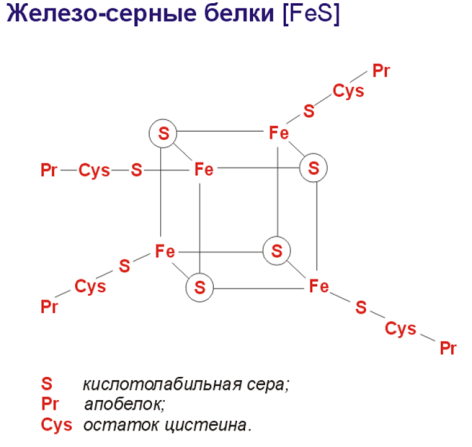

У человека убихинона-10, а у животных больше.
Семихинон-это когда убихинон на себя принимает 1 электрон и 1 протон.-восстанавливается наполовину.
Гидрохинон-восстановленная форма-убихинон принимает 2 электрона и 2 протона.
КОМПЛЕКС 2-это точка входа электронов и протонов с ФАДН2 в дыхательную цепь.
Цитохромопротеины-это хромопротеины, простетической группой которых является Fe, порфирины, гемоглобин.
У человека 5 цитохромов.
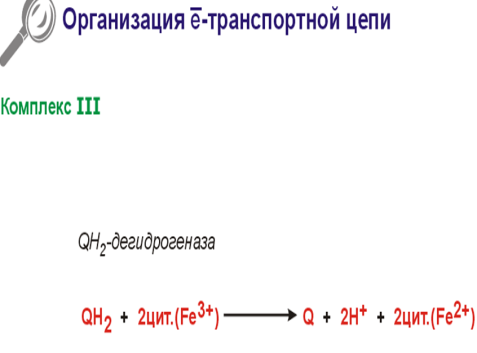
Цитохром С-очень хорошо растворим в воде.Перенос электронов от комплекса 3 на комплекс 4.

Цитохромоксидаза- ферментативные свойстава, каталитические свойства.

