
- •Соединения азота
- •2. Физико-химические основы и аппаратурное оформление процессов высокотемпературной фиксации атмосферного азота.
- •Термический метод
- •3 Теоретические основы получения низких температур
- •4Теоретические основы криогенной техники. Холодильные циклы. Технологические схемы н оборудование воздухе разделительных установок.
- •5. Теоретические основы разделения жидкого воздуха на азот и кислород. Устройство ректификационной установки.
- •7.Обзор и сравнение способов получения водорода
- •8 Газификация твердого топлива
- •9. Конверсия водяным паром
- •10. Основы конверсии природного газа кислородом и смесью окислителей. Оптимальный температурный режим.
- •11. Методы очистки газов от каталитических ядов. Очистка природного газа от сернистых соединений.
- •12.Технологическая схема 2-х ступенчатой каталитической конверсии природного газа под давлением 3-4 мПа.
- •13 Типовое оборудование стадии конверсии:
- •14.Устройство конверторов оксида углерода. Полочные, аксиальные и радиальные конверторы.
- •Аксиальный двухполочный конвертор.
- •Радиальный двухполочный конвертор.
- •17. Очистка конвертируемого газа от со2
- •Очистка конвертируемого газа р-рами на основе водных этанол-аминов.
- •Очистка конвертируемого газа водными р-рами карбонатов щелочных Ме
- •18. Физико-химические основы синтеза nh3. Равновесие и кинетика процесса. Виды катализаторов.
- •19. Обоснование оптимального режима синтеза аммиака
- •20. Промышленые способы синтеза амиака.Принцип.Схемы
- •21. Технологическая схема синтеза аммиака в агрегатах большой единичной мощности
- •22 Устройство колонны синтеза аммиака с полочной насадкой.
- •24 Физико-химические основы контактного окисления аммиака. Виды катализаторов. Оптимальный технологический режим.
- •26. Абсорбция оксидов азота осуществляется водой:
- •27Промышленые способы получения азотной кислоты
- •29. Методы обезвреживания хвостовых нитрозных газов в производстве азотной кислоты
- •30 Способы получения концентрированной азотной кислоты. Технологическая схема получения концентрированной азотной кислоты методом выпарки с водоотнимающимисредствами.
- •31. Прямой синтез конц. Hno3 из оксида азота
- •32.Вида азотных удобрений
- •Сульфат аммония
- •Аммонийной селитры
- •Карбамид
- •34. Физико-химические основы нейтрализации азотной кислоты аммиаком. Аппаратурное оформление процесса. Устройство оборудования.
- •35.Выпарка растворов аммиачной селитры. Гранулирование плава аммиачной селитры. Устройство основного оборудования.
- •36 Технологическая схема производства аммонийной селитры в ас-72
- •37. Физико-химические основы процесса синтеза
- •39.Технологическая схема карбамида с полным жидкостным рециклом.
- •40Технологическая схема производства карбамида (стрипинг процесс)
20. Промышленые способы синтеза амиака.Принцип.Схемы
1.Система, работающая под низким Р (10-15МПа)
2.Система, работающая под средним Р (25-35МПа)
3. Система, работающая под высоким Р (50-100МПа)
Схема системы низкого Р:
Синтез осуществляли при Р=10МПа на активном железном катализаторе. Т=400*С, W=3000, С(NH3)=8-10%
Система высокого Р(система Клода Казале):
Р=75-100МПа, W=100000, использовали обычные железные катализаторы, С(NH3)=25%
Схема Клода: разделение осуществлялось конденсацией путем охлаждения водой в водяных холодильниках. Предложено линейное расположение синтеза.









NH3Г
NH3Ж
Применения не нашла
С


NH3Ж
АВС
истема Казале: по циркуляционной схеме
Не получила широкого применения
Недостатки: 1)высокие энергетические затраты на получение АВС; 2)повышенные требования к конструкциям
Система среднего Р: первая в Германии.
С=10%. Поглощение водой – выделение аммиака. Используются усовершенствованные железные катализаторы
В 40-50г установили мощность до 200т/сут, в 80-ые гг – 1350-1500т/сут
При этих условиях концентрация аммиака составляет 14-15%. После колоны синтеза необходимо выделить прореагировавшую АВС
Методы выделения аммиака из прореагировавшей АВС : абсорбционный, конденсационный. 1)Выделение полного аммиака из газовой смеси получают не жидкий аммиак, а водный раствор (20-25%). При абсорбции водой происходит испарения воды. АВС нагревается водяным паром, но он является каталитическим ядом. 2) Выделение аммиака путем конденсации: охлаждение газовой смеси
T конд. NH3=-33,35*С. (Р=0.1МПа)
Чем ниже температура охлаждения, тем больше степень выделения аммиака, тем больше получается жидкого аммиака. Концентрация аммиака в газе после охлаждения определяется данным давлением.
С(NH3)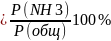
Т. к. процесс ведут под давлением, не обязательно охлаждать газовую смесь. Плотность газовой смеси велика, аммиак содержится в виде тумана.
Была предложена формула для расчета концентрации газовой смеси в зависимости от температуры и давления.
Lg
С(NH3)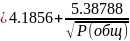 -
-

Для системы среднего давления концентрация аммиака составляет 3-3.5%. для достижения такой концентрации необходимо охлаждать до температуры 0- -5*С. Осуществляется двухступенчатая конденсация: 1ступень – охлаждение воздуха до 30-40*С. Остаточная концентрация 8-10% (в водяном холоде), 2 ступень – охлаждение в аммиачном холодильнике до 0- -5*С. При такой температуре С(ост)=3.5%.
В системе высокого давления выделение аммиака в одну ступень (в воздушных либо аммиачных холодильниках) получается весь аммиак в виде жидкого.
После охлаждения смеси жидкий аммиак дросселируется до 2МПа и подается в хранилище. При снижения давления образуются танковые газы. Непрореагировавшая АВС смешивается с новым потоком, сжимается и подается в цикл синтеза.
Основные стадии синтеза:
1.Сжатие АВС, очищенной от каталитических ядов
2. Смешение свежей АВС с циркуляционным газом
3. подогрев циркуляционного газа до температуры катализатора
4. синтез аммиака (реакционная смесь нагревается до 500*С)
5. прореагировавшая АВС подается на охлаждение
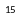
1- колонна синтеза; 2- т/о для подогрева воды; 3- выносной т/о; 4-воздушный холодильник; 5- сепаратор; 6- магнитный фильтр для улавливания kat-й пыли; 7- дроссельные вентили; 8- циркуляционный компрессор; 9- компрессор для сжатия свежей АВС; 10- конденсационная колона; 11,14,17- NH3–й холодильник; 12- хранилище ж.NH3; 13- конденсационная колона для выделения NH3; 15,18- сборник ж. NH3; 16- конденсационная колона для выделения NH3. из танкового газа.
