
- •Законы стехиометрии
- •Субатомные частицы
- •Электроны в атоме
- •7. Изменения химических свойств элементов и их соединений в группах:
- •Меняется размер атома
- •Изменения химических свойств элементов и их соединений в периодах:
- •Гомогенный катализ
- •Гетерогенный катализ
- •Аллотропные модификации углерода Кристаллический углерод
- •[Править]Аморфный углерод
- •В электротехнике
Аллотропные модификации углерода Кристаллический углерод
Алмаз
Графен
Графит
Карбин
Лонсдейлит
Наноалмаз
Фуллерены
Фуллерит
Углеродное волокно
Углеродные нановолокна
Углеродные нанотрубки
[Править]Аморфный углерод
Активированный уголь
Древесный уголь
Ископаемый уголь: антрацит и др.
Кокс каменноугольный, нефтяной и др.
Стеклоуглерод
Техуглерод
Сажа
Углеродная нанопена
Электронные орбитали атома углерода могут иметь различную геометрию, в зависимости от степени гибридизации его электронных орбиталей. Существует три основных геометрии атома углерода.
тетраэдрическая, образуется при смешении одного s- и трех p-электронов (sp3-гибридизация). Атом углерода находится в центре тетраэдра, связан четырьмя эквивалентными σ-связями с атомами углерода или иными в вершинах тетраэдра. Такой геометрии атома углерода соответствуют аллотропные модификации углерода алмаз и лонсдейлит. Такой гибридизацией обладает углерод, например, в метане и других углеводородах.
тригональная, образуется при смешении одной s- и двух p-электронных орбиталей (sp2-гибридизация). Атом углерода имеет три равноценные σ-связи, расположенные в одной плоскости под углом 120° друг к другу. Не участвующая в гибридизации p-орбиталь, расположенная перпендикулярно плоскости σ-связей, используется для образования π-связи с другими атомами. Такая геометрия углерода характерна для графита, фенола и др.
дигональная, образуется при смешении одного s- и одного p-электронов (sp-гибридизация). При этом два электронных облака вытянуты вдоль одного направления и имеют вид несимметричных гантелей. Два других р-электрона дают π-связи. Углерод с такой геометрией атома образует особую аллотропную модификацию — карбин.
При обычных температурах углерод химически инертен, при достаточно высоких соединяется со многими элементами, проявляет сильные восстановительные свойства. Химическая активность разных форм углерода убывает в ряду: аморфный углерод, графит, алмаз, на воздухе они воспламеняются при температурах соответственно выше 300—500 °C, 600—700 °C и 850—1000 °C.
Степени окисления +4 (напр., CO2), −4 (напр., CH4), редко +2 (СО, карбонилы металлов), +3 (C2N2); сродство к электрону 1,27эВ; энергия ионизации при последовательном переходе от С0 к С4+ соответственно 11,2604, 24,383, 47,871 и 64,19 эВ.
Кремний — элемент главной подгруппы четвёртой группы третьего периода периодической системы химических элементовД. И. Менделеева, с атомным номером 14. Обозначается символом S Кристаллическая решётка кремния кубическая гранецентрированная типа алмаза, параметр а = 0,54307 нм (при высоких давлениях получены и другие полиморфные модификации кремния), но из-за большей длины связи между атомами Si—Si по сравнению с длиной связи С—С твёрдость кремния значительно меньше, чем алмаза. Кремний хрупок, только при нагревании выше 800 °C он становится пластичным веществом. Интересно, что кремний прозрачен для инфракрасного излучения начиная с длины волны 1,1 мкм. Собственная концентрация носителей заряда — 5,81·1015 м−3(для температуры 300 K). При нормальных условиях кремний химически малоактивен и активно реагирует только с газообразным фтором, при этом образуется летучий тетрафторид кремния SiF4. Такая «неактивность» кремния связана с пассивацией поверхности наноразмерным слоем диоксида кремния, немедленно образующегося в присутствии кислорода, воздуха или воды (водяных паров). С водородом кремний непосредственно не реагирует, соединения кремния с водородом — силаны с общей формулой SinH2n+2 — получают косвенным путем. Моносилан SiH4 (его часто называют просто силаном) выделяется при взаимодействии силицидов металлов с растворами кислот, например:
![]()
С азотом кремний при температуре около 1000 °C образует нитрид Si3N4, с бором — термически и химически стойкие боридыSiB3, SiB6 и SiB12.
При температурах свыше 1000С °C можно получить соединение кремния и его ближайшего аналога по таблице Менделеева —углерода — карбид кремния SiC
Технический кремний находит следующие применения:
сырьё для металлургических производств: компонент сплава (бронзы, силумин); раскислитель (при выплавке чугуна); модификатор свойств металлов или легирующий элемент (например, добавка определённого количества кремния при производстве трансформаторных сталей уменьшает коэрцитивную силу готового продукта) и т. п.;
сырьё для производства более чистого поликристаллического кремния и очищенного металлургического кремния (в литературе «umg-Si»);
сырьё для производства кремнийорганических материалов, силанов;
иногда кремний технической чистоты и его сплав с железом (ферросилиций) используется для производства водорода в полевых условиях;
для производства солнечных батарей.
Графит используется в карандашной промышленности. Также его используют в качестве смазки при особо высоких или низких температурах.
Алмаз, благодаря исключительной твердости, незаменимый абразивный материал. Алмазным напылением обладают шлифовальные насадки бормашин. Кроме этого, ограненные алмазы — бриллианты используются в качестве драгоценных камней в ювелирных украшениях. Благодаря редкости, высоким декоративным качествам и стечению исторических обстоятельств, бриллиант неизменно является самым дорогим драгоценным камнем. Исключительно высокая теплопроводностьалмаза (до 2000 Вт/м·К) делает его перспективным материалом для полупроводниковой техники в качестве подложек дляпроцессоров. Но относительно высокая цена (около 50 долларов/грамм) и сложность обработки алмаза ограничивают его применение в этой области.
В фармакологии и медицине широко используются различные соединения углерода — производные угольной кислоты и карбоновых кислот, различные гетероциклы, полимеры и другие соединения. Так, карболен (активированный уголь), применяется для абсорбции и выведения из организма различных токсинов; графит (в виде мазей) — для лечения кожных заболеваний; радиоактивные изотопы углерода — для научных исследований (радиоуглеродный анализ).
Углерод играет огромную роль в жизни человека. Его применения столь же разнообразны, как сам этот многоликий элемент. В частности углерод является неотъемлемой составляющей стали (до 2,14 % масс.) и чугуна (более 2,14 % масс.)
44 Кислоро́д — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 8. Обозначается символом O (лат. Oxygenium). Кислород — химически активный неметалл, является самым лёгким элементом из группы халькогенов. Простое вещество кислород (CAS-номер: 7782-44-7) при нормальных условиях — газ без цвета, вкуса и запаха,молекула которого состоит из двух атомов кислорода (формула O2), в связи с чем его также называют дикислород. Жидкий кислород имеет светло-голубой цвет, а твёрдый представляет собой кристаллы светло-синего цвета.
Существуют и другие аллотропные формы кислорода, например, озон(CAS-номер: 10028-15-6) — при нормальных условиях газ голубого цвета со специфическим запахом, молекула которого состоит из трёх атомов кислорода (формула O3).
ри нормальных условиях кислород — это газ без цвета, вкуса и запаха.
1 л его имеет массу 1,429 г. Немного тяжелее воздуха. Слабо растворяется в воде(4,9 мл/100 г при 0 °C, 2,09 мл/100 г при 50 °C) и спирте (2,78 мл/100 г при 25 °C). Хорошо растворяется в расплавленном серебре (22 объёма O2 в 1 объёме Ag при 961 °C). Является парамагнетиком.
При нагревании газообразного кислорода происходит его обратимая диссоциация на атомы: при 2000 °C — 0,03 %, при 2600 °C — 1 %, 4000 °C — 59 %, 6000 °C — 99,5 %.
Жидкий кислород (температура кипения −182,98 °C) — это бледно-голубая жидкость
Твёрдый кислород (температура плавления −218,35°C) — синиекристаллы ильный окислитель, взаимодействует практически со всеми элементами, образуя оксиды. Степень окисления −2. Как правило, реакция окисления протекает с выделением тепла и ускоряется при повышении температуры (см. Горение). Пример реакций, протекающих при комнатной температуре:
![]()
![]()
Окисляет соединения, которые содержат элементы с не максимальной степенью окисления:
![]()
Окисляет большинство органических соединений:
![]()
При определённых условиях можно провести мягкое окисление органического соединения:
![]()
Кислород реагирует непосредственно (при нормальных условиях, при нагревании и/или в присутствии катализаторов) со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета. Косвенным путём получены оксиды золота и тяжёлых инертных газов (Xe, Rn). Во всех двухэлементных соединениях кислорода с другими элементами кислород играет роль окислителя, кроме соединений со фтором (см. ниже #фториды кислорода)
Озо́н (от др.-греч. ὄζω — пахну) — состоящая из трёхатомных молекул O3 аллотропнаямодификация кислорода. При нормальных условиях — голубой газ. При сжижении превращается в жидкость цвета индиго. В твёрдом виде представляет собой тёмно-синие, практически чёрные кристаллы. Молекулярная масса — 48 а.е.м.
Плотность газа при нормальных условиях — 2,1445 г/дм³. Относительная плотность газа по кислороду 1,5; по воздуху — 1,62 (1,658[4]).
Плотность жидкости при −183 °C — 1,71 г/см³
Температура кипения — −111,9 °C. Жидкий озон — тёмно-фиолетового цвета.
Температура плавления — −197,2 ± 0,2 °С (приводимая обычно т.пл. −251,4 °C ошибочна, так как при её определении не учитывалась большая способность озона к переохлаждению)[5]. В твёрдом состоянии — чёрного цвета с фиолетовым отблеском.
Растворимость в воде при 0 °С — 0,394 кг/м³ (0,494 л/кг), она в 10 раз выше по сравнению с кислородом.
В газообразном состоянии озон диамагнитен, в жидком — слабопарамагнитен.
Запах — резкий, специфический «металлический» (по Менделееву — «запах раков»). При больших концентрациях напоминает запах хлора. Запах ощутим даже при разбавлении 1 : 100000.
Образование озона проходит по обратимой реакции:
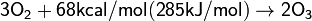
Молекула О3 неустойчива и при достаточных концентрациях в воздухе при нормальных условиях самопроизвольно за несколько десятков минут[6] превращается в O2 с выделением тепла. Повышение температуры и понижение давления увеличивают скорость перехода в двухатомное состояние. При больших концентрациях переход может носить взрывнойхарактер. Контакт озона даже с малыми количествами органических веществ, некоторых металлов или их окислов резко ускоряет превращение.
В присутствии небольших количеств HNO3 озон стабилизируется, а в герметичных сосудах из стекла, некоторых пластмасс или чистых металлов озон при низких температурах (—78 °С) практически не разлагается.
Озон — мощный окислитель, намного более реакционноспособный, чем двухатомный кислород. Окисляет почти все металлы(за исключением золота, платины и иридия) до их высших степеней окисления. Окисляет многие неметаллы. Продуктом реакции в основном является кислород.
45. Оксид углерода (II) (угарный газ, окись углерода, монооксид углерода) — бесцветный ядовитый газ (при нормальных условиях) без вкуса и запаха. Химическая формула — CO. Нижний и верхний концентрационные пределы распространения пламени: от 12,5 до 74 % (по объёму)[1]. Оксид углерода (II) представляет собой бесцветный газ без вкуса и запаха. Горюч. Так называемый «запах угарного газа» на самом деле представляет собой запах органических примесей. Основными типами химических реакций, в которых участвует оксид углерода (II), являются реакции присоединения иокислительно-восстановительные реакции, в которых он проявляет восстановительные свойства. Окисление СО в растворе часто идёт с заметной скоростью лишь в присутствии катализатора. Температура горения CO может достигать 2100 °C, она является цепной, причём инициаторами служат небольшие количества водородсодержащих соединений (вода, аммиак, сероводород и др.) Оксид углерода (II) реагирует с галогенами. Наибольшее практическое применение получила реакция с хлором:
![]()
Оксид углерода (II) реагирует с халькогенами. С серой образует сероксид углерода COS, реакция идёт при нагревании, по уравнению:
![]() ΔG°298 =
−229 кДж, ΔS°298 =
−134 Дж/K
ΔG°298 =
−229 кДж, ΔS°298 =
−134 Дж/K
Оксид углерода(IV) (углекислый газ, диоксид углерода, двуокись углерода,угольный ангидрид) — CO2, бесцветный газ (в нормальных условиях), без запаха, со слегка кисловатым вкусом. Плотность при нормальных условиях 1,97 кг/м³. При атмосферном давлении диоксид углерода не существует в жидком состоянии, переходя непосредственно из твёрдого состояния в газообразное. Твёрдый диоксид углерода называют сухим льдом. По химическим свойствам диоксид углерода относится к кислотным оксидам. При растворении в воде образует угольную кислоту. Реагирует со щёлочами с образованием карбонатов и гидрокарбонатов. Вступает в реакции электрофильного замещения (например, с фенолом ) и нуклеофильного присоединения (например, с магнийорганическими соединениями).
Оксид углерода (IV) – углекислый газ, газ без цвета и запаха, тяжелее воздуха, растворим в воде, при сильном охлаждении кристаллизуется в виде белой снегообразной массы – «сухого льда». При атмосферном давлении он не плавится, а испаряется, температура сублимации -78 °С. Углекислый газ образуется при гниении и горении органических веществ. Содержится в воздухе и минеральных источниках, выделяется при дыхании животных и растений. Мало растворим в воде (1 объем углекислого газа в одном объеме воды при 15 °С). Углекислый газ является тяжелым, по сравнению с воздухом, газом без цвета и запаха. Воздействие его повышенных концентраций на живые организмы относит его к удушающим газам (англ.)русск.. Незначительные повышения концентрации до 2-4% в непроветриваемых помещениях приводят к развитию сонливости и слабости. Опасными концентрациями считаются уровни 7-10%, при которых развивается удушье, проявляющее себя в головной боли, головокружении, расстройстве слуха и в потери сознания в течение периода времени от нескольких минут до одного часа.[3] Отравление этим газом не приводит к долговременным последствиям и после его завершения происходит полное восстановление организма.
46. p-блок в периодической таблице элементов — электронная оболочка атомов, валентныеэлектроны которых с наивысшей энергией занимают p-орбиталь.
В p-блок входят последние шесть групп главной подгруппы, исключая гелий (который находится в s-блоке). Данный блок содержит все неметаллы (исключая водород и гелий) и полуметаллы, а также некоторые металлы.
P-блок содержит в себе элементы, которые имеют различные свойства, как физические, так и механические. P-неметаллы — это, как правило, высокореакционные вещества, имеющие сильную электроотрицательность, p-металлы — умеренно активные металлы, причём их активность повышается к низу таблицы химических элементов.
1. Основной характер оксидов R2O5 увеличивается, а кислотный - ослабевает с увеличением порядкового номера.
2. Гидроксиды всех элементов в пятивалентном состоянии имеют кислотный характер.
3. Основной характер гидроксидов R(OH)3 увеличивается, а кислотный - ослабевает с увеличением порядкого номера.
RO33- + 3H+ = R(OH)3 = R3+ + 3OH- (R - элемент)
4. As, Sb, и Bi плохо растворимы в воде.
5. Восстановительные свойства водородных соединений RH3 усиливаются, а устойчивость уменьшается с увеличением порядкого номера.
В ряду - N - P - As - Sb - Bi увеличиваются размеры атомов, ослабляется притяжение валентных электронов к ядру, ослабляются неметаллические свойства, возрастают металлические свойства, ЭО уменьшается.
N, P - типичные неметаллы
As, Sb - проявляют неметаллические и металлические свойства
Bi - типичный металл
P, As и Bi существуют в твердом состоянии в нескольких модификациях.
47. Кислоро́д — элемент 16-й группы (по устаревшей классификации — главной подгруппы VI группы), второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 8. Обозначается символом O (лат. Oxygenium). Кислород — химически активный неметалл, является самым лёгким элементом из группы халькогенов. Простое вещество кислород (CAS-номер: 7782-44-7) при нормальных условиях — газ без цвета, вкуса и запаха,молекула которого состоит из двух атомов кислорода (формула O2), в связи с чем его также называют дикислород. Жидкий кислород имеет светло-голубой цвет, а твёрдый представляет собой кристаллы светло-синего цвета.
Существуют и другие аллотропные формы кислорода, например, озон(CAS-номер: 10028-15-6) — при нормальных условиях газ голубого цвета со специфическим запахом, молекула которого состоит из трёх атомов кислорода (формула O3).
ри нормальных условиях кислород — это газ без цвета, вкуса и запаха.
1 л его имеет массу 1,429 г. Немного тяжелее воздуха. Слабо растворяется в воде(4,9 мл/100 г при 0 °C, 2,09 мл/100 г при 50 °C) и спирте (2,78 мл/100 г при 25 °C). Хорошо растворяется в расплавленном серебре (22 объёма O2 в 1 объёме Ag при 961 °C). Является парамагнетиком.
При нагревании газообразного кислорода происходит его обратимая диссоциация на атомы: при 2000 °C — 0,03 %, при 2600 °C — 1 %, 4000 °C — 59 %, 6000 °C — 99,5 %.
Жидкий кислород (температура кипения −182,98 °C) — это бледно-голубая жидкость
Твёрдый кислород (температура плавления −218,35°C) — синиекристаллы ильный окислитель, взаимодействует практически со всеми элементами, образуя оксиды. Степень окисления −2. Как правило, реакция окисления протекает с выделением тепла и ускоряется при повышении температуры (см. Горение). Пример реакций, протекающих при комнатной температуре:
Окисляет соединения, которые содержат элементы с не максимальной степенью окисления:
Окисляет большинство органических соединений:
При определённых условиях можно провести мягкое окисление органического соединения:
Кислород реагирует непосредственно (при нормальных условиях, при нагревании и/или в присутствии катализаторов) со всеми простыми веществами, кроме Au и инертных газов (He, Ne, Ar, Kr, Xe, Rn); реакции с галогенами происходят под воздействием электрического разряда или ультрафиолета. Косвенным путём получены оксиды золота и тяжёлых инертных газов (Xe, Rn). Во всех двухэлементных соединениях кислорода с другими элементами кислород играет роль окислителя, кроме соединений со фтором (см. ниже #фториды кислорода)
Широкое промышленное применение кислорода началось в середине XX века, после изобретения турбодетандеров — устройств для сжижения и разделения жидкого воздуха. Кислород в баллонах голубого цвета широко используется для газопламенной резки и сварки металлов. В качестве окислителя для ракетного топлива применяется жидкий кислород, пероксид водорода, азотная кислота и другие богатые кислородом соединения. Смесь жидкого кислорода и жидкого озона — один из самых мощных окислителей ракетного топлива (удельный импульс смеси водород — озон превышает удельный импульс для пары водород-фтор и водород-фторид кислорода). Медицинский кислород хранится в металлических газовых баллонах высокого давления (для сжатых или сжиженных газов) голубого цвета различной ёмкости от 1,2 до 10,0 литров под давлением до 15 МПа (150 атм) и используется для обогащения дыхательных газовых смесей в наркозной аппаратуре, при нарушении дыхания, для купирования приступа бронхиальной астмы, устранения гипоксии любого генеза, при декомпрессионной болезни, для лечения патологии желудочно-кишечного тракта в виде кислородных коктейлей. пищевой промышленности кислород зарегистрирован в качестве пищевой добавки E948
Азо́т — элемент 15-й группы (по устаревшей классификации — главной подгруппы пятой группы) второго периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 7. Обозначается символом N (лат. Nitrogenium). Простое вещество азот (CAS-номер: 7727-37-9) — достаточно инертный при нормальных условиях двухатомный газ без цвета, вкуса и запаха (формула N2), из которого на три четверти состоит земная атмосфера. Азот является элементом, необходимым для существования животных и растений, он входит в состав белков (16—18 % по массе), аминокислот, нуклеиновых кислот, нуклеопротеидов, хлорофилла, гемоглобина и др При нормальных условиях азот это бесцветный газ, не имеет запаха, мало растворим в воде (2,3 мл/100г при 0 °C, 0,8 мл/100 г при 80 °C), плотность 1,2506 кг/м³ (при н.у.).
В жидком состоянии (темп. кипения −195,8 °C) — бесцветная, подвижная, как вода, жидкость. Плотность жидкого азота 808 кг/м³. При контакте с воздухом поглощает из него кислород.
При −209,86 °C азот переходит в твердое состояние в виде снегоподобной массы или больших белоснежных кристаллов. При контакте с воздухом поглощает из него кислород, при этом плавится, образуя раствор кислорода в азоте.
Азот в свободном состоянии существует в форме двухатомных молекул N2, электронная конфигурация которых описывается формулой σs²σs*2πx, y4σz², что соответствует тройной связи между молекулами азота N≡N (длина связи dN≡N = 0,1095 нм). Вследствие этого молекула азота крайне прочна, для реакции диссоциации N2 ↔ 2N изменение энтальпии в реакции ΔH°298=945 кДж/моль[4], константа скорости реакции К298=10−120, то есть диссоциация молекул азота при нормальных условиях практически не происходит (равновесие практически полностью сдвинуто влево). Молекула азота неполярна и слабо поляризуется, силы взаимодействия между молекулами очень слабые, поэтому в обычных условиях азот газообразен. Ввиду своей значительной инертности азот при обычных условиях реагирует только с литием:
![]()
при нагревании он реагирует с некоторыми другими металлами и неметаллами, также образуя нитриды:
![]()
![]()
Наибольшее практическое значение имеет нитрид водорода (аммиак) NH3, получаемый взаимодействием водорода с азотом
В электрическом разряде реагирует с кислородом, образуя оксид азота(II) NO.
Описано несколько десятков комплексов с молекулярным азотом.
Соединения азота в степени окисления −3 представлены нитридами, из которых практически наиболее важен аммиак;
Соединения азота в степени окисления −2 менее характерны, представлены пернитридами, из которых самый важный пернитрид водорода N2H4 или гидразин (существует также крайне неустойчивый пернитрид водорода N2H2, диимид);
Соединения азота в степени окисления −1 NH2OH (гидроксиламин) — неустойчивое основание, применяющееся, наряду с солями гидроксиламмония, в органическом синтезе;
Соединения азота в степени окисления +1 оксид азота(I) N2O (закись азота, веселящий газ);
Соединения азота в степени окисления +2 оксид азота(II) NO (монооксид азота);
Соединения азота в степени окисления +3 оксид азота(III) N2O3, азотистая кислота, производные аниона NO2−,трифторид азота (NF3);
Соединения азота в степени окисления +4 оксид азота(IV) NO2 (диоксид азота, бурый газ);
Соединения азота в степени окисления +5 оксид азота(V) N2O5, азотная кислота, её соли — нитраты и другие производные, а также тетрафтораммоний NF4+ и его сол
Промышленные применения газообразного азота обусловлены его инертными свойствами. Газообразный азот пожаро- и взрывобезопасен, препятствует окислению, гниению. В нефтехимии азот применяется для продувки резервуаров и трубопроводов, проверки работы трубопроводов под давлением, увеличения выработки месторождений. В горнодобывающем деле азот может использоваться для создания в шахтах взрывобезопасной среды, для распирания пластов породы. В производстве электроники азот применяется для продувки областей, не допускающих наличия окисляющего кислорода. Если в процессе, традиционно проходящем с использованием воздуха, окисление или гниение являются негативными факторами — азот может успешно заместить воздух. Газообразным азотом заполняют камеры шин шасси летательных аппаратов. Заморозка жидким азотом живых существ с возможностью последующей их разморозки проблематична. Проблема заключается в невозможности заморозить (и разморозить) существо достаточно быстро, чтобы неоднородность заморозки не сказалась на его жизненных функциях.
48. Несолеобразующий оксид. При нагревании разлагается на азот и кислород. При высоких концентрациях N2O возбуждает нервную систему («веселящий газ»). В медицине N2O применяют как слабое средство для наркоза.Окси́ды азо́та — неорганические бинарные соединения азота с кислородом.
Оксид азота NO (монооксид азота) — бесцветный газ, незначительно растворим в воде. Не взаимодействует с водой, растворами кислот и щелочей. Оксид азота (II) — очень реакционное соединение, может вступать в реакции присоединения с рядом солей (нитрозосоли), с галогенами (напр., нитрозилхлорид NOCl), органическими соединениями. При обычной температуре NO соединяется с кислородом с образованием NO2. Оксид NO получают каталитическим окислением при производстве азотной кислоты.
Оксид N2O3 (триоксид диазота, азотистый ангидрид) — темно-синяя жидкость, неустойчивая при обычных условиях, взаимодействует с водой, образуя азотистую кислоту HNO2.
Оксид азота NO2 (диоксид азота) — бурый газ, токсичен, тяжелее воздуха, легко сжижается. При комнатной температуре NO2находится в смеси с его бесцветным димером N2O4, приблизительно 1:1. Взаимодействует с водой:
![]()
и растворами щелочей:
![]()
Сильный окислитель. Многие вещества (уголь, сера, фосфор, органические соединения) могут гореть в NO2. Этот оксид окисляет SO2 до SO3, на этой реакции основан нитрозный метод получения серной кислоты. Раздражает дыхательные пути, при больших концентрациях появляется отёк легких.
Оксид азота N2O5 (пентаоксид диазота, азотный ангидрид) — бесцветное кристаллическое вещество, легко разлагается на NO2 и О2. Сильный окислитель. В воде легко растворяется с образованием азотной кислоты HNO3.
![]()
Тринитрамид открыт в 2010 году. Является перспективным кандидатом на роль высокоэффективного ракетного топлива, однако на данный момент неизвестно, является ли устойчивой твёрдая фаза вещества.
N40 Существует при температуре ниже −50 °C как бледно-жёлтое твёрдое вещество, выше этой температуры разлагается на N2O и N2.
Азотные удобрения — неорганические и органические азотосодержащие вещества, которые вносят в почву для повышенияурожайности. К минеральным азотным удобрениям относят амидные, аммиачные и нитратные. Азотные удобрения получают главным образом из синтетического аммиака. Из-за высокой мобильности соединений азота его низкое содержание в почве часто лимитирует развитие культурных растений, поэтому внесение азотных удобрений вызывает большой положительный эффект.
Из всех типов удобрений азотные наиболее подвержены воздействию со стороны почвенных микроорганизмов. В первую неделю после внесения до 70 % массы удобрения потребляется бактериями и грибами (иммобилизуются), лишь после их гибели входящий в их состав азот может использоваться растениями. Большие потери азота удобрений происходят из-за выноса легкорастворимых нитратов и солей аммония из почвенного профиля, а также в ходе денитрификации (газообразные потери) и из-за нитрификации (образование нитратов и их вынос). В итоге коэффициент использования удобрений растениями редко достигает 50 %, их применение может вызывать эвтрофикацию близлежащих водоёмов. Образующийся в ходе денитрификации N2O является сильным парниковым газом.
49. Современный способ её производства основан на каталитическом окислении синтетического аммиака на платино-родиевых катализаторах (процесс Оствальда) до смеси оксидов азота (нитрозных газов), с дальнейшим поглощением их водой
![]()
![]() Концентрация полученной
таким методом азотной кислоты колеблется
в зависимости от технологического
оформления процесса от 45 до 58 %.
лабораторных
условиях можно получить азотную кислоту,
воздействуя на калийную или натриевую
селитру, то есть на калий или натрий
азотнокислый концентрированной серной
кислотой, при повышеннойтемпературе.
Концентрация полученной
таким методом азотной кислоты колеблется
в зависимости от технологического
оформления процесса от 45 до 58 %.
лабораторных
условиях можно получить азотную кислоту,
воздействуя на калийную или натриевую
селитру, то есть на калий или натрий
азотнокислый концентрированной серной
кислотой, при повышеннойтемпературе.
Реакция идет по такой схеме: NaNO3 + H2SO4 = NaHSO4 + HNO3, азотная кислота выделяется в виде паров, которые улавливают.
50. Перспективно ли получать серную кислоту в лабораторных условиях по реакции SO2 + NO2 = SO3 + NO SO3 + H2O = H2SO4
Сырьём для получения серной кислоты служат сера, сульфиды металлов,сероводород, отходящие газы теплоэлектростанций, сульфаты железа, кальция и д В промышленности применяют два метода окисления SO2 в производстве серной кислоты: контактный — с использованием твердых катализаторов (контактов), и нитрозный (башенный) — с оксидами азота. Контактный способ вытесняет нитрозный.
Ниже приведены реакции по производству серной кислоты из минерала пирита на катализаторе — оксиде ванадия (V).
4FeS2 + 11O2 = 2Fe2O3 + 8SO2
2SO2 + O2 (V2O5) → 2SO3
SO3 + H2O → H2SO4
Нитрозный метод получения серной кислоты
SO2 + NO2 → SO3 + NO↑.
2NO+O2 → 2NO2
Получение серной кислоты (т.н. купоросное масло) из железного купороса - термическое разложение сульфата железа (II) с последующим охлаждением смеси
2FeSO4·7H2O→Fe2O3+SO2+H2O+O2
SO2+H2O+O2 ⇆ H2SO4
51. Галоге́ны (от греч. ἁλός — соль и γένος — рождение, происхождение; иногда употребляется устаревшее название гало́иды) — химические элементы 17-й группы периодической таблицы химических элементов Д.И. Менделеева (по устаревшей классификации — элементы главной подгруппы VII группы)[1].
Реагируют почти со всеми простыми веществами, кроме некоторых неметаллов. Все галогены — энергичные окислители, поэтому встречаются в природе только в виде соединений. С увеличением порядкового номера химическая активность галогенов уменьшается, химическая активность галогенид-ионов F−, Cl−, Br−, I−, At− уменьшается.
К галогенам относятся фтор F, хлор Cl, бром Br, иод I, астат At, а также (формально) искусственный элемент унунсептий Uus.
Фтор является трудносжижаемым, а хлор легкосжижаемым газом с удушливым резким запахом. Энергия связи галогенов сверху вниз по ряду изменяется не равномерно. Фтор имеет аномально низкую энергию связи (151 кДж/моль), это объясняется тем, что фтор не имеет d-подуровня и не способен образовывать полуторные связи, в отличие от остальных галогенов (Cl2 243, Br2 199, I2 150,7, At2 117 кДж/моль). От хлора к астату энергия связи постепенно ослабевает, что связано с увеличением атомного радиуса Все галогены проявляют высокую окислительную активность, которая уменьшается при переходе от фтора к астату. Фтор — самый активный из галогенов, реагирует со всеми металлами без исключения, многие из них в атмосфере фтора самовоспламеняются, выделяя большое количество теплоты, например:
2Al + 3F2 = 2AlF3 + 2989 кДж,
2Fe + 3F2 = 2FeF3 + 1974 кДж.
Без нагревания фтор реагирует и со многими неметаллами (H2, S, С, Si, Р) — все реакции при этом сильно экзотермические
При нагревании фтор окисляет все другие галогены по схеме
Hal2 + F2 = 2НalF
где Hal = Cl, Br, I, At, причем в соединениях HalF степени окисления хлора, брома, иода и астата равны +1.
Наконец, при облучении фтор реагирует даже с инертными (благородными) газами:
Хе + F2 = XeF2 + 152 кДж.
Взаимодействие фтора со сложными веществами также протекает очень энергично. Так, он окисляет воду, при этом реакция носит взрывной характер:
3F2 + ЗН2О = OF2↑ + 4HF + Н2О2.
Особый интерес представляет реакция с водородом. Так, при комнатной температуре, без освещения хлор практически не реагирует с водородом, тогда как при нагревании или при освещении (например, на прямом солнечном свету) эта реакция протекает со взрывом по приведенному ниже цепному механизму:
Cl2 + hν → 2Cl,
Cl + Н2 → HCl + Н,
Н + Cl2 → HCl + Cl,
Cl + Н2 → HCl + Н и т. д.
Хлор способен при нагревании вытеснять бром или иод из их соединений с водородом или металлами:
Cl2 + 2HBr = 2HCl + Br2,
52. d-блок в периодической таблице элементов — электронная оболочкаатомов, валентные электроны которых с наивысшей энергией занимаютd-орбиталь.
Данный блок представляет собой часть периодической таблицы; в него входят элементы от 3 до 12 группы[1][2]. Элементы данного блока заполняют d-оболочку d-электронами, которая у элементов начинается s2d1 (третья группа) и заканчивается s2d10 (двенадцатая группа). Однако существуют некоторые нарушения в этой последовательности, например, у хрома s1d5 (но не s2d4) вся одиннадцатая группа имеет конфигурацию s1d10 (но не s2d9). Одиннадцатая группа имеет заполненные s- и d-электроны.
D-блок-элементы также известны как переходные металлы или переходные элементы. Однако точные границы, отделяющие переходные металлы от остальных групп химических элементов, еще не проведены. Хотя некоторые авторы считают, что элементы, входящие в d-блок, являются переходными элементами[1], в которых d-электроны являются частично заполненными либо в нейтральных атомах или ионах, где степень окисления равна нулю[2][3]. ИЮПАК в данное время принимает такие исследования как достоверные и сообщает, что это относится только к 3—12 группам химических элементов[4]. Металлы 12ойвследствие полного заполнения d-оболочки не соответствуют классическому определению d-элементов, поэтому их можно считать и постпереходными металлами. Также было пересмотрено историческое применение термина «переходные элементы» и d-блока[5].
В s-блоке и p-блоке периодической таблицы аналогичные свойства, через периоды, как правило, не наблюдаются: самые важные свойства усиливаются по вертикали у нижних элементов данных групп. Примечательно, что различия элементов входящих в d-блок по горизонтали, через периоды, становятся более выраженными.
Лютеций и лоуренсий находятся в d-блоке, и они не считаются переходными металлами, но лантаноиды и актиноиды, что примечательно, таковыми считаются с точки зрения ИЮПАК[6]. Двенадцатая группа химических элементов хоть и находится в d-блоке, однако считается, что входящие в неё элементы являются постпереходными элементами[6].
Перехо́дные мета́ллы (перехо́дные элеме́нты) — элементы побочных подгрупп Периодической системы химических элементов Д. И. Менделеева, в атомах которых появляются электроны на d- и f-орбиталях. [1] В общем виде электронное строение переходных элементов можно представить следующим образом:
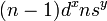 .
На ns-орбитали содержится один или
два электрона,
остальные валентные
электроны находятся
на
.
На ns-орбитали содержится один или
два электрона,
остальные валентные
электроны находятся
на 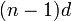 -орбитали.
Поскольку число валентных
электроновзаметно
меньше числа орбиталей, то простые
вещества,
образованные переходными элементами,
являются металлами.
Небольшие значения электроотрицательности.
-орбитали.
Поскольку число валентных
электроновзаметно
меньше числа орбиталей, то простые
вещества,
образованные переходными элементами,
являются металлами.
Небольшие значения электроотрицательности.Переменные степени окисления. Почти для всех d-элементов, в атомах которых на внешнем ns-подуровне находятся 2валентных электрона, известна степень окисления +2.
Начиная с d-элементов III группы Периодической системы химических элементов Д. И. Менделеева, элементы в низшейстепени окисления образуют соединения, которые проявляют основные свойства, в высшей — кислотные, в промежуточной — амфотерные.
54. Желе́зо — элемент побочной подгруппы восьмой группы четвёртого периода периодической системы химических элементовД. И. Менделеева с атомным номером 26. Обозначается символом Fe(лат. Ferrum). Один из самых распространённых в земной коре металлов (второе место после алюминия).
Простое вещество железо (CAS-номер: 7439-89-6) — ковкий металлсеребристо-белого цвета с высокой химической реакционной способностью: железо быстро корродирует при высоких температурах или при высокой влажности на воздухе. В чистом кислороде железо горит, а в мелкодисперсном состоянии самовозгорается и на воздухе.
Собственно, железом обычно называют его сплавы с малым содержанием примесей (до 0,8 %), которые сохраняют мягкость и пластичность чистого металла. Но на практике чаще применяются сплавы железа с углеродом: сталь (до 2,14 вес. % углерода) и чугун(более 2,14 вес. % углерода), а также нержавеющая (легированная) сталь с добавками легирующих металлов (хром, марганец, никель и др.). Совокупность специфических свойств железа и его сплавов делают его «металлом № 1» по важности для человека.
В природе железо редко встречается в чистом виде, чаще всего оно встречается в составе железо-никелевых метеоритов. Распространённость железа в земной коре — 4,65 % (4-е место послеO, Si, Al[2]). Считается также, что железо составляет бо́льшую частьземного ядра.
Оксид железа(II) FeO обладает основными свойствами, ему отвечает основание Fe(OH)2
Оксид железа(III) Fe2O3 слабо амфотерен, ему отвечает ещё более слабое, чем Fe(OH)2, основание Fe(OH)3, которое реагирует с кислотами:
![]()
Ферраты — соли не существующей в свободном виде железной кислоты H2FeO4. Это соединения фиолетового цвета, по окислительным свойствам напоминающие перманганаты, а по растворимости — сульфаты. Получают ферраты при действии газообразного хлора или озона на взвесь Fe(OH)3 в щелочи[20], например, феррат(VI) калия K2FeO4. Ферраты окрашены в фиолетовый цвет.
Ферраты также можно получить электролизом 30%-ного раствора щелочи на железном аноде:
![]()
Ферраты — сильные окислители. В кислой среде разлагаются с выделением кислорода:[21]:
![]()
Имеются сообщения об электрохимическом получении соединений железа(VIII).[22],[23],[24], однако независимых работ, подтверждающих эти результаты, нет.
Железо является основным компонентом сталей и чугунов — важнейшихконструкционных материалов.
Железо может входить в состав сплавов на основе других металлов — например, никелевых.
Магнитная окись железа (магнетит) — важный материал в производстве устройств долговременной компьютерной памяти: жёстких дисков, дискет и т. п.
Ультрадисперсный порошок магнетита используется во многих черно-белыхлазерных принтерах в смеси с полимерными гранулами в качестве тонера. Здесь одновременно используется чёрный цвет магнетита и его способность прилипать к намагниченному валику переноса.
Уникальные ферромагнитные свойства ряда сплавов на основе железа способствуют их широкому применению в электротехнике для магнитопроводов трансформаторов и электродвигателей.
Хлорид железа(III) (хлорное железо) используется в радиолюбительской практике для травления печатных плат.
Семиводный сульфат железа (железный купорос) в смеси с медным купоросом используется для борьбы с вредными грибками в садоводстве и строительстве.
Железо применяется в качестве анода в железо-никелевых аккумуляторах, железо-воздушных аккумуляторах.
Водные растворы хлоридов двухвалентного и трёхвалентного железа, а также его сульфатов используются в качествекоагулянтов в процессах очистки природных и сточных вод на водоподготовке промышленных предприятий.
Медь — элемент побочной подгруппы первой группы, четвёртого периода периодической системы химических элементовД. И. Менделеева, с атомным номером 29. Обозначается символом Cu(лат. Cuprum). Простое вещество медь (CAS-номер: 7440-50-8) — этопластичный переходный металл золотисто-розового цвета (розового цвета при отсутствии оксидной плёнки). C давних пор широко применяется человеком. На влажном воздухе медь окисляется, образуя основный карбонат меди(II):
![]()
Реагирует с концентрированной холодной серной кислотой:
![]()
С концентрированной горячей серной кислотой:
![]()
C разбавленной серной кислотой при нагревании в присутствии кислорода воздуха:
![]()
Реагирует с концентрированной азотной кислотой:
![]()
С разбавленной азотной кислотой:
![]()
С царской водкой:
![]()
C разбавленной хлороводородной кислотой в присутствии кислорода:
![]()
Также медь реагирует с концентрированной уксусной кислотой в присутствии кислорода:
![]()
Медь растворяется в концентрированном гидроксиде аммония, с образованием аммиакатов:
![]()
