- •1.Насосы, применяемые на магистральных нефтепроводах.
- •2.Исходные данные для технологического расчета нефтепроводов.
- •3.Основные расчетные формулы для определения потери напора.
- •4.Гидравлический уклон.
- •5.Перевальная точка и расчетная длина нефтепровода.
- •6.Уравнение баланса напоров.
- •7.Размещение лупингов и пс по трассе нефтепровода.
- •8.Режим работы нефтепровода при сбросах.
- •9.Режим работы нефтепровода при подкачках.
- •10.Состав сооружений и классификация магистральных газопроводов.
- •11.Основные физические свойства газов.
- •12.Влияние изменения температуры газа на производительность газопровода. Необходимость охлаждения газа на кс.
- •13.Коэффициент эффективности газопроводов.
- •14.Типы центробежных нагнетателей и их характеристики.
- •15.Гидраты и борьба с ними.
- •16.Особенности технологии последовательной перекачки нефти и нефтепродуктов.
- •17.Мероприятия по уменьшению смесеобразования при последовательной перекачки нефтепродуктов.
- •18.Характеристика горячего трубопровода.
- •19.Способы перекачки высоковязких нефтей.
- •2. Технико-экономическое обоснование строительства нефтебаз. Обоснование выбора типов и количества резервуаров.
- •Технико-экономические показатели нефтебаз:
- •Грузооборот (тыс.Т/год) и объём реализации нефтепродуктов:
- •Обоснование выбора типов и количества резервуаров.
- •3.Железнодорожные перевозки нефтепродуктов. Типы и устройство железнодорожных эстакад. Устройство для сливоналивных операций.
- •Устройства для сливоналивных операций
- •11. Классификация нефтебаз проводимых технологических операций. Состав сооружений и объектов нефтебаз.
- •Операции, проводимые на нефтебазах
- •Состав сооружений и объектов нефтебаз
- •12.Товарные нефтепродукты и основы их использования. Основные показатели качества топлив (см.1). Номенклатура масел, смазок, область их применения (см.1).
- •Классификация нефтяных топлив (класс f)
- •Классификация нефтепродуктов
- •13.Требования, предъявляемые к площадкам нефтебаз. Этапы разработки проекта нефтебазы.
- •Этапы разработки проекта нефтебазы
- •14.Принцип составления генерального плана нефтебаз. Обоснование выбора типов и количества резервуаров.
- •Обоснование выбора типов и количества резервуаров.
- •15.Типы нефтеналивных судов, их технико-экономические показатели. Технологические схемы слива и налива нефтеналивных судов.
- •Технико-экономические показатели
- •Погрузка и выгрузка танкера:
- •16.Классификация резервуаров, их назначение. Требования, предъявляемые к конструкциям. Оборудование резервуаров для светлых и тёмных нефтепродуктов.
- •Оборудование резервуаров
- •17.Способы учёта нефтепродуктов. Калибровка резервуаров. Автоматизированные системы учёта.
- •Калибровка резервуаров
- •Приборы количественного учёта нефтепродуктов
- •18.Насосные станции нефтебаз. Типы насосов и двигателей, применяемых на нефтебазах. Основные требования по подбору насосов.
- •19.Потери нефти и нефтепродуктов. Источники потерь. Потери от малых и больших «дыханий».
- •Потери при опорожнении и заполнении резервуаров, т.Е. Потери от «больших дыханий»
- •Потери от «малых дыханий»
- •20. Нормы естественной убыли нефти и нефтепродуктов. Методы сокращения потерь. Газоуравнительные системы нефтебаз.
- •Методы сокращения потерь
- •1)Физические свойства нефти и светлых нефтепродуктов: плотность и ее зависимость от температуры и давления. Формулы для расчетов.
- •2) Вязкость жидкостей. Коэффициенты динамической и кинематической вязкости, единицы измерения и их размерность. Понятия о вязко-пластичных жидкостях.
- •3) Деформация трубопровода под действием избыточного давления и температуры. Расчет изменения поперечного сечения и объема трубопровода.
- •4) Нпс. Назначение и классификация нпс. Основные объекты нпс и их назначение.
- •5) Насосные агрегаты, применяемые на нпс магистральных трубопроводов. Основные и подпорные насосы магистральных трубопроводов. Конструкция основных разновидностей насосов. Характеристика насоса.
- •6) Схемы включения насосов на нпс. Принцип получения основной характеристики насосов при различных схемах включения.
- •8) Средства контроля и защиты насосного агрегата. Назначение и составные элементы.
- •9) Резервуарные парки нпс. Назначение и рекомендуемые объемы резервуаров нпс. Конструкции резервуаров и их оснастка.
- •10) Очистка резервуаров от осадков. Оснастка резервуаров системами удаления осадков. Система слива подтоварной воды.
- •11) Учет нефти и нефтепродуктов. Методы и средства измерения количества нефти и нефтепродуктов на нпс. Погрешности измерений.
- •12) Компрессорные станции. Классификация и назначение кс. Основные показатели работы кс.
- •13) Генеральный план кс. Принципы проектирования кс. Основное и вспомогательное оборудование кс.
- •14) Компрессорные станции с поршневыми и центробежными нагнетателями газа. Основные технические параметры поршневых и центробежных нагнетателей газа.
- •15) Компрессорные цеха. Принципы компоновки компрессорных цехов с использованием различного типа нагнетателей газа и их привода.
- •16) Система маслоснабжения компрессорной станции и газоперекачивающих агрегатов. Состав и назначение основных элементов.
- •17) Измерение расхода природного газа. Автоматические расходоизмерительные комплексы на однониточных и многониточных пунктах учета.
- •1.Типы газохранилищ
- •2.Технические характеристики резервуаров.
- •3.Основные сведения о газораспределительных системах и способах хранения газа.
- •4.Газораспределительные станции. Классификация и структура грс.
- •6.(8). Подземные хранилища газа.
- •16.Транспорт сжиженных ув газов.
- •14) Неравномерность газораспределения и методы ее компенсации.
- •13) Хранение и распределение газа.
- •15) Хранение газа в газгольдерах.
- •12) Хранилища, сооружаемые методом глубинных взрывов.
- •11) Газораспределительные сети.
- •5. Хранилища природного газа и газозаправочные станции. Методы компенсации сезонных, суточных и часовых колебаний потребления газа.
- •2.Преимущества и недостатки трубопроводного транспорта
- •3.Составные части системы нефтепроводов
- •4.Составные части системы газопроводов
- •5.Составные части систем продуктопрводов.
- •6.Насосные станции
- •7. Газокомпрессорные станции
- •8.Газораспределительные станции
- •10. Подземные газонефтехранилища
- •11.Подводные и морские трубопроводы
11.Основные физические свойства газов.
Плотность газа (газовой смеси) определяется по правилу аддитивности (пропорционального сложения)
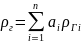 (1)
(1)
где
а.i—
объемная
(мольная) доля i-го
компонента смеси, имеющего плотность
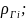 п
—
число компонентов смеси.
п
—
число компонентов смеси.
Согласно уравнению Менделеева — Клапейрона (состояния)

где Р, Т— давление и температура в системе; Z,R — соответственно коэффициент сжимаемости и газовая постоянная смеси.
Различают нормальные (Т = 273,15 К и Р = 0,1013 МПа) и стандартные (Т= 293,15 К и Р=0,1013 МПа) условия.
При нормальных условиях плотность газа можно определить по его молярной массе
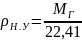
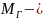 молярная
масса природного газа,кг/кмоль,
молярная
масса природного газа,кг/кмоль,
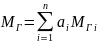 ;
;
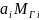 -—
соответственно
объемная доля и молярная масса i-го
компонента;
22,41 — объем одного киломоля газа при
нормальных условиях,
-—
соответственно
объемная доля и молярная масса i-го
компонента;
22,41 — объем одного киломоля газа при
нормальных условиях,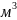 /КМОЛЬ.
/КМОЛЬ.
Пересчет плотности газа с одних параметров состояния (Р*, Т*, Z*) на другие (Р, Т, Z) можно осуществить по формуле
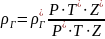
Р*,
Т*, Z*-
соответственно абсолютное давление,
абсолютная температура и коэффициент
сжимаемости, при которых известна
плотность газа
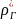 ;
Р,
Т, Z
— аналогичные
параметры, при которых надо определить
плотность
газа
.
;
Р,
Т, Z
— аналогичные
параметры, при которых надо определить
плотность
газа
.
Относительная
плотность газа,
численно
равной отношению плотности газа
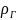 к плотности воздуха
к плотности воздуха
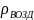 при
одних и тех же условиях
при
одних и тех же условиях
∆=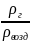
Удобство использования относительной плотности заключается в том, что величина не зависит от давления и температуры.
Газовая постоянная природного газа (Дж/(кг·К)) зависит от состава газовой смеси и вычисляется по формуле
R=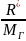
где
R
— универсальная
газовая постоянная,
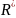 =
8314,3 Дж/(кмоль·К).
=
8314,3 Дж/(кмоль·К).
Критические параметры индивидуальных газов. Состояние индивидуального (однокомпонентного) газа определяется зависимостью между давлением Р, объемом V и температурой Т. Графически эта зависимость может быть изображена семейством изотерм (рис. ).
До точки А- сжатие газа, до В- конденсация газа,с точки В-сжатие конденсата без газовой фазы
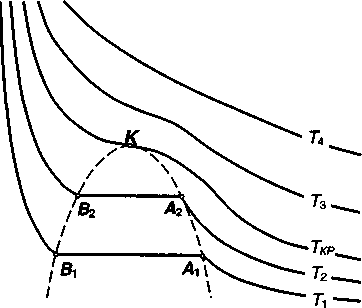
Геометрическое место точек А, В. ограничивает область двухфазного состояния газа. Наивысшая из этих точек (К) соответствует давлению РКР, объему VКР температуре Tкр которые называются критическими. При температуре выше критической газ не переходит в жидкость ни при каких давлениях. И наоборот, при давлении выше критического конденсат не станет газом ни при какой температуре.
Коэффициент сжимаемости учитывает отклонение свойств природного газа от законов идеального газа. Коэффициент сжимаемости г определяется по специальным номограммам в зависимости от приведенных температуры и давления, либо по формуле, рекомендованной отраслевыми нормами проектирования
Z=1-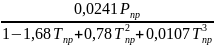
где РПР, ТПР — соответственно приведенные к псевдокритическим условиям значения давления и температуры газа, которые вычисляются по формулам
РПР
=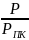 ТПР
=
ТПР
=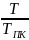
Вязкость газа является мерой внутреннего трения и определяет величину сопротивления при его движении в газопроводе. Величина вязкости газа, как правило, значительно меньше, чем вязкость жидкости, а характер ее изменения в зависимости от температуры и давления является сложным. При низких давлениях с повышением температуры вязкость газа увеличивается, так как возрастает частота столкновения его молекул. При высоких давлениях газ настолько уплотнен, что определяющее влияние на его вязкость, как и у жидкостей, оказывают силы межмолекулярного притяжения, которые с ростом температуры ослабляются, и соответственно, вязкость газа уменьшается.
Различают динамическую и кинематическую вязкости газа.
Динамическая вязкость газа (Па·с) определяется по формуле
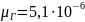 [1
+ ρст(1,1-0,25ρст)]-[0,037+ТПР(1-0,104
ТПР)]х...х[1+
[1
+ ρст(1,1-0,25ρст)]-[0,037+ТПР(1-0,104
ТПР)]х...х[1+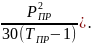
Кинематическая вязкость газа определяется как отношение динамической вязкости к плотности газа при одних и тех же значениях температуры и давления
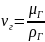
Теплоемкость газа зависит от его состава, давления и температуры. Изобарная теплоемкость (кДж/(кг·К)) природного газа с содержанием метана 85 % и более согласно отраслевым нормам проектирования газопроводов определяется по формуле