
- •1.Теория химического строения органических соединений а.М. Бутлерова
- •2. Строение атома углерода. Типы гибридизаций
- •3,4. Классификация и характеристика органических соединений.
- •III. По типу реагента реакции делятся на:
- •5. Изомерия. Виды изомерии.
- •6. Гомологические ряды органических соединений
- •7. Предельные углеводороды.Номенклатура алканов,изомерия,получение,физические свойства и химические свойства,применение.
- •8. Непредельные углеводороды ряда этилен.
- •9.Диеновые ув.
- •10.Непредельные ув ряда ацителена.
- •11. Ароматические углеводороды (арены)
- •13.Одноатомные спирты
- •14.Водородная связь в кислородосодержащих органических соединениях.
- •15. Многоатомные спирты
- •16. Фенолы
- •17. Альдегиды и их химические свойства
- •18. Одноосновные карбоновые кислоты
- •19. Сложные эфиры
- •20.Амины.
- •21.Аминокислоты
- •22. Гетероциклические соединения.Азотосодержащие орг.Соед….
- •23.Вмс.Мономеры,оигомеры,полимеры.
- •24. По характеру процессов
13.Одноатомные спирты
Спирты (алкоголи) – это производные углеводородов, содержащие в молекуле одну или несколько гидроксильных групп – ОН у насыщенных атомов углерода.
Предельные одноатомные спирты (алканолы). Их основные характеристики: 1) общая формула СnН2n+1ОН, n > 1; 2) атомы углерода и кислорода находятся в состоянии sp3-гибридизации; 3) в молекуле спирта имеются две полярные связи С-О и О-Н: Сδ+-Оδ--Нδ+, для них характерен гетеролитический разрыв связи.
Гомологический ряд: СН3ОН – метанол, СН3СН2ОН – этанол, СН3СН2СН2ОН – пропанол (первичный спирт), СН3СН(ОН)СН3 – изопропанол (вторичный спирт) и т.д.
Изомерия: 1) углеродного скелета; 2) положения ОН-группы; 3) межклассовая (изомерны простым эфиам); 4) оптическая.
Физические свойства. Температуры кипения спиртов больше температуры кипения соответствующих алканов с тем же числом атомов углерода. Это объясняется ассоциацией молекул спиртов вследствие образования межмолекулярных водородных связей.
Прочность ВС значительно меньше прочности ковалентной связи (5-7 ккал/моль), средняя Е образования ковалентной связи – 80-110 ккал/моль.
Образование межмолекулярных ВС между молекулами спирта можно показать так: Н–О: ·∙∙·∙ Н–О: ·∙∙·∙Н–О: (водородная связь изображена точками)
R R R
Химические свойства.
I. Кислотные свойства. Взаимодействие с активными металлами с образованием алкоголятов (алканолятов) металлов:

этанолят натрия
Эти реакции протекают только в безводной среде; в присутствии воды алкоголяты полностью гидролизуются.
II. Реакции нуклеофильного замещения (SN).
1) Взаимодействие с HHal с образованием галогеналканов:
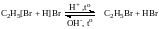
2) Взаимодействие с аммиаком с образованием аминов (300ºС).
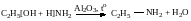
этиламин
III. Нуклеофильные свойства.
Взаимодействие с органическими и неорганическими кислотами с образованием сложных эфиров (реакции этерификации):
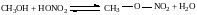
метиловый эфир азотной кислоты (метилнитрат)
IV. Реакции отщепления (Е).
1) Дегидратация спиртов:
Межмолекулярная дегидратация спиртов с образованием простых эфиров R–О–R'. Реакция протекает в присутствии Н2SO4(конц) и при 140ºС:
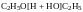 →
→
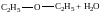
диэтиловый эфир (этоксиэтан)
2) Дегидрирование. При дегидрировании первичных спиртов образуются альдегиды, при дегидрировании вторичных спиртов – кетоны:
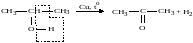
пропанол-2 (ацетон)
Третичные спирты не дегидрируются.
V. Реакции окисления.
1) Горение (полное окисление):
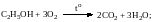 ΔН0 = –1374
кДж
ΔН0 = –1374
кДж
2. Неполное окисление под действием окислителей: кислорода воздуха в присутствии катализаторов (например, Сu), KMnO4, K2Cr2O7 и др. Реакции неполного окисления спиртов по своим результатам аналогичны реакциям дегидрирования.
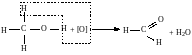
Получение предельных одноатомных спиртов.
1. Гидратация алкенов (H3PO4, 300ºC). При гидратации гомологов этилена образуются вторичные или третичные спирты (прав. Марковникова).
2. Гидролиз галогеналканов (водный раствор NaOH).
3. Гидрирование альдегидов и кетонов в присутствии Ni, Pt, Pd, Co альдегиды восстанавливаются до первичных спиртов, а кетоны – до вторичных.
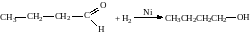
4. Специфические способы получения метанола и этанола:
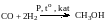
синтез-газ
Брожение (ферментация) углеводов – глюкозы или крахмала:

