
- •Содержание
- •5.2.1 Пример решения задачи 58
- •5.3.1 Пример решения задачи 61
- •10.1. Основные понятия 117
- •Гидромеханика
- •1. Жидкости и их физические свойства
- •1.1 Понятие жидкость
- •1.2 Важнейшие физические свойства жидкости
- •1.2.1 Пример решения задачи
- •1.2.2 Пример решения задачи
- •2. Гидростатика
- •2.1 Гидростатическое давление и его свойства
- •2.2 Дифференциальные уравнения равновесия жидкости
- •2.3 Основное уравнение гидростатики
- •2.4 Основные понятия гидростатики
- •2.4.1 Примеры решения задач
- •2.5 Эпюры гидростатического давления
- •2.5.1 Пример решения задачи
- •2.6 Закон Паскаля
- •2.7 Сила давления жидкости на плоские фигуры
- •2.8 Закон Архимеда
- •2.8.1 Пример решения задачи
- •Контрольные вопросы
- •3. Гидродинамика
- •3.1 Классификация движения
- •3.2 Струйчатое движение
- •3.3 Параметры струйки и потока жидкости
- •3.4 Уравнение неразрывности потока
- •3.5 Уравнение Бернулли для элементарной струйки идеальной жидкости
- •3.6 Трубка Пито
- •3.7 Уравнение Бернулли для элементарной струйки вязкой жидкости
- •3.8 Режимы движения жидкости
- •3.9 Уравнение Бернулли для потока реальной жидкости
- •3.10 Классификация потерь напора
- •3.11 Потери напора по длине
- •3.11.1 Пример решения задачи
- •3.12 Местные потери напора
- •3.12.1 Примеры решения задач
- •Контрольные вопросы
- •4. Истечение жидкости
- •4.1 Основные понятия
- •4.2 Истечение жидкости через отверстия
- •4.2.1 Примеры решения задач
- •4.3 Истечение через насадки
- •4.3.1 Пример решения задачи
- •Контрольные вопросы
- •Методики инженерных расчетов
- •5.1 Классификация трубопроводов и их расчеты
- •5 .2 Расчет сифонов
- •5.2.1 Пример решения задачи
- •5.4 Расчет мощности насосного агрегата
- •5.3.1 Пример решения задачи
- •Контрольные вопросы
- •5.4. Общие указания и задания к расчетно-графической работе
- •Термодинамика
- •6. Основные понятия и определения
- •6.1. Термодинамика
- •6.2. Термодинамические параметры и процессы
- •6.2.1. Термодинамическая система, окружающая среда и рабочее тело
- •6.2.2. Внутренняя энергия термодинамической системы.
- •6.2.3. Первый закон термодинамики
- •6.3. Параметры состояния и уравнение состояния газа
- •6.3.1. Параметры состояния
- •6.3.2. Идеальный газ
- •6.3.3. Основные законы идеальных газов.
- •1.3.4. Уравнение состояния идеального газа
- •Примеры решения задач
- •6.4. Газовые смеси
- •6.5. Теплоёмкость газа
- •6.6. Работа, внутренняя энергия и энтальпия
- •Контрольные вопросы
- •7. Второй закон термодинамики
- •7.1. Основные термодинамические процессы
- •7.1.1. Методика исследования расчета термодинамических процессов
- •7.1.2. Расчеты термодинамических процессов
- •Примеры решения задач
- •7.2. Циклы, понятие термического кпд
- •7.3. Второй закон термодинамики
- •7.4. Цикл Карно
- •Пример решения задачи
- •Контрольные вопросы
- •8. Теплосиловые газовые циклы
- •8.1 Циклы поршневых двигателей внутреннего сгорания
- •8.1.1 Цикл Отто
- •Пример решения задачи
- •8.1.2 Цикл Дизеля
- •Пример решения задачи
- •8.1.3 Цикл Тринклера
- •Пример решения задачи.
- •8.2 Газотурбинные установки
- •8.2.1 Общая характеристика
- •8.2.2 Схема и цикл простейшей гту
- •Пример решения задачи.
- •8.2.3 Способы повышения термодинамического кпд гту
- •Контрольные вопросы
- •9. Теплосиловые паровые циклы
- •9.1. Процесс парообразования и виды пара.
- •9.2 Цикл Ренкина
- •Контрольные вопросы
- •10. Холодильные циклы
- •10.1. Основные понятия
- •10.2 Судовые холодильные установки
- •10.3 Цикл воздушной холодильной установки
- •Контрольные вопросы
- •10.4. Общие указания и задания к расчетно-графической работе
- •Теплопередача
- •11. Общая характеристика процессов теплообмена
- •11.1. Теплопередача
- •11.1.1. Теплоотдача
- •11.1.2.Теплопроводность
- •11.1.3. Лучистый теплообмен
- •Контрольные вопросы
- •12. Основной закон теплопроводности
- •12.1. Температурное поле
- •12.2. Градиент температуры
- •12.3. Закон Фурье
- •12.4. Коэффициент теплопроводности
- •12.5. Теплопроводность плоской стенки
- •12.5.1. Однослойная стенка
- •12.5.2. Многослойная стенка
- •12.5.3. Примеры решения задач
- •12.6. Теплопроводность цилиндрической стенки
- •12.6.1. Однослойная стенка (труба)
- •2.6.2. Многослойная стенка
- •12.6.3. Упрощение расчетных формул
- •12.6.4. Примеры решения задач
- •12.7. Контрольные вопросы
- •13. Конвективный теплообмен
- •13.1. Общие понятия и определения
- •3.2. Основы теории подобия
- •13.3. Теплоотдача при обтекании плоской поверхности (пластины)
- •13.4. Теплоотдача при течении жидкости в трубе
- •3.4.1. Примеры решения задач
- •13.5. Теплоотдача при естественной конвекции
- •13.5.1. Теплоотдача в неограниченном пространстве.
- •13.5.2. Примеры решения задач
- •13.6.Теплоотдача при поперечном обтекании труб
- •13.6.1. Одиночные трубы
- •13.6.2. Поперечное обтекание пучков труб
- •13.6.3. Пример расчета задачи
- •Контрольные вопросы
- •14. Теплообмен при изменении агрегатного состояния
- •14.1. Теплообмен при кипении
- •14.1.1. Примеры решения задач
- •14.2. Теплоотдача при конденсации
- •14.2.1. Общее представление о процессе конденсации
- •14.2.2. Капельная конденсация
- •14.2.3. Теплоотдача при плёночной конденсации
- •14.2.4. Примеры решения задач
- •Контрольные вопросы
- •15. Тепловое излучение (лучистый теплообмен)
- •5.1. Общие сведения
- •15.2. Законы теплового излучения
- •15.3. Лучистый теплообмен между телами
- •15.4. Тепловое излучение газов
- •5.5. Примеры решения задач
- •Контрольные вопросы
- •16. Процессы теплопередачи
- •16.1. Теплопередача через стенки
- •16.1.1. Теплопередача через однослойную плоскую стенку
- •16.1.2. Многослойная плоская стенка
- •16.1.3. Однослойная цилиндрическая стенка (труба)
- •16.1.4. Многослойная цилиндрическая стенка
- •16.1.5. Упрощение расчетных формул
- •16.1.6. Примеры решения задач
- •16.2. Теплопередача через ребристые поверхности
- •16.3. Интенсификация процессов теплообмена
- •Контрольные вопросы
- •17. Общие указания и задания к расчетно-графической работе
- •Вопросы
- •Рекомендуемая литература
- •Основи теплоенергетики
- •65029, М. Одеса, вул.. Дідріхсона, 8.
Контрольные вопросы
Изобразите в pv- и Ts-диаграммах и охарактеризуйте цикл Отто (с подводом тепла при постоянном объеме). Запишите выражение для термического КПД цикла Отто.
Изобразите в pv- и Ts-диаграммах и охарактеризуйте цикл Дизеля (с изобарным подводом тепла). Запишите выражение для термического КПД цикла Дизеля.
Сравните циклы Отто и Дизеля.
Изобразите в pv- и Ts-диаграммах и охарактеризуйте цикл Тринклера (цикл со смешанным подводом теплоты). Как рассчитать термический КПД цикла Тринклера.
Изобразите в pv- и Ts-диаграммах и охарактеризуйте цикл простейшей судовой ГТУ. Запишите выражение для термического КПД.
Опишите способы повышения термического КПД ГТУ.
9. Теплосиловые паровые циклы
9.1. Процесс парообразования и виды пара.
В судовых паровых турбинах, в ядерных реакторах, в различных теплообменных аппаратах в качестве рабочего тела или теплоносителя применяют водяной пар и воду. Их применение обусловлено хорошими термодинамическими свойствами, дешевизной, доступностью и экологической безопасностью.
Переход рабочего тела из жидкого состояния в газообразное (или твердое) называется фазовым переходом. Фазовый переход из жидкого состояния в газообразное называется также парообразованием, а обратный переход из газообразной фазы в жидкую – конденсацией.
Образование пара из воды может происходить в результате двух процессов: испарения и кипения.
Парообразование при испарении происходит с поверхности раздела жидкой и газообразной фаз (со свободной поверхности воды) при любой температуре воды. Часть молекул, обладающих достаточной кинетической энергией, покидает поверхность воды. На преодоление сил притяжения затрачивается работа за счет энергии теплового движения молекул. При этом, если к жидкости не подводится теплота, то температура ее понижается, так как в жидкости остается все меньше молекул, имеющих большой запас кинетической энергии. Когда энергия улетающих молекул уравновесится теплотой, поступающей из окружающей среды, процесс понижения температуры воды прекратится. Если сосуд открыт, пар распространяется в окружающую среду, и испарение будет продолжаться до испарения всей жидкости. В закрытом сосуде наступит динамической равновесие, и количество частиц покидающих жидкость сравнится с количеством частиц, возвращающихся в жидкость за это же время.
Пар, находящийся в динамическом равновесии со своей жидкостью, называется насыщенным. Если к жидкости подводить теплоту, оставляя давление постоянным, то скорость движения молекул будет возрастать и интенсивность парообразования будет увеличиваться при возрастании температуры. Когда температура жидкости достигнет значения температуры насыщения при данном давлении, жидкость начнет кипеть. Кипение – это процесс интенсивного образования пузырьков пара на теплообменной поверхности в жидкости имеющей температуру насыщения. Внешним проявлением кипения является образование большого числа пузырьков на теплообменной поверхности, их отрыв от поверхности и всплытие их, интенсивно перемешивающее толщу воды. Поверхности пузырьков служат границами раздела фаз. Если увеличить подвод теплоты к кипящей жидкости, то парообразование будет протекать интенсивней. Однако температура воды и пара остается постоянной до тех пор, пока последняя капля жидкости не выкипит. Пар, не содержащий в своем составе частиц воды, но имеющий температуру и давление насыщения, называют сухим насыщенным паром.
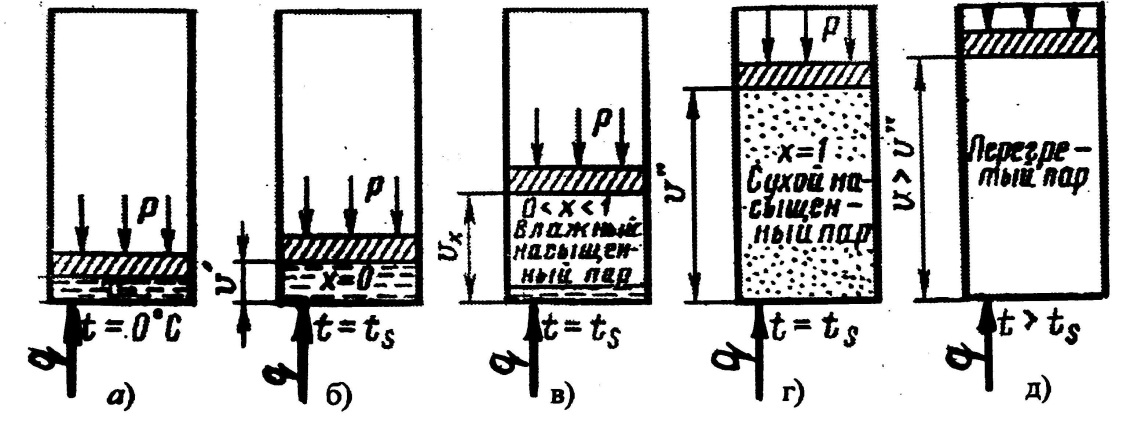
Рис. 9.1 Состояние парожидкостной смеси: а) нагрев жидкости; б) момент начала кипения; в) процесс кипения; г) момент конца кипения – вся жидкость превращена в пар; д) перегрев пара
Относительное количество сухого пара в общей массе, так же как и количество жидкости в процессе парообразования изменяется от нуля до единицы.
Количество сухого насыщенного пара (x) в одном килограмме парожидкостной смеси называется степенью сухости пара и выражается в долях единицы. Влага в этом килограмме парожидкостной смеси соответственно будет (1 – x) кг.
На рис. 9.1 изображено пять состояний парожидкостной смеси в цилиндрическом сосуде. В сосуд, закрытый свободно движущимся поршнем, налито 1 кг воды. Так как масса поршня не меняется, то при подводе к воде теплоты, процессы при этом наблюдаемые будут происходить при постоянном давлении.
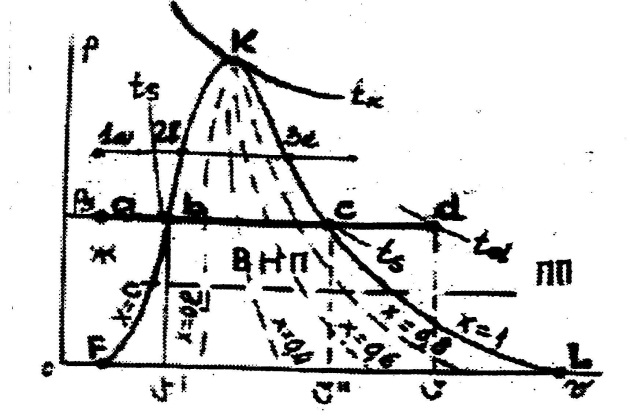
Рис. 9.2 Процесс превращения жидкости в перегретый пар в pv-диаграмме
На
диаграмме p–v (рис.
9.2) состояние воды в начале процесса
отображено точкой a.
Подвод теплоты к воде в этом состоянии
приведет к росту температуры воды, из-за
чего увеличится объем воды (рис. 9.1 б).
Процесс изобарного нагрева окончится
в точке b, (рис. 9.2)
когда температура жидкости достигнет
значения температуры насыщения при
данном давлении. Но так как подвод
теплоты продолжается, жидкость начинает
кипеть, возникает процесс парообразования,
объем парожидкостной смеси увеличивается
за счет объема, образовавшегося пара
(рис. 9.1 в). Объем пара увеличивается,
объем жидкости уменьшается. При этом
температура жидкости и температура
пара остается неизменной и равной
температуре насыщения. Процесс кипения
не только изобарный, но и изотермический
– отрезок b-c
на рис. 9.2. Момент, когда выкипела последняя
капля жидкости, степень сухости пара
![]() ,
в цилиндре находится сухой насыщенный
пар с температурой насыщения, показан
на рис. 9.1 г. Дальнейший подвод тепла при
отсутствии воды приводит к росту
температуры пара – пар становится
перегретым – процесс c-d
на рис. 9.2.
,
в цилиндре находится сухой насыщенный
пар с температурой насыщения, показан
на рис. 9.1 г. Дальнейший подвод тепла при
отсутствии воды приводит к росту
температуры пара – пар становится
перегретым – процесс c-d
на рис. 9.2.
На
диаграмме 9.2 кривая FbK,
называемая левой пограничной кривой,
определяет состояние жидкости, температура
которой доведена до температуры насыщения
(температуры кипения). На этой кривой
пара еще нет и степень сухости его
![]() .
Правая пограничная кривая KcL
соответствует состоянию сухого
насыщенного пара, на этой кривой нет
жидкости, а степень сухости пара x
= 1.
.
Правая пограничная кривая KcL
соответствует состоянию сухого
насыщенного пара, на этой кривой нет
жидкости, а степень сухости пара x
= 1.
Пространство между левой и правой пограничными кривыми – это область парожидкостной смеси, она называется областью влажного насыщенного пара (ВНП).
Область диаграмм левей левой пограничной кривой – это область переохлажденной жидкости, температура которой ниже температуры насыщения. Область правее правой пограничной кривой принадлежит перегретому пару, температура которого выше температуры насыщения. Чем выше температура перегретого пара, тем больше он приближается к идеальному газу.
В области ВНП изобары и изотермы являются горизонтальными прямыми линиями. Диаграммы p–v, T–s, h–s, дают возможность с достаточной степенью точности определить параметры пара, энтальпию, разность энтальпий, наглядно изображать адиабатный процесс, имеющий большое значение при изучении работы двигателей и решать многие другие практические задачи.
Пограничная кривая жидкости (левая) и пограничная кривая пара (правая) смыкаются в точке K. Точка K – критическая точка, в которой фазовый переход происходит без изменения удельного объема и других физических свойств.
Параметры
критической точки воды:![]() МПа,
МПа,
![]() ,
удельный объем
,
удельный объем
![]() м3/кг. За пределами критической
точки между жидкостью и паром нет
разницы. Это гомогенная масса.
м3/кг. За пределами критической
точки между жидкостью и паром нет
разницы. Это гомогенная масса.
